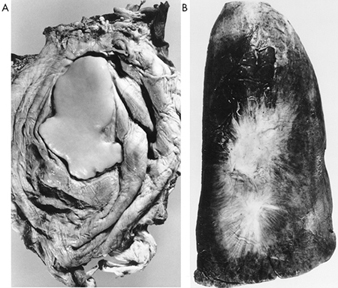
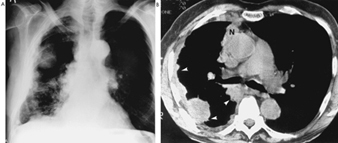
Validitätsprobleme im Studiendesign
Das Bedürfnis nach Geltung
Die Epidemiologie zielt darauf ab, das Krankheitserleben in Bevölkerungen zu verstehen. Insbesondere kann es genutzt werden, um Einblicke in die beruflichen Ursachen von Erkrankungen zu erhalten. Dieses Wissen stammt aus Studien, die an Gruppen von Menschen mit einer Krankheit durchgeführt wurden, indem sie mit Menschen ohne diese Krankheit verglichen wurden. Ein weiterer Ansatz besteht darin, zu untersuchen, welche Krankheiten Menschen bekommen, die in bestimmten Berufen mit besonderen Belastungen arbeiten, und diese Krankheitsbilder mit denen von nicht ähnlich exponierten Personen zu vergleichen. Diese Studien liefern Schätzungen des Krankheitsrisikos für bestimmte Expositionen. Damit Informationen aus solchen Studien zur Erstellung von Präventionsprogrammen, zur Anerkennung von Berufskrankheiten und zur angemessenen Entschädigung der von Expositionen betroffenen Arbeitnehmer verwendet werden können, müssen diese Studien valide sein.
Gültigkeit kann als die Fähigkeit einer Studie definiert werden, den wahren Sachverhalt widerzuspiegeln. Eine gültige Studie ist daher eine Studie, die den Zusammenhang (entweder positiv, negativ oder nicht vorhanden) zwischen einer Exposition und einer Krankheit korrekt misst. Sie beschreibt Richtung und Ausmaß eines echten Risikos. Es werden zwei Arten von Validität unterschieden: interne und externe Validität. Interne Validität ist die Fähigkeit einer Studie, das widerzuspiegeln, was wirklich unter den Studienteilnehmern passiert ist; Die externe Validität spiegelt wider, was in der Bevölkerung passieren könnte.
Validität bezieht sich auf die Wahrhaftigkeit einer Messung. Validität ist von der Genauigkeit der Messung zu unterscheiden, die von der Größe der Studie und der Effizienz des Studiendesigns abhängt.
Interne Gültigkeit
Eine Studie gilt als intern valide, wenn sie frei von Verzerrungen ist und somit den bei den Studienteilnehmern bestehenden Zusammenhang zwischen Exposition und Krankheit wirklich widerspiegelt. Ein beobachtetes Krankheitsrisiko im Zusammenhang mit einer Exposition kann zwar aus einem realen Zusammenhang resultieren und daher valide sein, aber es kann auch den Einfluss von Vorurteilen widerspiegeln. Eine Voreingenommenheit wird ein verzerrtes Bild der Realität geben.
Drei Haupttypen von Vorurteilen, auch genannt systematische Fehler, werden normalerweise unterschieden:
- Auswahlbias
- Informations- oder Beobachtungsverzerrung
- verwirrend
Sie werden im Folgenden anhand von Beispielen aus dem arbeitsmedizinischen Umfeld kurz vorgestellt.
Selektionsvorspannung
Ein Selektionsbias tritt auf, wenn der Eintritt in die Studie durch die Kenntnis des Expositionsstatus des potenziellen Studienteilnehmers beeinflusst wird. Dieses Problem tritt daher nur dann auf, wenn die Krankheit zum Zeitpunkt (bevor) die Person in die Studie aufgenommen wurde, bereits aufgetreten ist. Im epidemiologischen Umfeld geschieht dies typischerweise in Fall-Kontroll-Studien oder in retrospektiven Kohortenstudien. Dies bedeutet, dass eine Person eher als Fall betrachtet wird, wenn bekannt ist, dass sie exponiert war. Drei Umstände können zu einem solchen Ereignis führen, das auch von der Schwere der Krankheit abhängt.
Selbstselektionsverzerrung
Dies kann vorkommen, wenn Personen, die wissen, dass sie in der Vergangenheit bekannten oder vermuteten schädlichen Produkten ausgesetzt waren, und die überzeugt sind, dass ihre Krankheit das Ergebnis der Exposition ist, einen Arzt wegen Symptomen konsultieren, die andere Personen, die nicht so exponiert waren, möglicherweise ignoriert haben. Dies ist besonders wahrscheinlich bei Krankheiten, die nur wenige auffällige Symptome aufweisen. Ein Beispiel kann ein früher Schwangerschaftsverlust oder eine spontane Abtreibung bei weiblichen Krankenschwestern sein, die mit Arzneimitteln zur Krebsbehandlung umgehen. Diese Frauen sind sich der Fortpflanzungsphysiologie bewusster als die meisten anderen und, da sie sich Sorgen um ihre Fähigkeit machen, Kinder zu bekommen, erkennen oder etikettieren sie möglicherweise eher als spontane Abtreibung, was andere Frauen nur als Verzögerung des Beginns der Menstruation betrachten würden. Ein weiteres Beispiel aus einer retrospektiven Kohortenstudie, zitiert von Rothman (1986), betrifft eine Studie des Centers for Disease Control über Leukämie unter Truppen, die bei einem US-Atomtest in Nevada anwesend waren. Von den auf dem Testgelände anwesenden Truppen wurden 76 % aufgespürt und bildeten die Kohorte. Davon wurden 82 % von den Ermittlern gefunden, aber weitere 18 % kontaktierten die Ermittler selbst, nachdem sie von der Öffentlichkeit über die Studie gehört hatten. Vier Fälle von Leukämie waren unter den 82 % vorhanden, die von CDC verfolgt wurden, und vier Fälle waren unter den selbst überwiesenen 18 % vorhanden. Dies deutet stark darauf hin, dass die Fähigkeit der Ermittler, exponierte Personen zu identifizieren, mit dem Leukämie-Risiko zusammenhängt.
Diagnostische Verzerrung
Dies wird der Fall sein, wenn die Ärzte eine bestimmte Krankheit eher diagnostizieren, wenn sie wissen, was der Patient zuvor ausgesetzt war. Als beispielsweise die meisten Farben bleihaltig waren, war ein Symptom einer Erkrankung der peripheren Nerven, das als periphere Neuritis mit Lähmung bezeichnet wird, auch als „Handgelenkstropfen“ der Maler bekannt. Die Kenntnis des Berufs des Patienten erleichterte bereits im Frühstadium die Diagnose der Erkrankung, während bei Studienteilnehmern ohne bekannte berufliche Bleibelastung die Identifizierung des Erregers deutlich erschwert wäre.
Bias aufgrund der Weigerung, an einer Studie teilzunehmen
Wenn Menschen, ob gesund oder krank, gebeten werden, an einer Studie teilzunehmen, spielen mehrere Faktoren eine Rolle, ob sie zustimmen oder nicht. Die Bereitschaft, unterschiedlich lange Fragebögen zu beantworten, die manchmal nach heiklen Themen fragen, und noch mehr, Blut oder andere biologische Proben abzugeben, kann vom Grad des Eigeninteresses der Person bestimmt werden. Jemand, der sich der früheren möglichen Exposition bewusst ist, ist möglicherweise bereit, dieser Anfrage nachzukommen, in der Hoffnung, dass sie dabei hilft, die Ursache der Krankheit zu finden, während jemand der Meinung ist, dass er nichts Gefährlichem ausgesetzt war, oder der nicht interessiert ist wissen, können die Einladung zur Teilnahme an der Studie ablehnen. Dies kann zu einer Auswahl der Personen führen, die letztendlich Studienteilnehmer sein werden, im Vergleich zu allen, die es hätten sein können.
Informationsverzerrung
Dies wird auch als Beobachtungsverzerrung bezeichnet und betrifft den Krankheitsverlauf in Folgestudien und die Expositionsbeurteilung in Fall-Kontroll-Studien.
Differenzielle Ergebnisbewertung in prospektiven Folgestudien (Kohortenstudien).
Zu Beginn der Studie werden zwei Gruppen definiert: eine exponierte Gruppe und eine nicht exponierte Gruppe. Probleme der diagnostischen Verzerrung entstehen, wenn die Suche nach Fällen zwischen diesen beiden Gruppen unterschiedlich ist. Stellen Sie sich zum Beispiel eine Kohorte von Personen vor, die einer versehentlichen Freisetzung von Dioxin in einer bestimmten Branche ausgesetzt sind. Für die hochexponierte Gruppe wird ein aktives Nachsorgesystem mit regelmäßigen ärztlichen Untersuchungen und biologischem Monitoring eingerichtet, während der Rest der Erwerbsbevölkerung nur routinemäßig betreut wird. Es ist sehr wahrscheinlich, dass in der eng überwachten Gruppe mehr Krankheiten identifiziert werden, was zu einer potenziellen Überschätzung des Risikos führen würde.
Differenzielle Verluste in retrospektiven Kohortenstudien
In retrospektiven Kohortenstudien kann der umgekehrte Mechanismus zu dem im vorhergehenden Absatz beschriebenen auftreten. Die übliche Vorgehensweise bei diesen Studien ist, mit den Akten aller Personen zu beginnen, die in der Vergangenheit in einer bestimmten Branche beschäftigt waren, und Krankheit oder Sterblichkeit nach der Beschäftigung zu bewerten. Leider sind in fast allen Studien die Akten unvollständig, und die Tatsache, dass eine Person vermisst wird, kann entweder mit dem Expositionsstatus oder dem Krankheitsstatus oder mit beidem zusammenhängen. Beispielsweise wurden in einer kürzlich in der chemischen Industrie durchgeführten Studie bei Arbeitern, die aromatischen Aminen ausgesetzt waren, acht Tumore in einer Gruppe von 777 Arbeitern gefunden, die einem zytologischen Screening auf Harntumoren unterzogen worden waren. Insgesamt wurden nur 34 Datensätze als fehlend befunden, was einem Verlust von 4.4 % in der Expositionsbewertungsdatei entspricht, aber bei Blasenkrebsfällen fehlten Expositionsdaten für zwei von acht Fällen oder 25 %. Dies zeigt, dass die Akten von Personen, die zu Fällen wurden, mit größerer Wahrscheinlichkeit verloren gingen als die Akten anderer Mitarbeiter. Dies kann durch häufigere Stellenwechsel innerhalb des Unternehmens (die mit Expositionseffekten verbunden sein können), Kündigung, Entlassung oder reinen Zufall geschehen.
Differenzielle Bewertung der Exposition in Fall-Kontroll-Studien
Bei Fall-Kontroll-Studien ist die Erkrankung bei Studienbeginn bereits aufgetreten und es werden Informationen zu früheren Expositionen abgefragt. Voreingenommenheit kann entweder aus der Einstellung des Interviewers oder des Studienteilnehmers zur Untersuchung resultieren. Die Informationen werden normalerweise von geschulten Interviewern gesammelt, die sich der Hypothese, die der Forschung zugrunde liegt, bewusst sein können oder auch nicht. In einer bevölkerungsbezogenen Fall-Kontroll-Studie zu Blasenkrebs beispielsweise, die in einer hochindustrialisierten Region durchgeführt wurde, ist sich das Studienpersonal möglicherweise der Tatsache bewusst, dass bestimmte Chemikalien, wie beispielsweise aromatische Amine, Risikofaktoren für Blasenkrebs sind. Wenn sie auch wissen, wer die Krankheit entwickelt hat und wer nicht, können sie mit den Teilnehmern, die an Blasenkrebs erkrankt sind, wahrscheinlich eingehendere Interviews führen als mit den Kontrollen. Sie bestehen möglicherweise auf detaillierteren Informationen über frühere Berufe und suchen systematisch nach der Exposition gegenüber aromatischen Aminen, während sie für Kontrollen die Berufe eher routinemäßig erfassen. Die resultierende Vorspannung wird als bekannt Expositionsverdacht voreingenommen.
Auch die Teilnehmer selbst können für eine solche Voreingenommenheit verantwortlich sein. Das nennt man Voreingenommenheit erinnern um es von der Voreingenommenheit des Interviewers zu unterscheiden. Beide haben den Expositionsverdacht als Mechanismus für die Voreingenommenheit. Erkrankte Personen können einen beruflichen Ursprung ihrer Krankheit vermuten und werden daher versuchen, sich so genau wie möglich an alle gefährlichen Stoffe zu erinnern, denen sie möglicherweise ausgesetzt waren. Beim Umgang mit undefinierten Produkten neigen sie möglicherweise dazu, sich an die Namen konkreter Chemikalien zu erinnern, insbesondere wenn ihnen eine Liste verdächtiger Produkte zur Verfügung gestellt wird. Im Gegensatz dazu durchlaufen Kontrollen mit geringerer Wahrscheinlichkeit denselben Denkprozess.
Verwirrend
Confounding liegt vor, wenn der beobachtete Zusammenhang zwischen Exposition und Krankheit teilweise das Ergebnis einer Vermischung der Wirkung der untersuchten Exposition und eines anderen Faktors ist. Nehmen wir zum Beispiel an, dass wir bei Schweißern ein erhöhtes Lungenkrebsrisiko feststellen. Wir sind versucht, sofort zu schließen, dass es einen kausalen Zusammenhang zwischen der Exposition gegenüber Schweißrauch und Lungenkrebs gibt. Wir wissen aber auch, dass Rauchen der mit Abstand wichtigste Risikofaktor für Lungenkrebs ist. Wenn Informationen verfügbar sind, beginnen wir daher damit, den Raucherstatus von Schweißern und anderen Studienteilnehmern zu überprüfen. Wir können feststellen, dass Schweißer eher rauchen als Nicht-Schweißer. In dieser Situation ist bekannt, dass das Rauchen mit Lungenkrebs in Verbindung gebracht wird, und gleichzeitig wurde in unserer Studie festgestellt, dass das Rauchen auch mit dem Beruf des Schweißers in Verbindung gebracht wird. In epidemiologischer Hinsicht bedeutet dies, dass Rauchen, das sowohl mit Lungenkrebs als auch mit Schweißen in Verbindung gebracht wird, den Zusammenhang zwischen Schweißen und Lungenkrebs verfälscht.
Interaktions- oder Effektmodifikation
Im Gegensatz zu allen oben aufgeführten Aspekten, nämlich Selektion, Information und Confounding, die Verzerrungen darstellen, ist Interaktion keine Verzerrung aufgrund von Problemen im Studiendesign oder in der Analyse, sondern spiegelt die Realität und ihre Komplexität wider. Ein Beispiel für dieses Phänomen ist das folgende: Die Belastung durch Radon ist ein Risikofaktor für Lungenkrebs, ebenso wie das Rauchen. Darüber hinaus haben Rauchen und Radonexposition unterschiedliche Auswirkungen auf das Lungenkrebsrisiko, je nachdem, ob sie zusammen oder isoliert wirken. Die meisten Berufsstudien zu diesem Thema wurden unter Untertagebergleuten durchgeführt und haben teilweise widersprüchliche Ergebnisse geliefert. Insgesamt scheint es Argumente für eine Wechselwirkung von Rauchen und Radonexposition bei der Entstehung von Lungenkrebs zu geben. Das bedeutet, dass das Lungenkrebsrisiko durch Radonexposition auch bei Nichtrauchern erhöht wird, aber dass die Risikoerhöhung durch Radon bei Rauchern viel größer ist als bei Nichtrauchern. Epidemiologisch sprechen wir von einer multiplikativen Wirkung. Im Gegensatz zum oben beschriebenen Confounding muss die Interaktion sorgfältig analysiert und in der Analyse beschrieben und nicht einfach kontrolliert werden, da sie das widerspiegelt, was auf biologischer Ebene passiert, und nicht nur eine Folge eines schlechten Studiendesigns ist. Seine Erklärung führt zu einer valideren Interpretation der Ergebnisse einer Studie.
Externe Validität
Dieses Problem kann erst behoben werden, nachdem sichergestellt wurde, dass die interne Gültigkeit gesichert ist. Wenn wir davon überzeugt sind, dass die in der Studie beobachteten Ergebnisse reale Assoziationen widerspiegeln, können wir uns fragen, ob wir diese Ergebnisse auf die größere Population, aus der die Studienteilnehmer selbst gezogen wurden, oder sogar auf andere identische Populationen extrapolieren können oder zumindest sehr ähnlich. Die häufigste Frage ist, ob die für Männer erzielten Ergebnisse auch für Frauen gelten. Studien und insbesondere berufsepidemiologische Untersuchungen werden seit Jahren ausschließlich bei Männern durchgeführt. Studien unter Chemikern, die in den 1960er und 1970er Jahren in den Vereinigten Staaten, dem Vereinigten Königreich und Schweden durchgeführt wurden, ergaben alle ein erhöhtes Risiko für bestimmte Krebsarten – nämlich Leukämie, Lymphome und Bauchspeicheldrüsenkrebs. Aus dem, was wir über die Wirkungen der Exposition gegenüber Lösungsmitteln und einigen anderen Chemikalien wussten, hätten wir damals schon ableiten können, dass die Laborarbeit auch ein krebserzeugendes Risiko für Frauen mit sich bringt. Dies zeigte sich tatsächlich, als Mitte der 1980er Jahre schließlich die erste Studie unter Chemikerinnen veröffentlicht wurde, die ähnliche Ergebnisse wie bei Männern ergab. Es ist erwähnenswert, dass es sich bei anderen gefundenen übermäßigen Krebsarten um Tumore der Brust und der Eierstöcke handelte, die traditionell nur mit endogenen Faktoren oder der Fortpflanzung in Verbindung gebracht wurden, bei denen jedoch neu vermutete Umweltfaktoren wie Pestizide eine Rolle spielen könnten. Zu den berufsbedingten Determinanten von Krebserkrankungen bei Frauen muss noch viel mehr Arbeit geleistet werden.
Strategien für ein valides Studium
Eine vollkommen gültige Studie kann es nie geben, aber es obliegt dem Forscher, so viele Verzerrungen wie möglich zu vermeiden oder zumindest zu minimieren. Dies kann oft am besten in der Phase des Studiendesigns erfolgen, kann aber auch während der Analyse durchgeführt werden.
Studiendesign
Auswahl- und Informationsverzerrung können nur durch das sorgfältige Design einer epidemiologischen Studie und die sorgfältige Umsetzung aller sich daraus ergebenden täglichen Richtlinien, einschließlich der sorgfältigen Beachtung der Qualitätssicherung, für die Durchführung der Studie unter Feldbedingungen vermieden werden. Confounding kann entweder in der Entwurfs- oder in der Analysephase behandelt werden.
Auswahl
Kriterien für die Berücksichtigung eines Teilnehmers als Fall müssen explizit definiert werden. Man kann oder sollte zumindest nicht versuchen, schlecht definierte klinische Zustände zu untersuchen. Eine Möglichkeit zur Minimierung der Auswirkungen, die die Kenntnis der Exposition auf die Krankheitsbewertung haben kann, besteht darin, nur schwere Fälle einzubeziehen, die unabhängig von Informationen zur Krankengeschichte des Patienten diagnostiziert worden wären. Im Bereich Krebs werden Studien oft auf Fälle mit histologischem Nachweis der Erkrankung beschränkt, um den Einschluss von Borderline-Läsionen zu vermeiden. Dies bedeutet auch, dass die untersuchten Gruppen gut definiert sind. Beispielsweise ist in der Krebsepidemiologie wohlbekannt, dass Krebsarten verschiedener histologischer Typen innerhalb eines gegebenen Organs unterschiedliche Risikofaktoren haben können. Bei ausreichender Fallzahl ist es besser, das Adenokarzinom der Lunge vom Plattenepithelkarzinom der Lunge zu trennen. Was auch immer die endgültigen Kriterien für die Aufnahme in die Studie sein mögen, sie sollten immer klar definiert und beschrieben werden. Beispielsweise sollte der genaue Code der Krankheit anhand der Internationalen Klassifikation der Krankheiten (ICD) und bei Krebs auch der Internationalen Klassifikation der Krankheiten – Onkologie (ICD-O) angegeben werden.
Sobald die Kriterien festgelegt sind, sollten Anstrengungen unternommen werden, um die Teilnahme an der Studie zu maximieren. Die Entscheidung, eine Teilnahme abzulehnen, wird kaum zufällig getroffen und führt daher zu Voreingenommenheit. Studien sollten zunächst den Klinikern vorgestellt werden, die die Patienten behandeln. Ihre Zustimmung ist erforderlich, um Patienten anzusprechen, und daher müssen sie davon überzeugt werden, die Studie zu unterstützen. Ein oft überzeugendes Argument ist, dass die Studie im Interesse der öffentlichen Gesundheit ist. In diesem Stadium ist es jedoch besser, die genaue zu bewertende Hypothese nicht zu diskutieren, um eine übermäßige Beeinflussung der beteiligten Kliniker zu vermeiden. Ärzte sollten nicht aufgefordert werden, Nebentätigkeiten zu übernehmen; Es ist einfacher, medizinisches Personal davon zu überzeugen, eine Studie zu unterstützen, wenn von den Prüfärzten Mittel bereitgestellt werden, um alle zusätzlichen Aufgaben durchzuführen, die über die Routineversorgung hinausgehen und durch die Studie erforderlich sind. Interviewer und Datenextraktoren sollten den Krankheitsstatus ihrer Patienten nicht kennen.
Ähnliche Aufmerksamkeit sollte den Informationen geschenkt werden, die den Teilnehmern zur Verfügung gestellt werden. Das Ziel der Studie muss breit und neutral beschrieben werden, aber auch überzeugend und überzeugend sein. Es ist wichtig, dass Fragen der Vertraulichkeit und von Interesse für die öffentliche Gesundheit vollständig verstanden werden, während medizinischer Fachjargon vermieden wird. In den meisten Situationen wird der Einsatz von finanziellen oder anderen Anreizen nicht als angemessen erachtet, obwohl eine Entschädigung für alle Kosten bereitgestellt werden sollte, die einem Teilnehmer möglicherweise entstehen. Nicht zuletzt sollte die allgemeine Bevölkerung über ausreichende wissenschaftliche Kenntnisse verfügen, um die Bedeutung solcher Forschung zu verstehen. Sowohl die Vorteile als auch die Risiken der Teilnahme müssen jedem potenziellen Teilnehmer erklärt werden, wenn er Fragebögen ausfüllen und/oder biologische Proben zur Aufbewahrung und/oder Analyse bereitstellen muss. Es sollte kein Zwang angewendet werden, um eine vorherige und vollständig informierte Zustimmung zu erhalten. Bei Studien, die ausschließlich auf Aufzeichnungen basieren, muss die vorherige Zustimmung der für die Wahrung der Vertraulichkeit dieser Aufzeichnungen zuständigen Stellen eingeholt werden. In diesen Fällen kann in der Regel auf die Zustimmung der einzelnen Teilnehmer verzichtet werden. Stattdessen reicht die Zustimmung von Gewerkschafts- und Regierungsbeamten aus. Epidemiologische Untersuchungen bedrohen nicht das Privatleben des Einzelnen, sondern sind ein potenzielles Hilfsmittel zur Verbesserung der Gesundheit der Bevölkerung. Vor der Durchführung einer Studie ist die Zustimmung eines institutionellen Prüfungsausschusses (oder Ethikprüfungsausschusses) erforderlich, und vieles von dem, was oben gesagt wurde, wird von ihm für seine Überprüfung erwartet.
Informationen
In prospektiven Folgestudien müssen die Mittel zur Beurteilung des Krankheits- oder Mortalitätsstatus für exponierte und nicht exponierte Teilnehmer identisch sein. Insbesondere sollte nicht auf unterschiedliche Quellen zurückgegriffen werden, wie z. B. nur die Abfrage in einem zentralen Mortalitätsregister für nicht exponierte Teilnehmer und die Nutzung einer intensiven aktiven Überwachung für exponierte Teilnehmer. Ebenso muss die Todesursache auf streng vergleichbare Weise ermittelt werden. Das bedeutet, wenn ein System verwendet wird, um Zugang zu offiziellen Dokumenten für die nicht exponierte Bevölkerung, die oft die allgemeine Bevölkerung ist, zu erhalten, sollte man niemals planen, noch genauere Informationen durch Krankenakten oder Interviews über die Teilnehmer selbst oder ihre Familien zu erhalten die exponierte Untergruppe.
In retrospektiven Kohortenstudien sollten Anstrengungen unternommen werden, um festzustellen, wie genau die untersuchte Population mit der interessierenden Population verglichen wird. Man sollte sich vor möglichen unterschiedlichen Verlusten in exponierten und nicht exponierten Gruppen hüten, indem man verschiedene Quellen zur Zusammensetzung der Bevölkerung verwendet. Beispielsweise kann es sinnvoll sein, Gehaltslisten mit Gewerkschaftsmitgliedslisten oder anderen Berufsverzeichnissen zu vergleichen. Diskrepanzen müssen ausgeglichen werden, und das für die Studie angenommene Protokoll muss genau befolgt werden.
In Fall-Kontroll-Studien gibt es andere Optionen, um Verzerrungen zu vermeiden. Interviewer, Studienpersonal und Studienteilnehmer müssen sich der genauen zu untersuchenden Hypothese nicht bewusst sein. Wenn sie die getestete Assoziation nicht kennen, ist es weniger wahrscheinlich, dass sie versuchen, die erwartete Antwort zu geben. Das Studienpersonal über die Forschungshypothese im Dunkeln zu lassen, ist tatsächlich oft sehr unpraktisch. Der Interviewer kennt fast immer die Expositionen mit dem größten potenziellen Interesse sowie wer ein Fall und wer eine Kontrolle ist. Wir müssen uns daher auf ihre Ehrlichkeit und auch auf ihre Ausbildung in Grundlagenforschungsmethodik verlassen, die Teil ihres beruflichen Hintergrunds sein sollte; Objektivität ist das Markenzeichen auf allen Stufen der Wissenschaft.
Es ist einfacher, die Studienteilnehmer nicht über den genauen Forschungsgegenstand zu informieren. Gute, grundlegende Erläuterungen zur Notwendigkeit der Erhebung von Daten für ein besseres Verständnis von Gesundheit und Krankheit sind in der Regel ausreichend und genügen den Anforderungen einer Ethikprüfung.
Verwirrend
Confounding ist die einzige Verzerrung, die entweder in der Phase des Studiendesigns oder, sofern angemessene Informationen verfügbar sind, in der Analysephase behandelt werden kann. Wenn zum Beispiel das Alter als potenzieller Confounder der interessierenden Assoziation angesehen wird, weil das Alter mit dem Krankheitsrisiko (d. h. Krebs wird im höheren Alter häufiger) und auch mit der Exposition (Expositionsbedingungen variieren mit dem Alter oder mit altersbedingten Faktoren wie Qualifikation, berufliche Position und Beschäftigungsdauer) gibt es mehrere Lösungsansätze. Am einfachsten ist es, die Studie auf einen bestimmten Altersbereich zu begrenzen – nehmen Sie beispielsweise nur kaukasische Männer im Alter von 40 bis 50 Jahren auf. Dies liefert Elemente für eine einfache Analyse, hat aber auch den Nachteil, dass die Anwendung der Ergebnisse auf einen einzelnen beschränkt wird Geschlecht Alter/Rassengruppe. Eine andere Lösung ist das Matching nach Alter. Das bedeutet, dass für jeden Fall ein gleichaltriger Referent benötigt wird. Dies ist eine attraktive Idee, aber man muss die mögliche Schwierigkeit berücksichtigen, diese Anforderung zu erfüllen, wenn die Anzahl der passenden Faktoren zunimmt. Darüber hinaus wird es nach der Zuordnung eines Faktors unmöglich, seine Rolle beim Auftreten von Krankheiten zu bewerten. Die letzte Lösung besteht darin, genügend Informationen über potenzielle Confounder in der Studiendatenbank zu haben, um sie in der Analyse zu überprüfen. Dies kann entweder durch eine einfache stratifizierte Analyse oder mit ausgefeilteren Tools wie der multivariaten Analyse erfolgen. Es sollte jedoch daran erinnert werden, dass eine Analyse niemals in der Lage sein wird, eine schlecht konzipierte oder durchgeführte Studie zu kompensieren.
Fazit
Das Potenzial für Verzerrungen in der epidemiologischen Forschung ist seit langem bekannt. Dies war kein allzu großes Problem, wenn die untersuchten Assoziationen stark waren (wie dies bei Rauchen und Lungenkrebs der Fall ist) und daher einige Ungenauigkeiten kein allzu schwerwiegendes Problem verursachten. Jetzt, da es an der Zeit ist, schwächere Risikofaktoren zu bewerten, wird der Bedarf an besseren Instrumenten von größter Bedeutung. Dazu gehört die Notwendigkeit exzellenter Studiendesigns und die Möglichkeit, die Vorteile verschiedener traditioneller Designs wie Fall-Kontroll- oder Kohortenstudien mit innovativeren Ansätzen wie in einer Kohorte verschachtelten Fall-Kontroll-Studien zu kombinieren. Außerdem kann die Verwendung von Biomarkern die Möglichkeit bieten, genauere Einschätzungen aktueller und möglicherweise früherer Expositionen sowie für die frühen Krankheitsstadien zu erhalten.
Messung der Auswirkungen von Expositionen
Die Epidemiologie umfasst die Messung des Auftretens von Krankheiten und die Quantifizierung von Zusammenhängen zwischen Krankheiten und Expositionen.
Maßnahmen zum Auftreten von Krankheiten
Das Auftreten von Krankheiten kann gemessen werden durch Frequenzen (zählt), wird aber besser beschrieben durch Preise, die sich aus drei Elementen zusammensetzen: der Anzahl der Betroffenen (Zähler), der Anzahl der Personen in der Ausgangs- bzw. Grundgesamtheit (d. h. der Risikopopulation), aus der die betroffenen Personen stammen, und dem abgedeckten Zeitraum. Der Nenner der Rate ist die gesamte Personenzeit, die von der Quellpopulation erfahren wird. Raten ermöglichen aussagekräftigere Vergleiche zwischen Populationen unterschiedlicher Größe als Zählungen allein. Risiko, die Wahrscheinlichkeit, dass eine Person innerhalb eines bestimmten Zeitraums eine Krankheit entwickelt, ist ein Anteil zwischen 0 und 1 und keine Rate an sich. Angriffsgeschwindigkeit, der Anteil der Personen in einer Bevölkerung, die innerhalb eines bestimmten Zeitraums betroffen sind, ist technisch gesehen ein Risikomaß, keine Rate.
Krankheitsspezifische Morbidität umfasst Häufigkeit, die sich auf die Anzahl der Personen bezieht, bei denen die betreffende Krankheit neu diagnostiziert wird. Prävalenz bezieht sich auf die Anzahl der bestehenden Fälle. Sterblichkeit bezieht sich auf die Zahl der Verstorbenen.
Häufigkeit ist definiert als die Anzahl neu diagnostizierter Fälle innerhalb eines bestimmten Zeitraums, während die Inzidenzrate ist diese Zahl geteilt durch die gesamte Personenzeit, die von der Quellpopulation erfahren wird (Tabelle 1). Bei Krebs werden die Raten normalerweise als jährliche Raten pro 100,000 Personen ausgedrückt. Die Raten für andere häufigere Krankheiten können für eine kleinere Anzahl von Personen ausgedrückt werden. Beispielsweise werden Geburtsfehlerraten normalerweise pro 1,000 Lebendgeburten ausgedrückt. Kumulative Inzidenz, der Anteil der Personen, die innerhalb eines bestimmten Zeitraums zu Fällen werden, ist ein Maß für das durchschnittliche Risiko für eine Bevölkerung.
Tabelle 1. Maße für das Auftreten der Krankheit: Hypothetische Population, die über einen Zeitraum von fünf Jahren beobachtet wurde
|
Neu diagnostizierte Fälle |
10 |
|
Zuvor diagnostizierte lebende Fälle |
12 |
|
Todesfälle, alle Ursachen* |
5 |
|
Todesfälle, Krankheit von Interesse |
3 |
|
Personen in der Bevölkerung |
100 |
|
Jahre beobachtet |
5 |
|
Häufigkeit |
10 Personen |
|
Jährliche Inzidenzrate |
|
|
Punktprävalenz (am Ende des 5. Jahres) |
(10 + 12 - 3) = 19 Personen |
|
Periodenprävalenz (Fünfjahreszeitraum) |
(10 + 12) = 22 Personen |
|
Jährliche Todesrate |
|
|
Jährliche Sterblichkeitsrate |
|
*Um die Berechnungen zu vereinfachen, wird in diesem Beispiel davon ausgegangen, dass alle Todesfälle am Ende des Fünfjahreszeitraums eingetreten sind, sodass alle 100 Personen in der Bevölkerung die vollen fünf Jahre am Leben waren.
Prävalenz Dazu gehören Punkt Prävalenz, die Anzahl der Krankheitsfälle zu einem bestimmten Zeitpunkt und Periodenprävalenz, die Gesamtzahl der Fälle einer Krankheit, von denen bekannt ist, dass sie irgendwann während eines bestimmten Zeitraums aufgetreten sind.
Sterblichkeit, die sich eher auf Todesfälle als auf neu diagnostizierte Krankheitsfälle bezieht, spiegelt Faktoren wider, die Krankheiten verursachen, sowie Faktoren im Zusammenhang mit der Qualität der medizinischen Versorgung, wie z. B. Screening, Zugang zu medizinischer Versorgung und Verfügbarkeit wirksamer Behandlungen. Folglich können hypothesengenerierende Bemühungen und ätiologische Forschung informativer und leichter zu interpretieren sein, wenn sie auf Inzidenzdaten statt auf Mortalitätsdaten basieren. Allerdings sind Sterblichkeitsdaten für große Populationen oft leichter verfügbar als Inzidenzdaten.
Die Todesrate wird allgemein akzeptiert, um die Rate für Todesfälle aus allen Ursachen zusammen zu bezeichnen, wohingegen Sterblichkeitsrate ist die Todesrate aufgrund einer bestimmten Ursache. Für eine bestimmte Krankheit, die Fallsterblichkeitsrate (technisch gesehen ein Anteil, keine Rate) ist die Anzahl der Personen, die während eines bestimmten Zeitraums an der Krankheit sterben, dividiert durch die Anzahl der Personen mit der Krankheit. Das Komplement der Sterblichkeitsrate ist die Überlebensrate. Die Fünf-Jahres-Überlebensrate ist ein allgemeiner Maßstab für chronische Krankheiten wie Krebs.
Das Auftreten einer Krankheit kann zwischen Untergruppen der Bevölkerung oder im Laufe der Zeit variieren. Ein Krankheitsmaß für eine ganze Bevölkerung ohne Berücksichtigung von Untergruppen wird als a bezeichnet Rohsatz. Beispielsweise ist eine Inzidenzrate für alle Altersgruppen zusammen eine grobe Rate. Die Preise für die einzelnen Altersgruppen sind die altersspezifische Tarife. Um zwei oder mehr Populationen mit unterschiedlichen Altersverteilungen zu vergleichen, altersangepasst (oder, altersstandardisiert) Raten sollten für jede Population berechnet werden, indem jede altersspezifische Rate mit dem Prozentsatz der Standardpopulation (z. B. einer der untersuchten Populationen, der US-Bevölkerung von 1970) in dieser Altersgruppe multipliziert und dann über alle Altersgruppen summiert wird eine altersbereinigte Gesamtrate ergeben. Die Tarife können um andere Faktoren als das Alter, wie Rasse, Geschlecht oder Raucherstatus, angepasst werden, wenn die kategoriespezifischen Tarife bekannt sind.
Die Überwachung und Auswertung von deskriptiven Daten kann Hinweise auf die Krankheitsätiologie liefern, Untergruppen mit hohem Risiko identifizieren, die für Interventions- oder Screening-Programme geeignet sein könnten, und Daten über die Wirksamkeit solcher Programme liefern. Zu den Informationsquellen, die für Überwachungstätigkeiten verwendet wurden, gehören Sterbeurkunden, Krankenakten, Krebsregister, andere Krankheitsregister (z. B. Geburtsfehlerregister, Register für Nierenerkrankungen im Endstadium), Verzeichnisse der beruflichen Exposition, Kranken- oder Berufsunfähigkeitsversicherungsunterlagen und Arbeitnehmerentschädigungen Aufzeichnungen.
Maßnahmen der Assoziation
Die Epidemiologie versucht, Faktoren zu identifizieren und zu quantifizieren, die Krankheiten beeinflussen. Im einfachsten Ansatz wird das Auftreten von Krankheiten bei Personen, die einem verdächtigen Faktor ausgesetzt sind, mit dem Auftreten von Personen verglichen, die nicht exponiert sind. Das Ausmaß eines Zusammenhangs zwischen Exposition und Krankheit kann in beiden ausgedrückt werden Absolute or relativ Bedingungen. (Siehe auch „Fallbeispiel: Maßnahmen“).
Absolute Effekte werden gemessen durch Tarifunterschiede und Risikounterschiede (Tabelle 2). EIN Tarifunterschied ist eine Rate minus einer zweiten Rate. Wenn zum Beispiel die Inzidenzrate von Leukämie unter Benzol-exponierten Arbeitern 72 pro 100,000 Personenjahre und die Rate unter nicht exponierten Arbeitern 12 pro 100,000 Personenjahre beträgt, dann beträgt die Ratendifferenz 60 pro 100,000 Personenjahre. EIN Risiko Unterschied ist ein Unterschied in den Risiken oder der kumulativen Inzidenz und kann von -1 bis 1 reichen.
Tabelle 2. Assoziationsmaße für eine Kohortenstudie
|
Projekte |
Personenjahre gefährdet |
Preis pro 100,000 |
|
|
Ausgesetzt |
100 |
20,000 |
500 |
|
Unbelichtet |
200 |
80,000 |
250 |
|
Gesamt |
300 |
100,000 |
300 |
Ratendifferenz (RD) = 500/100,000 - 250/100,000
= 250/100,000 pro Jahr
(146.06/100,000 - 353.94/100,000)*
Ratenverhältnis (oder relatives Risiko) (RR) = ![]()
Zurechenbares Risiko bei Exponierten (ARe) = 100/20,000 - 200/80,000
= 250/100,000 pro Jahr
Zurechenbares Risiko in Prozent der Exponierten (ARe%) =![]()
Bevölkerungsbezogenes Risiko (PAR) = 300/100,000 - 200/80,000
= 50/100,000 pro Jahr
Bevölkerungsbezogenes Risiko in Prozent (PAR%) =
![]()
* In Klammern 95-%-Konfidenzintervalle, berechnet mit den Formeln in den Kästchen.
Relative Effekte basieren auf Quotenverhältnissen oder Risikomaßen statt auf Differenzen. EIN Ratenverhältnis ist das Verhältnis einer Rate in einer Population zu der Rate in einer anderen. Das Ratenverhältnis wurde auch als das bezeichnet Risikoverhältnis, relatives Risiko, relative Rate und Häufigkeit (oder Sterblichkeit) Ratenverhältnis. Das Maß ist dimensionslos und reicht von 0 bis unendlich. Wenn die Rate in zwei Gruppen ähnlich ist (dh es gibt keine Wirkung von der Exposition), die Ratenverhältnis gleich Eins (1) ist. Eine Exposition, die das Risiko erhöht, würde ein Ratenverhältnis größer als eins ergeben, während ein Schutzfaktor ein Verhältnis zwischen 0 und 1 ergeben würde übermäßiges relatives Risiko ist das relative Risiko minus 1. Beispielsweise kann ein relatives Risiko von 1.4 auch als ein zusätzliches relatives Risiko von 40 % ausgedrückt werden.
In Fall-Kontroll-Studien (auch Fall-Referenz-Studien genannt) werden Personen mit Krankheit identifiziert (Fälle) und Personen ohne Krankheit identifiziert (Kontrollen oder Referenzen). Vergangene Expositionen der beiden Gruppen werden verglichen. Die Wahrscheinlichkeit, ein exponierter Fall zu sein, wird mit der Wahrscheinlichkeit, eine exponierte Kontrolle zu sein, verglichen. Vollständige Zählungen der Quellpopulationen von exponierten und nicht exponierten Personen sind nicht verfügbar, daher können keine Krankheitsraten berechnet werden. Stattdessen können die exponierten Fälle durch Berechnung von mit den exponierten Kontrollen verglichen werden relative ChancenOder das Wahrscheinlichkeit (Tisch 3).
Tabelle 3. Assoziationsmaße für Fall-Kontroll-Studien: Exposition gegenüber Holzstaub und Adenokarzinom der Nasenhöhle und der Nasennebenhöhlen
|
Projekte |
Steuergriffe |
|
|
Ausgesetzt |
18 |
55 |
|
Unbelichtet |
5 |
140 |
|
Gesamt |
23 |
195 |
Relative Quoten (Odds Ratio) (OR) = ![]()
Zurechenbares Risiko in Prozent der exponierten (![]() ) =
) = ![]()
Bevölkerungsbezogenes Risiko in Prozent (PAR%) = ![]()
woher ![]() = Anteil der exponierten Kontrollen = 55/195 = 0.28
= Anteil der exponierten Kontrollen = 55/195 = 0.28
* In Klammern 95-%-Konfidenzintervalle, berechnet mit den Formeln im Kasten auf der Rückseite.
Quelle: Adaptiert von Hayes et al. 1986.
Relative Wirkungsmaße werden häufiger als absolute Maße verwendet, um die Stärke eines Zusammenhangs zu beschreiben. Absolute Maße können jedoch einen besseren Hinweis auf die Auswirkungen einer Assoziation auf die öffentliche Gesundheit geben. Ein kleiner relativer Anstieg bei einer häufigen Krankheit wie Herzerkrankungen kann mehr Personen betreffen (großer Risikounterschied) und stärkere Auswirkungen auf die öffentliche Gesundheit haben als ein großer relativer Anstieg (aber kleiner absoluter Unterschied) bei einer seltenen Krankheit wie z Angiosarkom der Leber.
Signifikanztest
Das Testen auf statistische Signifikanz wird häufig an Wirkungsmaßen durchgeführt, um die Wahrscheinlichkeit zu bewerten, dass die beobachtete Wirkung von der Nullhypothese abweicht (dh keine Wirkung). Während viele Studien, insbesondere in anderen Bereichen der biomedizinischen Forschung, ihre Bedeutung zum Ausdruck bringen können p-Werte, typischerweise epidemiologische Studien vorhanden Vertrauensintervalle (CI) (auch genannt Grenzen des Selbstvertrauens). Ein 95-%-Konfidenzintervall ist beispielsweise ein Bereich von Werten für das Effektmaß, das das aus den Studiendaten erhaltene geschätzte Maß und dasjenige umfasst, das mit 95-%-Wahrscheinlichkeit den wahren Wert enthält. Bei Werten außerhalb des Intervalls ist es unwahrscheinlich, dass sie das wahre Maß der Wirkung enthalten. Wenn das KI für ein Ratenverhältnis Eins enthält, gibt es keinen statistisch signifikanten Unterschied zwischen den verglichenen Gruppen.
Konfidenzintervalle sind aussagekräftiger als p-Werte allein. Die Größe eines p-Werts wird durch einen oder beide von zwei Gründen bestimmt. Entweder ist das Assoziationsmaß (z. B. Rate Ratio, Risikodifferenz) groß oder die untersuchten Populationen sind groß. Beispielsweise kann ein kleiner Unterschied in den Krankheitsraten, der in einer großen Population beobachtet wird, zu einem hochsignifikanten p-Wert führen. Aus dem p-Wert allein lassen sich die Gründe für den großen p-Wert nicht erkennen. Konfidenzintervalle ermöglichen es uns jedoch, die beiden Faktoren voneinander zu trennen. Erstens ist die Größe des Effekts durch die Werte des Effektmaßes und die vom Intervall umfassten Zahlen erkennbar. Größere Risikokennzahlen weisen beispielsweise auf eine stärkere Wirkung hin. Zweitens beeinflusst die Größe der Grundgesamtheit die Breite des Konfidenzintervalls. Kleine Populationen mit statistisch instabilen Schätzungen erzeugen breitere Konfidenzintervalle als größere Populationen.
Das zum Ausdrücken der Variabilität der Ergebnisse gewählte Konfidenzniveau (die „statistische Signifikanz“) ist willkürlich, liegt jedoch traditionell bei 95 %, was einem p-Wert von 0.05 entspricht. Ein Konfidenzintervall von 95 % enthält mit einer Wahrscheinlichkeit von 95 % das wahre Maß des Effekts. Gelegentlich werden auch andere Konfidenzniveaus wie 90 % verwendet.
Expositionen können dichotom sein (z. B. exponiert und nicht exponiert) oder können viele Expositionsniveaus beinhalten. Wirkungsmaße (dh Reaktion) können je nach Expositionsgrad variieren. Auswerten Expositions-Antwort Beziehungen ist ein wichtiger Teil der Interpretation epidemiologischer Daten. Das Analogon zur Expositions-Wirkung im Tierversuch ist die „Dosis-Wirkung“. Wenn die Reaktion mit der Expositionshöhe zunimmt, ist ein kausaler Zusammenhang wahrscheinlicher, als wenn kein Trend beobachtet wird. Zu den statistischen Tests zur Bewertung von Expositions-Wirkungs-Beziehungen gehören der Mantel-Erweiterungstest und der Chi-Quadrat-Trendtest.
Standardisierung
Um andere Faktoren als die interessierende primäre Exposition und die Krankheit zu berücksichtigen, können Assoziationsmaße verwendet werden standardisiert B. durch Schichtungs- oder Regressionstechniken. Schichtung bedeutet die Einteilung der Populationen in homogene Gruppen in Bezug auf den Faktor (z. B. Geschlechtsgruppen, Altersgruppen, Rauchergruppen). Risikokennzahlen oder Quotenverhältnisse werden für jede Schicht berechnet und gewichtete Gesamtdurchschnitte der Risikokennzahlen oder Quotenverhältnisse werden berechnet. Diese Gesamtwerte spiegeln den um den Stratifizierungsfaktor bereinigten Zusammenhang zwischen der primären Exposition und der Erkrankung wider, dh den Zusammenhang mit den Effekten des Stratifizierungsfaktors herausgerechnet.
A standardisiertes Ratenverhältnis (SRR) ist das Verhältnis zweier standardisierter Zinssätze. Mit anderen Worten, ein SRR ist ein gewichteter Durchschnitt von schichtspezifischen Ratenverhältnissen, wobei die Gewichtungen für jede Schicht die Personen-Zeit-Verteilung der nicht exponierten oder Bezugsgruppe sind. SRRs für zwei oder mehr Gruppen können verglichen werden, wenn dieselben Gewichte verwendet werden. Konfidenzintervalle können für SRRs wie für Ratenverhältnisse konstruiert werden.
Das standardisierte Sterblichkeitsrate (SMR) ist ein gewichteter Durchschnitt von altersspezifischen Quotenverhältnissen, wobei die Gewichtungen (z. B. Person-Time-at-Risk) von der untersuchten Gruppe und die Quoten von der Referenzpopulation stammen, das Gegenteil der Situation in einer SRR. Die übliche Bezugspopulation ist die allgemeine Bevölkerung, deren Sterblichkeitsraten möglicherweise leicht verfügbar sind und auf großen Zahlen basieren und daher stabiler sind als die Verwendung von Raten aus einer nicht exponierten Kohorte oder Untergruppe der untersuchten Berufsgruppe. Die Verwendung der Gewichte der Kohorte anstelle der Referenzpopulation wird als indirekte Standardisierung bezeichnet. Die SMR ist das Verhältnis der beobachteten Anzahl von Todesfällen in der Kohorte zur erwarteten Anzahl, basierend auf den Raten der Referenzpopulation (das Verhältnis wird zur Darstellung typischerweise mit 100 multipliziert). Wenn kein Zusammenhang besteht, beträgt die SMR 100. Es sollte beachtet werden, dass zwei oder mehr SMRs tendenziell nicht vergleichbar sind, da die Raten von der Referenzpopulation und die Gewichtungen von der Studiengruppe stammen. Diese Nicht-Vergleichbarkeit wird bei der Interpretation epidemiologischer Daten oft vergessen und es können falsche Schlussfolgerungen gezogen werden.
Healthy-Worker-Effekt
Berufskohorten haben sehr häufig eine niedrigere Gesamtmortalität als die allgemeine Bevölkerung, selbst wenn die Arbeitnehmer einem erhöhten Risiko für ausgewählte Todesursachen aufgrund von Expositionen am Arbeitsplatz ausgesetzt sind. Dieses Phänomen, genannt die gesunder Arbeitereffekt, spiegelt die Tatsache wider, dass jede Gruppe von Erwerbstätigen im Durchschnitt wahrscheinlich gesünder ist als die allgemeine Bevölkerung, zu der Arbeitnehmer und Personen gehören, die aufgrund von Krankheiten und Behinderungen nicht arbeiten können. Die Gesamtsterblichkeitsrate in der Allgemeinbevölkerung ist tendenziell höher als die Rate bei Arbeitnehmern. Die Wirkung ist je nach Todesursache unterschiedlich stark. Beispielsweise scheint es bei Krebs im Allgemeinen weniger wichtig zu sein als bei chronisch obstruktiven Lungenerkrankungen. Ein Grund dafür ist, dass sich die meisten Krebserkrankungen wahrscheinlich nicht aus einer Prädisposition für Krebs entwickelt hätten, die der Berufswahl in einem jüngeren Alter zugrunde liegt. Der Gesunde-Arbeiter-Effekt in einer bestimmten Gruppe von Arbeitnehmern nimmt im Laufe der Zeit tendenziell ab.
Proportionale Sterblichkeit
Manchmal ist eine vollständige tabellarische Aufstellung einer Kohorte (dh gefährdete Personenzeit) nicht verfügbar, und es gibt nur Informationen zu den Todesfällen oder einer Teilmenge von Todesfällen in der Kohorte (z. B. Todesfälle unter Rentnern und aktiven Angestellten, aber nicht unter Arbeitnehmern). die ihre Erwerbstätigkeit aufgegeben haben, bevor sie Anspruch auf eine Rente hatten). Die Berechnung von Personenjahren erfordert spezielle Methoden zur Erfassung der Personenzeit, einschließlich Sterbetafelmethoden. Ohne Angaben zur gesamten Personenzeit aller Kohortenmitglieder, unabhängig vom Krankheitsstatus, können SMRs und SRRs nicht berechnet werden. Stattdessen, proportionale Sterblichkeitsverhältnisse (PMRs) verwendet werden. Ein PMR ist das Verhältnis der beobachteten Anzahl von Todesfällen aufgrund einer bestimmten Ursache im Vergleich zu der erwarteten Anzahl, basierend auf dem Anteil der Gesamttodesfälle aufgrund der spezifischen Ursache in der Referenzpopulation, multipliziert mit der Anzahl der Gesamttodesfälle in der Studie Gruppe, multipliziert mit 100.
Da der Anteil der Todesfälle aus allen Todesursachen zusammen 1 (PMR = 100) betragen muss, scheinen einige PMRs zu hoch zu sein, sind aber tatsächlich künstlich aufgeblasen aufgrund echter Defizite bei anderen Todesursachen. In ähnlicher Weise können einige offensichtliche Defizite lediglich tatsächliche Exzesse bei anderen Todesursachen widerspiegeln. Wenn beispielsweise Pestizidausbringer aus der Luft einen großen realen Überschuss an Todesfällen aufgrund von Unfällen haben, kann die mathematische Anforderung, dass der PMR für alle Ursachen zusammen gleich 100 ist, dazu führen, dass die eine oder andere Todesursache mangelhaft erscheint, selbst wenn die Sterblichkeit zu hoch ist. Um dieses potenzielle Problem zu lindern, können Forscher, die sich hauptsächlich für Krebs interessieren, kalkulieren proportionale Krebssterblichkeitsraten (PCMR). PCMRs vergleichen die beobachtete Zahl der Krebstodesfälle mit der erwarteten Zahl basierend auf dem Anteil der gesamten Krebstodesfälle (anstelle aller Todesfälle) für den interessierenden Krebs in der Referenzpopulation multipliziert mit der Gesamtzahl der Krebstodesfälle in der Studiengruppe, multipliziert mit 100. Somit wird die PCMR nicht durch eine Abweichung (Überschuss oder Mangel) bei einer nicht krebsbedingten Todesursache wie Unfällen, Herzerkrankungen oder nicht bösartigen Lungenerkrankungen beeinflusst.
PMR-Studien können besser analysiert werden mit Sterblichkeit Odds Ratios (MORs), wobei die Daten im Wesentlichen so analysiert werden, als ob sie aus einer Fall-Kontroll-Studie stammen würden. Die „Kontrollen“ sind die Todesfälle aus einer Untergruppe aller Todesfälle, von denen angenommen wird, dass sie in keinem Zusammenhang mit der untersuchten Exposition stehen. Wenn beispielsweise das Hauptinteresse der Studie Krebs war, könnten die Sterblichkeitswahrscheinlichkeitsverhältnisse berechnet werden, indem die Exposition bei den Krebstoten mit der Exposition bei den kardiovaskulären Todesfällen verglichen wird. Dieser Ansatz vermeidet wie die PCMR die Probleme mit der PMR, die entstehen, wenn eine Schwankung bei einer Todesursache das offensichtliche Risiko einer anderen beeinflusst, einfach weil die Gesamt-PMR gleich 100 sein muss. Die Wahl der Kontrolltodesursachen ist jedoch kritisch . Wie oben erwähnt, müssen sie nicht mit der Exposition zusammenhängen, aber die mögliche Beziehung zwischen Exposition und Krankheit ist möglicherweise für viele potenzielle Kontrollkrankheiten nicht bekannt.
Zurechenbares Risiko
Es stehen Maßzahlen zur Verfügung, die das Krankheitsausmaß ausdrücken, das einer Exposition zuzuschreiben wäre, wenn der beobachtete Zusammenhang zwischen der Exposition und der Krankheit kausal wäre. Das zurechenbares Risiko im Exponierten (ARe) ist die Krankheitsrate bei den Exponierten minus der Rate bei den Nicht-Exponierten. Da Krankheitsraten in Fall-Kontroll-Studien nicht direkt gemessen werden können, ist der ARe ist nur für Kohortenstudien berechenbar. Eine verwandte, intuitivere Maßnahme, die zurechenbaren Risikoprozentsatz im Exponierten (ARe%), können aus beiden Studiendesigns gewonnen werden. Die ARe% ist der Anteil der in der exponierten Bevölkerung aufgetretenen Fälle, der auf die Exposition zurückzuführen ist (Formel siehe Tabelle 2 und Tabelle 3). Die ARe% ist das Quotenverhältnis (oder Odds Ratio) minus 1, geteilt durch das Quotenverhältnis (oder Odds Ratio), multipliziert mit 100.
Das der Bevölkerung zuzurechnendes Risiko (PAR) und die der Bevölkerung zuzurechnendes Risiko in Prozent (PAR%) oder ätiologische Fraktion, drücken das Ausmaß der Erkrankung in der Gesamtbevölkerung aus, die sich aus exponierten und nicht exponierten Personen zusammensetzt, die auf die Exposition zurückzuführen ist, wenn der beobachtete Zusammenhang kausal ist. Der PAR kann aus Kohortenstudien erhalten werden (Tabelle 28.3) und der PAR% kann sowohl in Kohorten- als auch in Fall-Kontroll-Studien berechnet werden (Tabelle 2 und Tabelle 3).
Repräsentativität
Es gibt mehrere Risikomaße, die beschrieben wurden. Jeder übernimmt zugrunde liegende Methoden zum Zählen von Ereignissen und in die Repräsentanten dieser Ereignisse zu einer definierten Gruppe. Wenn Ergebnisse studienübergreifend verglichen werden, ist ein Verständnis der verwendeten Methoden unerlässlich, um beobachtete Unterschiede zu erklären.
Optionen im Studiendesign
Der Epidemiologe interessiert sich für Beziehungen zwischen Variablen, hauptsächlich Expositions- und Ergebnisvariablen. Typischerweise möchten Epidemiologen feststellen, ob das Auftreten einer Krankheit mit dem Vorhandensein eines bestimmten Erregers (Exposition) in der Bevölkerung zusammenhängt. Die Art und Weise, wie diese Beziehungen untersucht werden, kann sehr unterschiedlich sein. Man kann alle Personen identifizieren, die diesem Agens ausgesetzt sind, und sie nachverfolgen, um das Auftreten der Krankheit zu messen, indem man dieses Auftreten mit dem Auftreten der Krankheit in einer geeigneten, nicht exponierten Population vergleicht. Alternativ kann man einfach unter den Belichteten und Unbelichteten Proben nehmen, ohne eine vollständige Aufzählung von ihnen zu haben. Oder man kann als dritte Alternative alle Personen identifizieren, die in einem definierten Zeitraum eine interessierende Krankheit entwickeln („Fälle“) und eine geeignete Gruppe von krankheitsfreien Personen (eine Stichprobe der Quellpopulation von Fällen) und ermitteln ob sich die Expositionsmuster zwischen den beiden Gruppen unterscheiden. Eine Möglichkeit ist die Nachbeobachtung der Studienteilnehmer (in sogenannten Längsschnittstudien): In dieser Situation besteht eine zeitliche Verzögerung zwischen dem Auftreten der Exposition und dem Ausbruch der Erkrankung. Eine alternative Möglichkeit ist ein Bevölkerungsquerschnitt, bei dem sowohl die Exposition als auch die Erkrankung zum gleichen Zeitpunkt gemessen werden.
In diesem Artikel wird auf die gängigen Studiendesigns – Kohorte, Fall-Referent (Fall-Kontrolle) und Querschnitt – eingegangen. Betrachten Sie als Grundlage für diese Diskussion eine große Viskosefabrik in einer kleinen Stadt. Eine Untersuchung, ob eine Schwefelkohlenstoffbelastung das Risiko für Herz-Kreislauf-Erkrankungen erhöht, wird eingeleitet. Die Untersuchung hat mehrere Gestaltungsmöglichkeiten, einige mehr und andere weniger offensichtlich. Eine erste Strategie besteht darin, alle Arbeiter zu identifizieren, die Schwefelkohlenstoff ausgesetzt waren, und sie auf kardiovaskuläre Mortalität zu verfolgen.
Kohortenstudien
Eine Kohortenstudie umfasst Forschungsteilnehmer, die ein gemeinsames Ereignis teilen, die Exposition. Eine klassische Kohortenstudie identifiziert eine definierte Gruppe von exponierten Personen, und dann werden alle weiterverfolgt und ihre Morbiditäts- und/oder Mortalitätserfahrungen registriert. Neben einer gemeinsamen qualitativen Exposition sollte die Kohorte auch auf andere Weise definiert werden AuswahlkriterienB. Altersgruppe, Geschlecht (männlich oder weiblich oder beides), Mindestdauer und -intensität der Exposition, Freiheit von anderen Expositionen und dergleichen, um die Aussagekraft und Effizienz der Studie zu verbessern. Bei der Aufnahme sollten alle Kohortenmitglieder frei von der zu untersuchenden Krankheit sein, gemäß dem empirischen Kriterienkatalog, der zur Messung der Krankheit verwendet wird.
Wird beispielsweise in der Kohortenstudie zu den Auswirkungen von Schwefelkohlenstoff auf die koronare Morbidität eine koronare Herzkrankheit empirisch als klinischer Infarkt gemessen, müssen diejenigen, die zu Studienbeginn einen Koronarinfarkt in der Vorgeschichte hatten, aus der Kohorte ausgeschlossen werden. Im Gegensatz dazu können elektrokardiographische Anomalien ohne Infarktanamnese akzeptiert werden. Wenn jedoch das Auftreten neuer elektrokardiographischer Veränderungen das empirische Ergebnismaß ist, sollten die Kohortenmitglieder auch normale Elektrokardiogramme zu Studienbeginn haben.
Die Morbidität (in Bezug auf die Inzidenz) oder die Mortalität einer exponierten Kohorte sollte mit einer Referenzkohorte verglichen werden, die der exponierten Kohorte idealerweise in allen relevanten Aspekten, mit Ausnahme der Exposition, so ähnlich wie möglich sein sollte, um das relative Risiko zu bestimmen Krankheit oder Tod durch Exposition. Die Verwendung einer ähnlichen, aber nicht exponierten Kohorte als Anbieter der Referenzerfahrung ist der üblichen (Fehl-)Praxis vorzuziehen, die Morbidität oder Mortalität der exponierten Kohorte mit altersstandardisierten nationalen Zahlen zu vergleichen, da die allgemeine Bevölkerung selbst die meisten nicht erfüllt elementare Anforderungen an die Vergleichsvalidität. Das standardisierte Morbiditäts- (oder Mortalitäts-)Verhältnis (SMR), das sich aus einem solchen Vergleich ergibt, führt normalerweise zu einer Unterschätzung des wahren Risikoverhältnisses, da in der exponierten Kohorte eine Verzerrung auftritt, was zu einer mangelnden Vergleichbarkeit zwischen den beiden Populationen führt. Diese Vergleichsverzerrung wird als „Healthy Worker Effect“ bezeichnet. Es handelt sich jedoch nicht wirklich um einen echten „Effekt“, sondern um eine Verzerrung durch negatives Confounding, das wiederum durch gesundheitsselektive Fluktuation in einer erwerbstätigen Bevölkerung entstanden ist. (Menschen mit schlechter Gesundheit neigen dazu, „exponierte“ Kohorten zu verlassen oder nie in sie einzutreten, da ihr Endziel oft der arbeitslose Teil der Allgemeinbevölkerung ist.)
Denn eine „exponierte“ Kohorte ist nur definiert als eine bestimmte Exposition Wirkungen, die durch diese einzelne Exposition verursacht wurden (oder Mischung von Expositionen) können gleichzeitig studiert werden. Andererseits erlaubt das Kohortendesign die Untersuchung von mehrere Krankheiten gleichzeitig. Man kann auch gleichzeitig verschiedene Manifestationen derselben Krankheit untersuchen – zum Beispiel Angina pectoris, EKG-Veränderungen, klinische Myokardinfarkte und koronare Mortalität. Eine Kohortenstudie ist zwar gut geeignet, um spezifische Hypothesen zu testen (z. B. „Einwirkung von Schwefelkohlenstoff verursacht koronare Herzkrankheit“), liefert aber auch Antworten auf die allgemeinere Frage: „Welche Krankheiten werden durch diese Einwirkung verursacht?“
Beispielsweise werden in einer Kohortenstudie, die das Risiko von Gießereiarbeitern untersucht, an Lungenkrebs zu sterben, die Mortalitätsdaten aus dem nationalen Todesursachenregister bezogen. Obwohl die Studie klären sollte, ob Gießereistaub Lungenkrebs verursacht, gibt die Datenquelle bei gleichem Aufwand auch Auskunft über alle anderen Todesursachen. Daher können gleichzeitig andere mögliche Gesundheitsrisiken untersucht werden.
Der Zeitpunkt einer Kohortenstudie kann entweder retrospektiv (historisch) oder prospektiv (gleichzeitig) sein. In beiden Fällen ist die Designstruktur dieselbe. Eine vollständige Zählung der exponierten Personen erfolgt zu einem bestimmten Zeitpunkt oder Zeitraum, und das Ergebnis wird für alle Personen bis zu einem definierten Endpunkt gemessen. Der Unterschied zwischen prospektiv und retrospektiv liegt im Zeitpunkt der Studie. Wenn rückwirkend, ist der Endpunkt bereits eingetreten; wenn Interessent, muss man darauf warten.
Beim retrospektiven Design wird die Kohorte zu einem bestimmten Zeitpunkt in der Vergangenheit definiert (z. B. diejenigen, die am 1. Januar 1961 exponiert waren oder zwischen 1961 und 1970 eine exponierte Arbeit übernommen haben). Die Morbidität und/oder Mortalität von alle Kohortenmitglieder wird dann bis in die Gegenwart verfolgt. Obwohl „alle“ bedeutet, dass auch die Ausgeschiedenen erfasst werden müssen, ist eine 100-prozentige Erfassung in der Praxis selten zu erreichen. Je vollständiger jedoch das Follow-up ist, desto aussagekräftiger ist die Studie.
Beim prospektiven Design wird die Kohorte zum gegenwärtigen Zeitpunkt oder während eines zukünftigen Zeitraums definiert, und die Morbidität wird dann in die Zukunft verfolgt.
Bei der Durchführung von Kohortenstudien muss genügend Zeit für die Nachverfolgung eingeplant werden, damit die Endpunkte der Bedenken genügend Zeit haben, sich zu manifestieren. Da historische Aufzeichnungen möglicherweise nur für einen kurzen Zeitraum in der Vergangenheit verfügbar sind, ist es manchmal dennoch wünschenswert, diese Datenquelle zu nutzen, da dies bedeutet, dass ein kürzerer Zeitraum der prospektiven Nachverfolgung erforderlich wäre, bevor Ergebnisse aus der Studie vorliegen könnten erhältlich. In diesen Situationen kann eine Kombination aus retrospektivem und prospektivem Kohortenstudiendesign effizient sein. Das allgemeine Layout von Häufigkeitstabellen mit Kohortendaten ist in Tabelle 1 dargestellt.
Tabelle 1. Das allgemeine Layout von Häufigkeitstabellen mit Kohortendaten
|
Komponente der Krankheitsrate |
Exponierte Kohorte |
Nicht exponierte Kohorte |
|
Krankheits- oder Todesfälle |
c1 |
c0 |
|
Anzahl der Personen in der Kohorte |
N1 |
N0 |
Der beobachtete Anteil an Erkrankten in der exponierten Kohorte wird berechnet als:
![]()
und die der Referenzkohorte als:
![]()
Das Ratenverhältnis wird dann ausgedrückt als:

N0 und N1 werden in der Regel in Personen-Zeit-Einheiten und nicht als Anzahl der Personen ausgedrückt die Bevölkerungen. Personenjahre werden für jede Person separat berechnet. Verschiedene Personen treten oft während eines bestimmten Zeitraums in die Kohorte ein, nicht zum selben Zeitpunkt. Daher beginnen ihre Nachverfolgungszeiten zu unterschiedlichen Zeitpunkten. Ebenso sind sie nach ihrem Tod oder nach Eintreten des interessierenden Ereignisses nicht mehr „gefährdet“ und sollten nicht weiterhin Personenjahre zum Nenner beitragen.
Wenn die RR größer als 1 ist, ist die Morbidität der exponierten Kohorte höher als die der Referenzkohorte und umgekehrt. Die RR ist eine Punktschätzung, für die ein Konfidenzintervall (KI) berechnet werden sollte. Je größer die Studie, desto schmaler wird das Konfidenzintervall. Wenn RR = 1 nicht im Konfidenzintervall enthalten ist (z. B. das 95 %-KI 1.4 bis 5.8 beträgt), kann das Ergebnis auf dem gewählten Wahrscheinlichkeitsniveau (in diesem Beispiel α = 0.05) als „statistisch signifikant“ angesehen werden.
Wird die allgemeine Bevölkerung als Referenzbevölkerung verwendet, c0 wird durch die „erwartete“ Zahl ersetzt, E (c1 ), abgeleitet von den altersstandardisierten Morbiditäts- oder Mortalitätsraten dieser Population (dh der Anzahl der Fälle, die in der Kohorte aufgetreten wären, wenn die interessierende Exposition nicht stattgefunden hätte). Dies ergibt das standardisierte Mortalitäts- (oder Morbiditäts-) Verhältnis, SMR. Daher,
![]()
Auch für die SMR sollte ein Konfidenzintervall berechnet werden. Es ist besser, dieses Maß in einer Veröffentlichung anzugeben als einen p-Wert, da statistische Signifikanztests bedeutungslos sind, wenn die allgemeine Bevölkerung die Referenzkategorie ist. Ein solcher Vergleich bringt eine beträchtliche Verzerrung mit sich (die gesunder Arbeitereffekt oben erwähnt) und statistische Signifikanztests, die ursprünglich für die experimentelle Forschung entwickelt wurden, sind bei Vorliegen systematischer Fehler irreführend.
Angenommen, die Frage lautet, ob Quarzstaub Lungenkrebs verursacht. Üblicherweise tritt Quarzstaub zusammen mit anderen Karzinogenen auf – etwa Radon-Tochterprodukte und Dieselabgase in Bergwerken oder polyaromatische Kohlenwasserstoffe in Gießereien. Granitsteinbrüche setzen die Steinarbeiter diesen anderen Karzinogenen nicht aus. Daher wird das Problem am besten unter Steinarbeitern untersucht, die in Granitsteinbrüchen beschäftigt sind.
Nehmen wir dann an, dass alle 2,000 Arbeiter, die zwischen 20 und 1951 in 1960 Steinbrüchen beschäftigt waren, in die Kohorte aufgenommen werden und ihre Krebsinzidenz (alternativ nur Mortalität) ab zehn Jahren nach der ersten Exposition verfolgt wird (um eine Induktionszeit zu ermöglichen) und bis 1990. Dies ist eine 20- bis 30-jährige (je nach Eintrittsjahr) oder, sagen wir, durchschnittlich 25-jährige Nachbeobachtung der Krebsmortalität (oder -morbidität) unter 1,000 der Steinbrucharbeiter, die waren speziell Granitarbeiter. Die Expositionsgeschichte jedes Kohortenmitglieds muss aufgezeichnet werden. Diejenigen, die die Steinbrüche verlassen haben, müssen aufgespürt und ihre spätere Expositionsgeschichte aufgezeichnet werden. In Ländern, in denen alle Einwohner eindeutige Registrierungsnummern haben, ist dies ein einfaches Verfahren, das hauptsächlich durch nationale Datenschutzgesetze geregelt wird. Wo kein solches System existiert, kann es äußerst schwierig sein, Mitarbeiter zu Nachverfolgungszwecken aufzuspüren. Wo entsprechende Todes- oder Krankheitsregister existieren, kann die Sterblichkeit aus allen Ursachen, allen Krebsarten und spezifischen Krebsherden aus dem nationalen Register der Todesursachen abgerufen werden. (Für die Krebssterblichkeit ist das nationale Krebsregister eine bessere Quelle, da es genauere Diagnosen enthält. Außerdem können auch Inzidenz- (oder Morbiditäts-) Daten abgerufen werden.) Die Todesraten (oder Krebsinzidenzraten) können verglichen werden mit „ erwartete Zahlen“, berechnet aus nationalen Raten unter Zugrundelegung der Personenjahre der exponierten Kohorte.
Nehmen wir an, dass 70 tödliche Fälle von Lungenkrebs in der Kohorte gefunden werden, während die erwartete Zahl (die Zahl, die aufgetreten wäre, wenn es keine Exposition gegeben hätte) 35 ist. Dann:
c1 = 70, E (c1) = 35
![]()
Somit ist die SMR = 200, was auf eine zweifache Erhöhung des Risikos, an Lungenkrebs zu sterben, unter den Exponierten hinweist. Wenn detaillierte Expositionsdaten verfügbar sind, kann die Krebssterblichkeit in Abhängigkeit von verschiedenen Latenzzeiten (z. B. 10, 15, 20 Jahre), Arbeit in verschiedenen Arten von Steinbrüchen (verschiedene Granitsorten), verschiedenen historischen Perioden und verschiedenen Expositionen untersucht werden Intensitäten und so weiter. Allerdings lassen sich 70 Fälle nicht in zu viele Kategorien unterteilen, da die Zahl der Fälle für eine statistische Auswertung schnell zu gering wird.
Beide Arten von Kohortendesigns haben Vor- und Nachteile. Eine retrospektive Studie kann in der Regel nur die Mortalität messen, da Daten für mildere Manifestationen meist fehlen. Eine Ausnahme bilden Krebsregister und vielleicht einige andere, wie Schlaganfallregister und Krankenhausentlassungsregister, in denen auch Inzidenzdaten verfügbar sind. Die Bewertung früherer Expositionen ist immer ein Problem, und die Expositionsdaten sind in retrospektiven Studien normalerweise eher schwach. Dies kann zu einer Effektmaskierung führen. Andererseits liegen die Ergebnisse der Studie viel früher vor, da die Fälle bereits aufgetreten sind; in, sagen wir, zwei bis drei Jahren.
Eine prospektive Kohortenstudie kann besser geplant werden, um den Bedürfnissen des Forschers gerecht zu werden, und Expositionsdaten können genau und systematisch gesammelt werden. Es können mehrere unterschiedliche Manifestationen einer Krankheit gemessen werden. Sowohl Expositions- als auch Ergebnismessungen können wiederholt werden, und alle Messungen können standardisiert und ihre Gültigkeit überprüft werden. Wenn die Krankheit jedoch eine lange Latenz hat (wie Krebs), wird viel Zeit – sogar 20 bis 30 Jahre – vergehen müssen, bevor die Ergebnisse der Studie vorliegen können. In dieser Zeit kann viel passieren. Zum Beispiel Fluktuation von Forschern, Verbesserungen der Techniken zur Messung der Exposition, Umbau oder Schließung der für die Untersuchung ausgewählten Anlagen und so weiter. All diese Umstände gefährden den Studienerfolg. Auch die Kosten einer prospektiven Studie sind in der Regel höher als die einer retrospektiven Studie, dies liegt aber meist an der deutlich höheren Anzahl an Messungen (wiederholte Expositionsüberwachung, klinische Untersuchungen etc.) und nicht an der teureren Sterberegistrierung. Deshalb, die Kosten pro Informationseinheit nicht notwendigerweise über die einer retrospektiven Studie hinausgehen. Vor diesem Hintergrund eignen sich prospektive Studien eher für Erkrankungen mit eher kurzer Latenz, die ein kurzes Follow-up erfordern, während retrospektive Studien besser für Erkrankungen mit langer Latenz geeignet sind.
Fallkontrollstudien (oder fallbezogene Studien).
Kommen wir zurück zur Viskosefabrik. Eine retrospektive Kohortenstudie ist möglicherweise nicht durchführbar, wenn die Dienstpläne der exponierten Arbeiter verloren gegangen sind, während eine prospektive Kohortenstudie erst nach sehr langer Zeit solide Ergebnisse liefern würde. Eine Alternative wäre dann der Vergleich zwischen den in der Stadt im Laufe eines definierten Zeitraums an koronarer Herzkrankheit Verstorbenen und einer Stichprobe der Gesamtbevölkerung in der gleichen Altersgruppe.
Das klassische fallkontrollierte (oder fallbezogene) Design basiert auf der Stichprobenziehung aus einer dynamischen (offenen, durch einen Mitgliederwechsel gekennzeichneten) Population. Diese Bevölkerung kann die eines ganzen Landes, eines Bezirks oder einer Gemeinde sein (wie in unserem Beispiel), oder es kann die administrativ definierte Bevölkerung sein, aus der Patienten in ein Krankenhaus aufgenommen werden. Die definierte Population stellt sowohl die Fälle als auch die Kontrollen (oder Referenzen) bereit.
Die Technik besteht darin, alle Fälle der fraglichen Krankheit zu sammeln, die bei a existieren Punkt in der Zeit (häufige Fälle) oder während eines definierten Zeitraums aufgetreten sind Zeit der Zeit (Ereignisfälle). Die Fälle können somit Morbiditäts- oder Mortalitätsregistern entnommen werden oder direkt von Krankenhäusern oder anderen Quellen mit gültiger Diagnostik gesammelt werden. Die Steuerelemente werden als gezeichnet Sample aus derselben Population, entweder aus Nicht-Fällen oder aus der Gesamtpopulation. Eine andere Möglichkeit ist wählen Patienten mit einer anderen Krankheit als Kontrollen, aber dann müssen diese Patienten repräsentativ für die Bevölkerung sein, aus der die Fälle stammen. Für jeden Fall kann es eine oder mehrere Kontrollen (dh Referenten) geben. Der Stichprobenansatz unterscheidet sich von Kohortenstudien, die die gesamte Bevölkerung untersuchen. Es versteht sich von selbst, dass die Vorteile in Bezug auf die geringeren Kosten von Fall-Kontroll-Designs beträchtlich sind, aber es ist wichtig, dass die Stichprobe es ist Vertreter der gesamten Population, aus der die Fälle stammen (dh die „Studienbasis“) – andernfalls kann die Studie verzerrt sein.
Wenn Fälle und Kontrollen identifiziert wurden, werden ihre Expositionsgeschichten durch Fragebögen, Interviews oder in einigen Fällen aus bestehenden Aufzeichnungen (z. B. Gehaltslisten, aus denen Arbeitsverläufe abgeleitet werden können) gesammelt. Die Daten können entweder von den Teilnehmern selbst oder, falls sie verstorben sind, von nahen Angehörigen erhoben werden. Um einen symmetrischen Rückruf zu gewährleisten, ist es wichtig, dass der Anteil von toten und lebenden Fällen und Referenten gleich ist, da nahe Verwandte normalerweise eine weniger detaillierte Expositionsgeschichte als die Teilnehmer selbst angeben. Informationen über das Expositionsmuster bei den Fällen werden mit denen bei den Kontrollen verglichen, was eine Schätzung der Wahrscheinlichkeit (OR), ein indirektes Maß für die Risiko unter den Exponierten, an der Krankheit zu erkranken relativ zu dem der Unbelichteten.
Da das Fall-Kontroll-Design auf den Expositionsinformationen beruht, die von Patienten mit einer bestimmten Krankheit (dh Fällen) zusammen mit einer Stichprobe von nicht erkrankten Personen (dh Kontrollen) aus der Population, aus der die Fälle stammten, erhalten wurden, ist die Verbindung mit Expositionen gegeben kann nur recherchiert werden eine Krankheit. Im Gegensatz dazu ermöglicht dieses Design die gleichzeitige Untersuchung der Wirkung von mehrere unterschiedliche Belichtungen. Die fallbezogene Studie ist gut geeignet, um spezifische Forschungsfragen zu beantworten (z. B. „Wird eine koronare Herzkrankheit durch die Exposition gegenüber Schwefelkohlenstoff verursacht?“), aber sie kann auch helfen, die allgemeinere Frage zu beantworten: „Welche Expositionen können diese Krankheit verursachen? ?”
Die Frage, ob die Exposition gegenüber organischen Lösungsmitteln primären Leberkrebs verursacht, wird (als Beispiel) in Europa aufgeworfen. Fälle von primärem Leberkrebs, einer vergleichsweise seltenen Erkrankung in Europa, werden am besten aus einem nationalen Krebsregister erfasst. Angenommen, alle Krebsfälle, die während drei Jahren auftreten, bilden die Fallserie. Die Bevölkerungsbasis für die Studie ist dann ein dreijähriges Follow-up der gesamten Bevölkerung in dem betreffenden europäischen Land. Die Kontrollen werden als Stichprobe von Personen ohne Leberkrebs aus der gleichen Population gezogen. Aus Gründen der Bequemlichkeit (d. h. dass dieselbe Quelle für die Probenahme der Kontrollen verwendet werden kann) können Patienten mit einer anderen Krebsart, die nicht mit Lösungsmittelexposition in Verbindung steht, als Kontrollen verwendet werden. Dickdarmkrebs hat keinen bekannten Zusammenhang mit Lösungsmittelexposition; daher kann dieser Krebstyp zu den Kontrollen gezählt werden. (Die Verwendung von Krebskontrollen minimiert Erinnerungsverzerrungen, da die Genauigkeit der Anamnese von Fällen und Kontrollen im Durchschnitt symmetrisch ist. Wenn jedoch später ein derzeit unbekannter Zusammenhang zwischen Dickdarmkrebs und Lösungsmittelexposition aufgedeckt würde, würde diese Art der Kontrolle zu Problemen führen eine Unterschätzung des wahren Risikos – keine Übertreibung davon.)
Für jeden Fall von Leberkrebs werden zwei Kontrollen gezogen, um eine größere statistische Aussagekraft zu erreichen. (Man könnte noch mehr Kontrollen ziehen, aber verfügbare Mittel können ein limitierender Faktor sein. Wenn die Mittel nicht begrenzt wären, wären vielleicht bis zu vier Kontrollen optimal. Über vier hinaus gilt das Gesetz des abnehmenden Ertrags.) Nach Einholung einer entsprechenden Erlaubnis von Daten Schutzbehörden, die Fälle und Kontrollen oder ihre nahen Angehörigen werden kontaktiert, in der Regel mittels eines per Post zugesandten Fragebogens, in dem um eine detaillierte Berufsgeschichte mit besonderem Schwerpunkt auf einer chronologischen Liste der Namen aller Arbeitgeber, der Arbeitsabteilungen, der Arbeitsaufgaben in unterschiedlichen Beschäftigungen und die Dauer der Beschäftigung in der jeweiligen Tätigkeit. Diese Daten sind nur schwer von Verwandten zu bekommen; An bestimmte Chemikalien oder Handelsnamen erinnern sich Verwandte jedoch normalerweise nicht gut. Der Fragebogen sollte auch Fragen zu möglichen Stördaten wie Alkoholkonsum, Kontakt mit aflatoxinhaltigen Lebensmitteln und Hepatitis-B- und -C-Infektionen enthalten. Um eine ausreichend hohe Responsequote zu erreichen, werden zwei Reminder im Abstand von drei Wochen an Nicht-Responder versendet. Dies führt in der Regel zu einer endgültigen Rücklaufquote von über 70 %. Die berufliche Vorgeschichte wird dann von einem Arbeitshygieniker überprüft, ohne Kenntnis des Falls oder des Kontrollstatus des Befragten, und die Exposition wird in hohe, mittlere, niedrige, keine und unbekannte Exposition gegenüber Lösungsmitteln eingeteilt. Die zehnjährige Exposition unmittelbar vor der Krebsdiagnose werden nicht berücksichtigt, da es biologisch nicht plausibel ist, dass Karzinogene vom Initiatortyp bei einer so kurzen Latenzzeit die Ursache des Krebses sein können (obwohl Promotoren dies tatsächlich könnten). In diesem Stadium ist es auch möglich, zwischen verschiedenen Arten der Lösungsmittelbelastung zu unterscheiden. Da eine vollständige Erwerbshistorie vorgelegt wurde, ist es auch möglich, andere Expositionen zu untersuchen, obwohl diese in der ursprünglichen Studienhypothese nicht enthalten waren. Odds Ratios können dann für die Exposition gegenüber einem beliebigen Lösungsmittel, bestimmten Lösungsmitteln, Lösungsmittelgemischen, verschiedenen Kategorien der Expositionsintensität und für verschiedene Zeitfenster in Bezug auf die Krebsdiagnose berechnet werden. Es ist ratsam, Personen mit unbekannter Exposition von der Analyse auszuschließen.
Die Fälle und Kontrollen können als Proben entnommen und analysiert werden eigenständige Serie or passende Gruppen. Matching bedeutet, dass Kontrollen für jeden Fall basierend auf bestimmten Merkmalen oder Attributen ausgewählt werden, um Paare (oder Sätze, wenn mehr als eine Kontrolle für jeden Fall ausgewählt wird) zu bilden. Der Abgleich erfolgt normalerweise auf der Grundlage eines oder mehrerer solcher Faktoren, wie Alter, Vitalzustand, Rauchergeschichte, Kalenderzeit der Falldiagnose und dergleichen. In unserem Beispiel werden Fälle und Kontrollen dann nach Alter und Vitalstatus abgeglichen. (Vitalstatus ist wichtig, da Patienten selbst in der Regel eine genauere Expositionsgeschichte angeben als nahe Verwandte, und Symmetrie aus Validitätsgründen unerlässlich ist.) Heute wird empfohlen, beim Matching restriktiv vorzugehen, da dieses Verfahren negative (Effektmaskierung) einführen kann ) verwirrend.
Wenn ein Steuerelement einem Fall zugeordnet ist, wird das Design a genannt Matched-Pair-Design. Vorausgesetzt, die Kosten für die Untersuchung weiterer Kontrollen sind nicht unerschwinglich, verbessert mehr als ein Referent pro Fall die Stabilität der Schätzung des OR, wodurch die Studie größeneffizienter wird.
Die Aufteilung der Ergebnisse einer ungepaarten Fall-Kontroll-Studie ist in Tabelle 2 dargestellt.
Tabelle 2. Musterlayout von Fallkontrolldaten
|
Expositionsklassifizierung |
||
|
Ausgesetzt |
Unbelichtet |
|
|
Projekte |
c1 |
c0 |
|
Nicht-Fälle |
n1 |
n0 |
Aus dieser Tabelle können die Expositionswahrscheinlichkeiten unter den Fällen und die Expositionswahrscheinlichkeiten unter der Population (den Kontrollen) berechnet und geteilt werden, um das Expositionswahrscheinlichkeitsverhältnis OR zu erhalten. Für die Fälle ist die Expositionswahrscheinlichkeit c1 / c0, und für die Kontrollen ist es n1 / n0. Die Abschätzung des OR ist dann:
![]()
Wenn relativ mehr Fälle als Kontrollen exponiert wurden, liegt das OR über 1 und umgekehrt. Konfidenzintervalle müssen für das OR auf die gleiche Weise wie für das RR berechnet und bereitgestellt werden.
Als weiteres Beispiel dient ein arbeitsmedizinisches Zentrum eines großen Unternehmens für 8,000 Mitarbeiter, die einer Vielzahl von Stäuben und anderen chemischen Arbeitsstoffen ausgesetzt sind. Uns interessiert der Zusammenhang zwischen Mischstaubbelastung und chronischer Bronchitis. Die Studie umfasst eine einjährige Nachbeobachtung dieser Population. Als diagnostisches Kriterium für eine chronische Bronchitis haben wir „Morgenhusten und Schleimproduktion für drei Monate in zwei aufeinanderfolgenden Jahren“ festgelegt. Kriterien für eine „positive“ Staubexposition werden vor Studienbeginn festgelegt. Jeder Patient, der das Gesundheitszentrum besucht und diese Kriterien während eines Zeitraums von einem Jahr erfüllt, ist ein Fall, und der nächste Patient, der wegen nicht pulmonaler Probleme ärztlichen Rat einholt, wird als Kontrolle definiert. Angenommen, während des Studienzeitraums werden 100 Fälle und 100 Kontrollen aufgenommen. Es seien 40 Fälle und 15 Kontrollen als staubexponiert einzustufen. Dann
c1 = 40, c0 = 60, n1 = 15 und n0 = 85.
Folglich
![]()
Im vorstehenden Beispiel wurde die Möglichkeit einer Verwechslung nicht berücksichtigt, die aufgrund systematischer Unterschiede zwischen Fällen und Kontrollen in einer Variablen wie dem Alter zu einer Verzerrung des OR führen kann. Eine Möglichkeit, diese Verzerrung zu reduzieren, besteht darin, die Kontrollen den Fällen nach Alter oder anderen verdächtigen Faktoren zuzuordnen. Daraus ergibt sich ein in Tabelle 3 dargestelltes Datenlayout.
Tabelle 3. Layout der Fallkontrolldaten, wenn jedem Fall eine Kontrolle zugeordnet wird
|
Referenten |
||
|
Projekte |
Belichtung (+) |
Belichtung (-) |
|
Belichtung (+) |
f+ + |
f+ - |
|
Belichtung (-) |
f- + |
f- - |
Die Analyse konzentriert sich auf die diskordanten Paare: „Fall exponiert, Kontrolle nicht exponiert“ (f+–); und „Fall unbelichtet, Kontrolle belichtet“ (f–+). Wenn beide Mitglieder eines Paares exponiert oder nicht exponiert sind, wird das Paar nicht berücksichtigt. Das OR in einem Matched-Pair-Studiendesign ist definiert als
![]()
In einer Studie zum Zusammenhang zwischen Nasenkrebs und Holzstaubbelastung gab es insgesamt 164 Fall-Kontroll-Paare. Bei nur einem Paar waren sowohl der Fall als auch die Kontrolle exponiert worden, und bei 150 Paaren waren weder der Fall noch die Kontrolle exponiert worden. Diese Paare werden nicht weiter betrachtet. Das Gehäuse, aber nicht die Kontrolle, wurde in 12 Paaren exponiert, und die Kontrolle, aber nicht das Gehäuse, in einem Paar. Somit,
![]()
und da die Einheit in diesem Intervall nicht enthalten ist, ist das Ergebnis statistisch signifikant – das heißt, es besteht ein statistisch signifikanter Zusammenhang zwischen Nasenkrebs und Holzstaubbelastung.
Fall-Kontroll-Studien sind effizienter als Kohortenstudien, wenn die Krankheit ist selten; sie können tatsächlich die einzige Option bieten. Aber auch Volkskrankheiten können mit dieser Methode untersucht werden. Wenn die Exposition ist selten, eine expositionsbasierte Kohorte ist das bevorzugte oder einzig mögliche epidemiologische Design. Selbstverständlich können auch Kohortenstudien zu gemeinsamen Expositionen durchgeführt werden. Die Wahl zwischen Kohorten- und Fall-Kontroll-Designs, wenn sowohl die Exposition als auch die Erkrankung häufig sind, wird normalerweise unter Berücksichtigung von Validitätserwägungen entschieden.
Da sich Fall-Kontroll-Studien auf retrospektive Expositionsdaten stützen, die normalerweise auf der Erinnerung der Teilnehmer beruhen, ist ihre Schwachstelle die Ungenauigkeit und Rohheit der Expositionsinformationen, was zu einer Effektmaskierung führt nicht differenziell (symmetrische) Fehlklassifizierung des Expositionsstatus. Darüber hinaus kann der Rückruf manchmal zwischen Fällen und Kontrollen asymmetrisch sein, Fälle, von denen normalerweise angenommen wird, dass sie sich „besser“ erinnern (dh Rückrufverzerrung).
Selektive Rückrufe können eine effektverstärkende Verzerrung bewirken Differential (asymmetrische) Fehlklassifizierung des Expositionsstatus. Die Vorteile von Fall-Kontroll-Studien liegen in ihrer Kosteneffektivität und ihrer Fähigkeit, relativ schnell eine Problemlösung zu liefern. Aufgrund der Stichprobenstrategie ermöglichen sie die Untersuchung sehr großer Zielpopulationen (z. B. durch nationale Krebsregister) und erhöhen damit die statistische Aussagekraft der Studie. In Ländern, in denen Datenschutzgesetze oder das Fehlen guter Bevölkerungs- und Morbiditätsregister die Durchführung von Kohortenstudien behindern, können krankenhausbasierte Fall-Kontroll-Studien die einzige praktische Möglichkeit sein, epidemiologische Forschung durchzuführen.
Fall-Kontroll-Stichprobe innerhalb einer Kohorte (verschachtelte Fall-Kontroll-Studiendesigns)
Eine Kohortenstudie kann auch für Stichproben anstelle einer vollständigen Nachverfolgung konzipiert werden. Dieses Design wurde früher als „verschachtelte“ Fall-Kontroll-Studie bezeichnet. Ein Stichprobenansatz innerhalb der Kohorte stellt andere Anforderungen an die Kohorteneignung, da die Vergleiche nun innerhalb derselben Kohorte erfolgen. Dies sollte daher nicht nur stark exponierte Arbeitnehmer, sondern auch weniger exponierte und sogar nicht exponierte Arbeitnehmer umfassen, um eine Versorgung zu gewährleisten Belichtungskontraste in sich. Es ist wichtig, diesen Unterschied in den Zulassungsvoraussetzungen bei der Zusammenstellung der Kohorte zu berücksichtigen. Wenn zuerst eine vollständige Kohortenanalyse an einer Kohorte durchgeführt wird, deren Eignungskriterien auf einer „hohen“ Exposition lagen, und später eine „verschachtelte“ Fall-Kontroll-Studie an derselben Kohorte durchgeführt wird, wird die Studie unempfindlich. Dies führt zu einer Effektmaskierung, da die Belichtungskontraste aufgrund einer fehlenden Variabilität in der Belichtungserfahrung unter den Mitgliedern der Kohorte „absichtlich“ unzureichend sind.
Vorausgesetzt, die Kohorte verfügt über ein breites Spektrum an Expositionserfahrung, ist der verschachtelte Fall-Kontroll-Ansatz jedoch sehr attraktiv. Man fasst alle in der Kohorte auftretenden Fälle über den Nachbeobachtungszeitraum zur Fallserie zusammen, während nur a Sample der Nicht-Fälle wird für die Kontrollreihe gezogen. Die Forscher sammeln dann, wie beim traditionellen Fall-Kontroll-Design, detaillierte Informationen über die Expositionserfahrung, indem sie Fälle und Kontrollen (oder ihre nahen Verwandten) befragen, die Personallisten der Arbeitgeber prüfen, indem sie a Job-Exposure-Matrix, oder durch Kombinieren von zwei oder mehr dieser Ansätze. Die Kontrollen können entweder den Fällen zugeordnet oder als eigenständige Serie behandelt werden.
Der Stichprobenansatz kann im Vergleich zur umfassenden Informationsbeschaffung über jedes Mitglied der Kohorte weniger kostspielig sein. Da insbesondere nur eine Stichprobe von Kontrollen untersucht wird, können mehr Ressourcen für eine detaillierte und genaue Expositionsbewertung für jeden Fall und jede Kontrolle aufgewendet werden. Allerdings herrschen die gleichen statistischen Power-Probleme wie in klassischen Kohortenstudien. Um eine ausreichende statistische Aussagekraft zu erreichen, muss die Kohorte je nach Größe des zu erfassenden Risikos immer eine „ausreichende“ Anzahl exponierter Fälle umfassen.
Querschnittsstudiendesigns
Im wissenschaftlichen Sinne ist ein Querschnittsdesign ein Querschnitt der Studienpopulation ohne zeitliche Berücksichtigung. Sowohl Exposition als auch Morbidität (Prävalenz) werden zum gleichen Zeitpunkt gemessen.
Aus ätiologischer Sicht ist dieses Studiendesign schwach, auch weil es sich nicht um die Inzidenz, sondern um die Prävalenz handelt. Die Prävalenz ist ein zusammengesetztes Maß, das sowohl von der Inzidenz als auch von der Dauer der Krankheit abhängt. Dies schränkt auch den Einsatz von Querschnittsstudien auf lang andauernde Erkrankungen ein. Noch gravierender ist die starke negative Verzerrung, die durch die gesundheitsbedingte Eliminierung der gegenüber Expositionswirkungen empfindlicheren Personen aus der exponierten Gruppe verursacht wird. Daher werden ätiologische Probleme am besten durch Längsschnittdesigns gelöst. Tatsächlich lassen Querschnittsstudien keine Rückschlüsse darauf zu, ob eine Exposition einer Erkrankung vorausging oder umgekehrt. Der Wirkungsquerschnitt ist nur dann ätiologisch aussagekräftig, wenn zwischen der Exposition und dem Ergebnis ein echter zeitlicher Zusammenhang besteht, das heißt, dass die aktuelle Exposition unmittelbare Auswirkungen haben muss. Die Exposition kann jedoch querschnittlich gemessen werden, so dass sie einen längeren vergangenen Zeitraum darstellt (z. B. der Blutbleispiegel), während das Ergebnismaß eine Prävalenz ist (z. B. Nervenleitungsgeschwindigkeiten). Die Studie ist dann eher eine Mischung aus einem Längsschnitt- und einem Querschnittsdesign als ein bloßer Querschnitt der Studienpopulation.
Deskriptive Querschnittsbefragungen
Querschnittserhebungen sind oft eher für praktische und administrative als für wissenschaftliche Zwecke nützlich. Epidemiologische Prinzipien können auf systematische Überwachungsaktivitäten im arbeitsmedizinischen Umfeld angewendet werden, wie zum Beispiel:
- Beobachtung der Morbidität in Bezug auf Beruf, Arbeitsbereich oder bestimmte Expositionen
- regelmäßige Befragungen von Arbeitnehmern, die bekannten Berufsgefahren ausgesetzt sind
- Untersuchung von Arbeitnehmern, die mit neuen Gesundheitsgefahren in Kontakt kommen
- biologische Überwachungsprogramme
- Expositionserhebungen zur Identifizierung und Quantifizierung von Gefahren
- Screening-Programme verschiedener Arbeitnehmergruppen
- Bewertung des Anteils der Arbeitnehmer, die einer Vorbeugung oder regelmäßigen Kontrolle bedürfen (z. B. Blutdruck, koronare Herzkrankheit).
Es ist wichtig, repräsentative, gültige und spezifische Morbiditätsindikatoren für alle Arten von Erhebungen auszuwählen. Eine Befragung oder ein Screening-Programm kann im Gegensatz zur klinischen Diagnostik nur wenige Tests verwenden, daher ist der Vorhersagewert des Screening-Tests wichtig. Unempfindliche Methoden können die interessierende Krankheit nicht nachweisen, während hochempfindliche Methoden zu viele falsch positive Ergebnisse liefern. Ein Screening auf seltene Erkrankungen ist im beruflichen Umfeld nicht sinnvoll. Alle Aktivitäten zur Fallfindung (dh Screening) erfordern auch einen Mechanismus zur Betreuung von Personen mit „positiven“ Befunden, sowohl in Bezug auf Diagnostik als auch Therapie. Andernfalls wird nur Frustration resultieren, bei der möglicherweise mehr Schaden als Nutzen entsteht.
Berufsbedingt erworbene Lungeninfektionen
Obwohl epidemiologische Studien zur beruflich erworbenen Pneumonie (OAP) begrenzt sind, nimmt man an, dass die Häufigkeit arbeitsbedingter Lungeninfektionen weltweit zurückgeht. Im Gegensatz dazu könnten Rentner in Industrienationen in Berufen zunehmen, die mit der biomedizinischen Forschung oder dem Gesundheitswesen verbunden sind. OAP bei Krankenhausangestellten spiegelt weitgehend die vorherrschenden ambulant erworbenen Krankheitserreger wider, aber das Wiederauftreten von Tuberkulose, Masern und Keuchhusten im Gesundheitswesen stellt ein zusätzliches Risiko für Gesundheitsberufe dar. In Entwicklungsländern und in bestimmten Berufen in entwickelten Ländern verursachen einzigartige infektiöse Krankheitserreger, die normalerweise nicht in der Gemeinschaft zirkulieren, viele OAPs.
Es kann schwierig sein, eine Infektion eher einer beruflichen als einer gemeinschaftlichen Exposition zuzuschreiben, insbesondere für Krankenhausmitarbeiter. In der Vergangenheit wurde ein Berufsrisiko nur in Situationen sicher dokumentiert, in denen Arbeitnehmer mit Erregern infiziert wurden, die am Arbeitsplatz vorkamen, aber nicht in der Gemeinschaft vorhanden waren. In Zukunft wird der Einsatz molekularer Techniken zur Verfolgung spezifischer mikrobieller Klone am Arbeitsplatz und in den Gemeinden die Risikobestimmungen klarer machen.
Wie die ambulant erworbene Pneumonie resultiert OAP aus der Mikroaspiration von Bakterien, die den Oropharynx besiedeln, der Inhalation lungengängiger infektiöser Partikel oder der hämatogenen Aussaat der Lunge. Die meisten ambulant erworbenen Lungenentzündungen resultieren aus Mikroaspiration, aber OAP ist normalerweise auf das Einatmen von infektiösen 0.5 bis 10 μm großen Partikeln in der Luft am Arbeitsplatz zurückzuführen. Größere Partikel erreichen die Alveolen aufgrund von Impaktion oder Sedimentation an den Wänden der großen Atemwege nicht und werden anschließend entfernt. Kleinere Partikel bleiben während des Inspirations- und Exspirationsflusses suspendiert und werden selten in den Alveolen abgelagert. Bei einigen Krankheiten, wie z. B. dem hämorrhagischen Fieber mit Nierensyndrom in Verbindung mit einer Hantavirus-Infektion, ist der Hauptübertragungsweg die Inhalation, aber der primäre Krankheitsherd ist möglicherweise nicht die Lunge. Beruflich erworbene Erreger, die nicht durch Inhalation übertragen werden, können sekundär die Lunge betreffen, werden hier aber nicht behandelt.
In dieser Übersicht werden einige der wichtigsten beruflich erworbenen Krankheitserreger kurz diskutiert. Eine ausführlichere Liste beruflich erworbener Lungenerkrankungen, klassifiziert nach spezifischen Ätiologien, ist in Tabelle 1 dargestellt.
Tabelle 1. Beruflich erworbene Infektionskrankheiten, übertragen durch Mikroaspiration oder Inhalation infektiöser Partikel
|
Krankheit (Erreger) |
Reservoir |
Risikopopulationen |
|
Bakterien, Chlamydien, Mykoplasmen und Rickettsien |
||
|
Brucellose (Brucella spp.) |
Vieh (Rinder, Ziegen, Schweine) |
Tierpfleger, Landarbeiter, Laborarbeiter, Schlachthofarbeiter |
|
Milzbrand beim Einatmen (Bacillus Anthracis) |
Tierische Produkte (Wolle, Häute) |
Landarbeiter, Gerber, Schlachthofarbeiter, Textilarbeiter, Laboranten |
|
Lungenpest (Yersinia pestis) |
Wilde Nagetiere |
Veterinärpfleger, Jäger/Fallensteller, Labormitarbeiter |
|
Keuchhusten (Bordatella pertussis) |
Humans |
Mitarbeiter von Pflegeheimen, medizinisches Personal |
|
Legionärskrankheit (Legionella spp.) |
Kontaminierte Wasserquellen (z. B. Kühltürme, Verdampferkondensatoren) |
Mitarbeiter im Gesundheitswesen, Labormitarbeiter, Industrielabormitarbeiter, Brunnenbagger |
|
Melioidose (Pseudomonas pseudomallei) |
Erde, stehendes Wasser, Reisfelder |
Militärpersonal, Landarbeiter |
|
Streptococcus pneumoniae |
Humans |
Beschäftigte im Gesundheitswesen, Landarbeiter, unterirdische Bergleute |
|
Neisseria meningitidis |
Humans |
Mitarbeiter des Gesundheitswesens, Labormitarbeiter, Militärpersonal |
|
Pasteurellose (Pasteurella multocida) |
Vielzahl von domestizierten (Katzen, Hunden) und wilden Tieren |
Landarbeiter, Tierpfleger |
|
Respiratorische Tularämie (Francisella tularensis) |
Wilde Nagetiere und Kaninchen |
Arbeiter, Militärangehörige, Laboranten, Jäger/Fallensteller, Landarbeiter |
|
Ornithose (Chlamydia psittaci) |
Vögel |
Arbeiter in Zoohandlungen, Arbeiter in der Geflügelproduktion, Tierpfleger, Laborarbeiter |
|
TWAR-Pneumonie (Chlamydia pneumoniae) |
Humans |
Mitarbeiter des Gesundheitswesens, Militärpersonal |
|
Q-Fieber (Coxiella burnetii) |
Haustiere (Rinder, Schafe, Ziegen) |
Laboranten, Textilarbeiter, Schlachthofarbeiter, Milchvieharbeiter, Tierpfleger |
|
Atypische Pneumonie (Mycoplasma pneumoniae) |
Humans |
Militärangehörige, Beschäftigte im Gesundheitswesen, institutionelle Beschäftigte |
|
Pilze/Mykobakterien |
||
|
Histoplasmose (Histoplasma capsulatum) |
Boden; Vogel- oder Fledermauskot (endemisch im östlichen Nordamerika) |
Landarbeiter, Laboranten, Arbeiter |
|
Kokzidioidomykose (Coccidioides immitis) |
Boden (endemisch im westlichen Nordamerika) |
Militärangehörige, Landarbeiter, Arbeiter, Textilarbeiter, Laboranten |
|
Blastomykose (Blastomyces dermatitidis) |
Boden (endemisch im östlichen Nordamerika) |
Laboranten, Landarbeiter, Arbeiter, Forstarbeiter |
|
Parakokzidioidomykose (Paracoccidioides brasiliensis) |
Boden (endemisch in Venezuela, Kolumbien, Brasilien) |
Landarbeiter |
|
Sporotrichose (Sporothrix schenkii) |
Pflanzenreste, Baum- und Gartenpflanzenrinde |
Gärtner, Floristen, Bergleute |
|
Tuberkulose (Mycobacterium tuberculosis, M. bovis, M. africanum) |
Menschliche und nichtmenschliche Primaten, Rinder |
Hartgesteinsbergleute, Gießereiarbeiter, Gesundheits- und Laborarbeiter, Schlachthofarbeiter, tierärztliche Pflegekräfte, Militärpersonal, Wirtshausarbeiter |
|
Andere Mykobakteriose als Tuberkulose (Mycobacterium spp..) |
Boden |
Silica-exponierte Arbeiter, einschließlich Sandstrahler |
|
Viren |
||
|
Hantavirus |
Nagetiere |
Landarbeiter, Hirten, Nagetierbekämpfungsarbeiter |
|
Masern |
Humans |
Mitarbeiter im Gesundheitswesen und im Labor |
|
Röteln |
Humans |
Mitarbeiter im Gesundheitswesen und im Labor |
|
Grippe |
Humans |
Mitarbeiter im Gesundheitswesen und im Labor |
|
Varicella zoster |
Humans |
Mitarbeiter des Gesundheitswesens und Labors, Militärpersonal |
|
Respiratorisches Synzytial-Virus |
Humans |
Mitarbeiter im Gesundheitswesen und im Labor |
|
Adenovirus |
Humans |
Mitarbeiter des Gesundheitswesens und Labors, Militärpersonal |
|
Parainfluenza-Virus |
Humans |
Mitarbeiter im Gesundheitswesen und im Labor |
|
Virus der lymphozytären Choriomeningitis (Arenavirus) |
Nagetiere |
Labormitarbeiter, Tierpfleger |
|
Lassafieber (Arenavirus) |
Nagetiere |
Mitarbeiter des Gesundheitswesens |
|
Marburg- und Ebola-Viren (Filovirus) |
Menschliche und nichtmenschliche Primaten, möglicherweise Fledermäuse |
Labormitarbeiter, Tierpfleger, Mitarbeiter des Gesundheitswesens, Arbeiter in Baumwollfabriken |
Berufsbedingt erworbene Infektionen bei Landarbeitern
Zusätzlich zu Gasen und organischen Stäuben, die die Atemwege beeinträchtigen und Infektionskrankheiten imitieren, betreffen mehrere zoonotische (bei Tieren und Menschen verbreitete Krankheitserreger) und andere Infektionskrankheiten, die mit dem Leben auf dem Land verbunden sind, ausschließlich Landarbeiter. Diese Krankheiten werden durch Einatmen infektiöser Aerosole erworben und selten von einer Person auf eine andere übertragen. Solche Krankheiten, die bei Landarbeitern auftreten, sind Anthrax, Brucellose, Q-Fieber, Ornithose, Tuberkulose und Pest (Tabelle 1). Pilzpathogene umfassen Histoplasmose, Blastomykose, Kokzidioidomykose, Parakokzidioidomykose und Kryptokokkose (Tabelle 1). Abgesehen von den hantaviralen Erkrankungen sind Viruserkrankungen keine wichtige Ursache für berufsbedingte Lungenerkrankungen bei Landarbeitern.
Es wird angenommen, dass einige dieser Infektionen häufiger auftreten, aber ihre Inzidenz ist schwierig zu bestimmen, weil: (1) die meisten Infektionen subklinisch sind, (2) die klinische Erkrankung mild oder wegen unspezifischer Symptome schwer zu diagnostizieren ist, (3) medizinisch und diagnostische Dienste sind für die meisten Landarbeiter kaum verfügbar, (4) es gibt kein organisiertes Meldesystem für viele dieser Krankheiten und (5) viele davon sind seltene Krankheiten in der Allgemeinheit und werden vom medizinischen Personal nicht erkannt. Obwohl beispielsweise epidemische Nephritis aufgrund des Puumala-Virus, eines Hantavirus, in Westeuropa selten gemeldet wird, haben Serountersuchungen bei Landarbeitern eine Prävalenz von 2 bis 7 % von Antikörpern gegen Hantaviren gezeigt.
Zoonotische Infektionen in Industrienationen nehmen aufgrund aktiver Krankheitsbekämpfungsprogramme ab, die sich an die Tierpopulationen richten. Trotz dieser Kontrollen bleiben Landarbeiter und Personen, die in landwirtschaftlich verwandten Bereichen arbeiten (wie Tierärzte, Fleischverpacker, Geflügelverarbeiter und Haar-/Hautarbeiter) einem Risiko für viele Krankheiten ausgesetzt.
Hantavirus-Infektion
Hantavirus-Infektion die zu hämorrhagischem Fieber mit renalem Syndrom (HFRS) oder epidemischer Nephritis (EN) führt, wird seit mehr als 50 Jahren bei Landarbeitern, Militärangehörigen und Labormitarbeitern in Endemiegebieten Asiens und Europas klinisch beschrieben. Die Infektion erfolgt durch Einatmen von Aerosolen aus Urin, Speichel und Fäkalien von infizierten Nagetieren. Hämorrhagische Erkrankungen und verminderte Nierenfunktion entwickeln sich während der meisten Hantavirus-Erkrankungen eher als bei einer Lungenentzündung, aber Lungenödeme aufgrund erhöhter Gefäßpermeabilität wurden in HFRS und EN berichtet. Die tiefgreifenden pulmonalen Folgen von Hantavirus-Infektionen wurden bis zu einem kürzlichen Ausbruch des Hantavirus-Lungensyndroms (HPS) im Zusammenhang mit einer Infektion mit einem kürzlich isolierten Hantavirus im Westen der Vereinigten Staaten (Muerto-Canyon-Virus, Four-Corners-Virus oder Sin-Nombre-Virus) nicht vollständig erkannt.
Hantaviren sind Mitglieder der Bunyaviridae, eine Familie von RNA-Viren. Fünf Hantaviren wurden mit Erkrankungen des Menschen in Verbindung gebracht. HFRS wurde mit dem Hantaan-Virus in Ostasien, dem Dobrava-Virus auf dem Balkan und dem weltweit verbreiteten Seoul-Virus in Verbindung gebracht. EN wurde in Westeuropa mit dem Puumala-Virus in Verbindung gebracht. HPS wurde mit einem neu isolierten Hantavirus im Westen der Vereinigten Staaten in Verbindung gebracht. Von 1951 bis 1983 wurden 12,000 Fälle von HFRS aus der Republik Korea gemeldet. Es wird berichtet, dass die Krankheitsinzidenz in China mit Epidemien in ländlichen und städtischen Zentren zunimmt, und 1980 wurden 30,500 Fälle mit 2,000 Todesfällen auf HFRS zurückgeführt.
Klinische Präsentation
Bei den Viren, die HFRS oder EN verursachen, führt die Infektion normalerweise zu einer asymptomatischen Entwicklung von Anti-Hantavirus-Antikörpern. Bei erkrankten Menschen sind die Anzeichen und Symptome der frühen Phase unspezifisch, und eine Hantavirus-Infektion kann nur durch serologische Tests diagnostiziert werden. Eine langsame Genesung ist üblich, aber einige Personen entwickeln sich zu HFRS oder EN und entwickeln Proteinurie, mikroskopische Hämaturie, Azotämie und Oligurie. Personen mit HFRS entwickeln auch starke Blutungen aufgrund von disseminierter intravasaler Gerinnung, erhöhter Gefäßpermeabilität und Schock. Die Sterblichkeit bei Personen mit dem vollständigen HFRS-Syndrom variiert zwischen 5 und 20 %.
HPS ist gekennzeichnet durch diffuse interstitielle Lungeninfiltrate und das plötzliche Einsetzen von akuter Atemnot und Schock. Eine ausgeprägte Leukozytose kann als Folge erhöhter Zytokine auftreten, die Hantavirus-Erkrankungen charakterisieren. Bei HPS kann die Sterblichkeit mehr als 50 % betragen. Die Inzidenz asymptomatischer Infektionen oder unerkannter HPS ist unvollständig untersucht.
Diagnosetest
Die Diagnose erfolgt durch den Nachweis des Vorhandenseins von Immunglobulin M oder eines steigenden Titers von Immunglobulin G unter Verwendung hochspezifischer und sensitiver indirekter Immunfluoreszenz und neutralisierender Antikörper-Assays. Andere diagnostische Verfahren umfassen Polymerase-Kettenreaktion für virale Ribonukleinsäure und Immunhistochemie für virales Antigen.
Epidemiologie
Die Infektion erfolgt durch Einatmen von Aerosolen aus Urin, Speichel und Fäkalien infizierter Nagetiere. Infizierte Nagetiere haben keine offensichtliche Krankheit. Die Übertragung kann durch perkutane Inokulation von Urin, Speichel oder Fäkalien infizierter Nagetiere erfolgen, es gibt jedoch keine Hinweise auf eine Übertragung von Mensch zu Mensch.
Seroepidemiologische Untersuchungen an Menschen und Nagetieren haben gezeigt, dass Hantaviren endemisch mit einer weltweiten Verbreitung in ländlichen und städtischen Umgebungen sind. In endemischen ländlichen Gebieten nehmen Nagetier-Mensch-Interaktionen zu, wenn Nagetiere saisonal in Häuser eindringen oder die menschliche Aktivität in Gebieten mit hoher Nagetierdichte zunimmt. Personen in ländlichen Berufen sind am stärksten von einer Ansteckung bedroht. In Umfragen unter asymptomatischer Landbevölkerung in Italien hatten 4 bis 7 % der Forstarbeiter, Ranger, Landwirte und Jäger Anti-Hantavirus-Antikörper, verglichen mit 0.7 % der Soldaten. Bei asymptomatischen Landarbeitern in Irland und der Tschechoslowakei betrug die Prävalenz von Anti-Hantavirus-Antikörpern 1 bis 2 % bzw. 20 bis 30 %. Pflanzen, Ernten, Dreschen, Hüten und Forstwirtschaft sind Risikofaktoren für eine Virusinfektion. Serostudien im Westen der Vereinigten Staaten zur Bestimmung des beruflichen Risikos einer Hantavirus-Infektion sind im Gange, aber in einer Studie mit Mitarbeitern des Gesundheitswesens (HCWs), die sich um HPS-Patienten kümmern, wurden keine Infektionen festgestellt. Bei den ersten 68 Personen mit HPS scheint es, dass landwirtschaftliche Aktivitäten in Lebensräumen infizierter Nagetiere Risikofaktoren für eine Infektion sind. Die Patienten pflügten eher von Hand, säuberten Lebensmittellager, pflanzten, säuberten Tierställe und waren Viehhirten. Das Hauptreservoir für HPS ist die Hirschmaus, Peromyscus maniculatus.
Andere betroffene Berufe
In städtischen Umgebungen ist das Nagetierreservoir für das Seoul-Virus die Hausratte. Städtische Arbeiter, wie Hafenarbeiter, Arbeiter in Getreidelagern, Zooarbeiter und Arbeiter zur Nagetierbekämpfung, können einem Hantavirus-Infektionsrisiko ausgesetzt sein. Forschungslabore, die Nagetiere für andere Forschungszwecke als die Hantavirus-Forschung einsetzen, waren gelegentlich unerwartete Quellen für Hantavirus-Infektionen von Labormitarbeitern. Andere Berufe, wie Militärpersonal und Feldbiologen, sind einem Hantavirus-Infektionsrisiko ausgesetzt.
Behandlung
Ribavirin hat gezeigt in vitro Aktivität gegen mehrere Hantaviren und klinische Wirksamkeit gegen Hantaan-Virusinfektionen und wurde zur Behandlung von Personen mit HPS verwendet.
Kontrollen der öffentlichen Gesundheit
Es steht kein Impfstoff zur Verfügung, obwohl laufende Bemühungen zur Entwicklung von Lebendimpfstoffen und Totvakzinen unternommen werden. Die Minimierung des menschlichen Kontakts mit Nagetieren und die Verringerung der Nagetierpopulationen in der menschlichen Umgebung verringern das Krankheitsrisiko. In Hantavirus-Forschungslabors begrenzen hochrangige Biosicherheitseinrichtungen das Risiko einer Virusvermehrung in Zellkulturen oder beim Umgang mit Materialien mit hohen Viruskonzentrationen. In anderen Forschungslabors, in denen Nagetiere verwendet werden, kann eine regelmäßige serologische Überwachung der Nagetierkolonien auf eine Hantavirus-Infektion in Betracht gezogen werden.
Lymphozytäre Choriomeningitis (LCM)
LCM ist wie die hantaviralen Infektionen natürlicherweise eine Infektion wilder Nagetiere, die sich gelegentlich auf den Menschen ausbreitet. Das LCM-Virus ist ein Arenavirus, die Übertragung erfolgt jedoch normalerweise durch Aerosolisierung. Zu den natürlichen Wirten gehören Wildmäuse, aber eine anhaltende Infektion von Haushamstern ist gut dokumentiert. Eine Infektion ist daher bei den meisten Berufen möglich, die mit der Aerosolisierung von Nagetierurin verbunden sind. Der jüngste dokumentierte arbeitsbedingte Ausbruch dieser Krankheit ereignete sich bei Laborpersonal, das T-Zell-defizienten Nacktmäusen ausgesetzt war, die als Ergebnis der Inokulation kontaminierter Tumorzelllinien persistent infiziert waren.
Klinische Präsentation
Die meisten Fälle von LCM sind asymptomatisch oder mit einer unspezifischen grippeähnlichen Erkrankung verbunden und werden daher nicht erkannt. Obwohl der Respirationstrakt die Eintrittsstelle ist, sind respiratorische Symptome eher unspezifisch und selbstlimitierend. Meningitis oder Meningoenzephalitis entwickelt sich bei einem kleinen Prozentsatz der Patienten und kann zu einer spezifischen Diagnose führen.
Diagnosetest
Die Diagnose erfolgt in der Regel durch den serologischen Nachweis eines steigenden Virustiters bei entsprechenden klinischen Anzeichen. Gelegentlich werden auch Virusisolierung und Gewebeimmunfluoreszenz verwendet.
Epidemiologie
Etwa 20 % der Wildmäuse sind mit diesem Virus infiziert. Die transplazentare Übertragung des Virus bei anfälligen Nagetieren führt zu T-Zell-Toleranz und angeboren infizierten Mäusen (oder Hamstern), die ihr ganzes Leben lang persistierend infiziert bleiben. In ähnlicher Weise können T-Zell-defiziente Mäuse, wie Nacktmäuse, dauerhaft mit dem Virus infiziert werden. Menschen werden durch Aerosolübertragung infiziert. Darüber hinaus können Nagetierzelllinien mit dem Virus kontaminiert sein und dieses vermehren. Menschen infizieren sich normalerweise durch Aerosole, obwohl die Übertragung direkt oder über Insektenvektoren erfolgen kann.
Andere betroffene Berufe
Jeder Beruf, der mit Stäuben verbunden ist, die mit den Exkrementen wildlebender Nagetiere kontaminiert sind, birgt das Risiko einer LCM-Infektion. Tierpfleger in Labortiereinrichtungen, Arbeiter in der Tierhandlung und Labormitarbeiter, die mit Nagetierzelllinien arbeiten, können sich infizieren.
Behandlung
Eine LCM-Infektion ist in der Regel selbstlimitierend. In schweren Fällen kann eine unterstützende Behandlung erforderlich sein.
Kontrollen der öffentlichen Gesundheit
Es ist kein Impfstoff verfügbar. Das Screening von Forschungsmäusen, Hamstern und Zelllinien hat die meisten im Labor erworbenen Infektionen begrenzt. Für T-Zell-defiziente Mäuse erfordern serologische Tests die Verwendung von immunkompetenten Sentinel-Mäusen. Die Verwendung routinemäßiger Laborsicherheitsvorkehrungen wie Handschuhe, Augenschutz und Laborkittel ist angemessen. Die Reduzierung der Anzahl wilder Nagetiere in der menschlichen Umwelt ist wichtig für die Bekämpfung von LCM, Hantavirus und Pest.
Respiratorische Chlamydiose
Respiratorische Chlamydiose aufgrund von Chlamydia psittaci ist die am häufigsten gemeldete Ursache für OAP im Zusammenhang mit der Schlachtung von Tieren (Geflügel) und der Fleischverarbeitung. Chlamydiose und andere Krankheiten werden oft mit dem Kontakt mit kranken Tieren in Verbindung gebracht, was der einzige Hinweis auf die Quelle und Art der Infektion sein kann. Bei der Verarbeitung infizierter Tiere entstehen Aerosole, die Personen infizieren, die von der Fleischverarbeitung entfernt sind, und die Arbeit in der Nähe von Fleischverarbeitungsbetrieben kann ein Hinweis auf die Art der Infektion sein. Respiratorische Chlamydiose kann mit der Exposition gegenüber Papageien (Psittakose) oder Nicht-Papageienvögeln (Ornithose) verbunden sein. Nicht-Vogel-Quellen von Chlamydia psittaci werden in der Regel nicht als potenzielle Zoonosen angesehen, obwohl bei Menschen, die Schaf- und Ziegenstämmen ausgesetzt waren, über Spontanaborte und Konjunktivitis berichtet wurde. Lungenentzündung durch C. pneumoniae ist eine kürzlich beschriebene häufige Ursache für ambulant erworbene Pneumonie C. psittaci Infektionen. Aufgrund seiner jüngsten Entdeckung, die Rolle von C. pneumoniae bei OAPs ist unvollständig untersucht und wird in diesem Review nicht weiter diskutiert.
Klinische Präsentation
Die Ornithose reicht von einer leichten grippeähnlichen Erkrankung bis zu einer schweren Lungenentzündung mit Enzephalitis, die in der Präantibiotika-Ära eine Todesfallrate (CFR) von mehr als 20 % aufwies. Prodromalfieber, Schüttelfrost, Myalgie, Kopfschmerzen und unproduktiver Husten können bis zu drei Wochen vor der Diagnose einer Lungenentzündung anhalten. Neurologische, hepatische und renale Veränderungen sind häufig. Röntgenologische Befunde umfassen eine Konsolidierung des unteren Lappens mit Hilus-Lymphadenopathie. Der klinische Verdacht nach Feststellung arbeitsbedingter oder sonstiger Expositionen gegenüber Vögeln ist diagnostisch entscheidend, da keine pathognomonischen Befunde vorliegen.
Diagnosetest
Ornithose führt in der Regel zu einem hohen Titer von Komplementbindungs(CF)-Antikörpern, obwohl eine frühzeitige Behandlung mit Tetracyclinen die Antikörperbildung unterdrücken kann. Ein einzelner akuter Serumtiter ³1:16 Verdünnung von CF-Antikörpern mit einem kompatiblen klinischen Erscheinungsbild oder einer vierfachen Änderung des CF-Antikörpertiters kann zur Diagnosestellung verwendet werden. Unsachgemäß gepaarte Serumproben und der hohe Hintergrund von Chlamydien-Antikörpern in Risikogruppen unterminieren den Nutzen von Antikörper-Assays zur Diagnose der meisten Chlamydien-Erkrankungen.
Epidemiologie
C. psittaci kommt in praktisch allen Vogelarten vor und ist bei Säugetieren weit verbreitet. Die Infektion resultiert normalerweise aus einer zoonotischen Übertragung, es wurde jedoch auch von einer Übertragung von Mensch zu Mensch berichtet. Eine asymptomatische Infektion ist weit verbreitet und bis zu 11 % der Landarbeiter ohne Krankheitsgeschichte haben Antikörper dagegen C. psittaci. Begrenzte Ausbrüche bleiben sporadisch, aber Pandemien im Zusammenhang mit dem Handel mit exotischen Vögeln traten zuletzt 1930 auf. In den Vereinigten Staaten werden jährlich 70 bis 100 Fälle von Ornithose gemeldet, und fast ein Drittel dieser Krankheiten wird beruflich erworben. Die meisten beruflich erworbenen Infektionen treten bei Arbeitern in der Heimtier- oder Geflügel verarbeitenden Industrie auf und stehen im Zusammenhang mit der Aerosolisierung von Gewebe oder Fäkalien von Vögeln. In Ländern, in denen Vögel häufig als Haustiere gehalten werden und Einfuhrquarantänen schlecht durchgesetzt werden, sind Ausbrüche häufiger, aber die Beschäftigung ist ein geringerer Risikofaktor.
Andere betroffene Berufe
Die Krankheit tritt am häufigsten bei Arbeitern in der Geflügelverarbeitung auf, aber Arbeiter in Verteilungs- und Vogelquarantäneeinrichtungen für exotische Vögel, Zuchtvolieren und Tierkliniken sind gefährdet.
Behandlung
Tetracyclin oder Erythromycin für 10 bis 14 Tage sollten eine angemessene Behandlung sein, aber ein klinischer Rückfall ist häufig, wenn die Behandlung für eine unzureichende Dauer gegeben wird.
Kontrollen der öffentlichen Gesundheit
In den Vereinigten Staaten werden exotische Vögel zur Chemoprophylaxe mit Tetracyclinen unter Quarantäne gestellt. Ähnliche Methoden werden in anderen Ländern angewandt, in denen ein Handel mit exotischen Vögeln besteht. Für Ornithose wurde kein Impfstoff entwickelt. Programme zur Erhöhung der Belüftung, um die Aerosolkonzentration zu verdünnen, die Aerosolbildung oder das Einatmen infektiöser Partikel zu reduzieren oder kranke Vögel in kommerziellen Verarbeitungsanlagen zu behandeln, wurden eingeführt, aber ihre Wirksamkeit wurde nicht nachgewiesen.
Brucellose
Jährlich treten weltweit etwa 500,000 Fälle von Brucellose auf, die durch mehrere Brucella-Arten verursacht werden. Die Pathogenität von Brucella Infektionen hängt von der infizierenden Spezies ab, die dazu neigt, unterschiedliche Reservoirwirte zu haben. Die Stauseen für Brucella abortus, B. suis, B. melitensis, B. ovis, B. canis, und B. neotomae sind in der Regel Rinder, Schweine, Ziegen, Schafe, Hunde bzw. Ratten.
Brucellose kann aus einer Infektion auf verschiedenen Wegen, einschließlich Aerosolisierung, resultieren. Die meisten Krankheiten resultieren jedoch aus der Einnahme von nicht pasteurisierten Milchprodukten von Ziegen. Die daraus resultierende systemische Erkrankung wird verursacht durch B. Melitensis aber nicht mit bestimmten Berufen verbunden. Eine Lungenentzündung tritt in 1 % der Fälle auf, obwohl Husten häufig vorkommt.
In entwickelten Ländern wird die berufsbedingte Brucellose normalerweise verursacht durch brucella abortus und resultiert aus der Einnahme oder Inhalation von infektiösen Aerosolen, die mit der Plazenta von Schweinen und Rindern in Verbindung stehen. Eine subklinische Infektion ist häufig; Bis zu 1 % der Landarbeiter haben Antikörper dagegen B. Abortus. Bei etwa 10 % der Infizierten entwickelt sich eine Krankheit. Im Gegensatz zu Krankheit durch B. Melitensis, Krankheit verbunden mit B. Abortus ist in der Regel beruflich erworben und weniger schwer. Personen mit akuter Brucellose entwickeln hohes tägliches Fieber, Arthralgie und Hepatosplenomegalie. Bei der primären Brucella-Pneumonie ist eine pneumonische Konsolidierung tatsächlich selten, und Lungenbefunde können Heiserkeit oder Keuchen, Hilusadenopathie, peribronchiale Infiltrate, Parenchymknoten oder ein miliäres Muster umfassen. Die Isolierung kann in 90 % der akuten Fälle aus Knochenmark und in 50 bis 80 % der Fälle aus Blut erfolgen. Die Diagnose kann serologisch mit einer Vielzahl von Antikörpertests gestellt werden. Tetracycline sollten für vier bis sechs Wochen verwendet werden, und Rifampin kann zur Synergie hinzugefügt werden. Rinder-, Ziegen-, Schaf- und Schweinezüchter, Milcharbeiter, Schlachthausarbeiter, Tierärzte und Metzger sind die primär gefährdeten Bevölkerungsgruppen. Brucella-Test- und Ausrottungsprogramme haben die Zahl der infizierten Tiere stark reduziert und die Herden identifiziert, die das größte Risiko für die Übertragung von Krankheiten darstellen. Bei der Arbeit mit Brucella-infizierten Tieren sind Vermeidung oder persönlicher Schutz, insbesondere nach Abort oder Geburt, die einzigen wirksamen Methoden zur Krankheitsbekämpfung.
Milzbrand beim Einatmen
Lungenmilzbrand tritt weltweit auf, ist aber weniger verbreitet als Hautmilzbrand. Anthrax ist eine systemische Erkrankung bei vielen Tieren und wird normalerweise durch perkutane Infektion bei der Verarbeitung oder durch den Verzehr von kontaminiertem Fleisch auf den Menschen übertragen. Lungenmilzbrand wird durch das Einatmen von Sporen verursacht Bacillus Anthracis aus Knochen, Haaren oder Fell von Schafen, Ziegen oder Rindern („Wollsortiererkrankheit“) oder selten bei der Verarbeitung von infiziertem Fleisch. Sporen werden von Alveolarmakrophagen phagozytiert und zu mediastinalen Lymphknoten transportiert, wo sie keimen. Dies führt zu einer hämorrhagischen Mediastinitis, die sich jedoch selten als primäre Pneumonie manifestiert. Die Krankheit ist gekennzeichnet durch ein erweitertes Mediastinum, Lungenödem, Pleuraergüsse, Splenomegalie und ein schnelles Fortschreiten zu Atemversagen. Die Sterblichkeitsrate beträgt trotz Antibiotika und Beatmungsunterstützung 50 % oder mehr. Positive Blutkulturen sind häufig, aber serologische Tests mit einem Blotting-Immunoassay können verwendet werden. Erkrankte werden mit hochdosiertem Penicillin oder bei Penicillinallergie alternativ mit intravenösem Ciprofloxacin behandelt. Tierzüchter, Tierärzte, Tierpfleger, Haar- und Fellverarbeiter und Schlachthofarbeiter sind einem erhöhten Risiko ausgesetzt. Für Tiere in Endemiegebieten und Menschen mit hohem Krankheitsrisiko ist eine jährliche Impfung verfügbar. Spezifische Kontrollmaßnahmen gegen Inhalations-Milzbrand umfassen Formaldehyd-Dekontamination, Dampfsterilisation oder Bestrahlung von Haaren und Häuten; Verbot der Einfuhr von Häuten aus endemischen Gebieten; und persönlicher Atemschutz für Arbeiter.
Lungenpest
Pest, verursacht durch Yersinia pestis, ist überwiegend eine flohübertragene Krankheit, die bei wilden Nagetieren enzootisch ist. Menschen infizieren sich normalerweise, wenn sie von einem infizierten Floh gebissen werden, und entwickeln häufig eine Blutvergiftung. In den Vereinigten Staaten entwickelte sich von 1970 bis 1988 bei etwa 10 % der Personen mit Septikämie eine sekundäre Pneumonie durch hämatogene Ausbreitung. Tiere und Menschen mit Lungenpest produzieren infektiöse Aerosole. Primäre Lungenentzündung beim Menschen kann durch Einatmen eines infektiösen Aerosols entstehen, das um sterbende Tiere mit sekundärer Lungenentzündung entsteht. Trotz des Potenzials einer pneumonischen Ausbreitung ist eine Übertragung von Mensch zu Mensch selten und hat in den Vereinigten Staaten seit fast 50 Jahren nicht mehr stattgefunden. Seuchenkontrollen umfassen die Isolierung von Personen mit Lungenpest und die Verwendung von persönlichem Atemschutz durch medizinisches Personal. Eine Aerosolübertragung auf Krankenhausmitarbeiter ist möglich, und eine Tetracyclin-Prophylaxe sollte für jeden in Betracht gezogen werden, der mit Menschen oder Tieren mit Lungenpest in Kontakt kommt. Eine Reihe von Berufen sind durch Aerosolübertragung gefährdet, darunter biomedizinische und Krankenhauslabormitarbeiter und in endemischen Gebieten eine Reihe ländlicher Berufe, darunter Tierärzte, Nagetierbekämpfungskräfte, Jäger/Fallensteller, Mammologen, Wildtierbiologen und Landarbeiter. Für Personen in Risikoberufen wird ein Totimpfstoff empfohlen.
Fieber
Verursacht durch Einatmen von Coxiella burnetii, Q-Fieber ist eine systemische Erkrankung, die sich bei 10 bis 60 % der infizierten Personen als atypische Lungenentzündung äußert. Viele verschiedene Isolate von C. burnetii Krankheiten hervorrufen, und Theorien über Plasmid-abhängige Virulenz sind umstritten. C. burnetii infiziert viele Haustiere (z. B. Schafe, Rinder, Ziegen, Katzen) weltweit; aus Urin, Fäkalien, Milch, Plazenta oder Uterusgewebe vernebelt wird; bildet eine hochresistente Endospore, die jahrelang infektiös bleibt; und ist extrem ansteckend.
Klinische Präsentation
Nach einer 4- bis 40-tägigen Inkubationszeit stellt sich das akute Q-Fieber als eine grippeähnliche Erkrankung dar, die sich zu einer atypischen Lungenentzündung entwickelt, ähnlich der Mycoplasma. Die akute Erkrankung dauert etwa zwei Wochen, kann aber bis zu neun Wochen andauern. Chronische Erkrankungen, überwiegend eine Endokarditis und Hepatitis, können sich bis zu 20 Jahre nach einer akuten Erkrankung entwickeln.
Diagnosetest
Primärisolierung von C. burnetii wird selten durchgeführt, da ein hohes Maß an biologischer Sicherheit erforderlich ist. Die Diagnose wird serologisch durch den Nachweis eines CF-Antikörpertiters von 1:8 oder höher in einem geeigneten klinischen Umfeld oder einer vierfachen Veränderung des CF-Titers gestellt.
Andere betroffene Berufe
Mitarbeiter in der Landwirtschaft (insbesondere bei Milchprodukten und Wolle), in Krankenhauslabors und in der biomedizinischen Forschung sind einem Infektionsrisiko ausgesetzt.
Behandlung
Es gibt keinen wirksamen Impfstoff für C. burnetii. Eine zweiwöchige Behandlung mit Tetracyclinen oder Ciprofloxacin wird zur Behandlung akuter Erkrankungen eingesetzt.
Kontrollen der öffentlichen Gesundheit
Aufgrund der weit verbreiteten geografischen Verbreitung, zahlreichen Tierreservoirs und der Resistenz gegen Inaktivierung sind persönlicher Atemschutz und technische Kontrollen zur Eindämmung infektiöser Aerosole die einzigen wirksamen vorbeugenden Maßnahmen. Diese Kontrollverfahren sind jedoch in vielen landwirtschaftlichen Umgebungen (z. B. Schaf- und Rinderhaltung) schwierig umzusetzen. Die frühzeitige Diagnose von Q-Fieber durch medizinisches Personal kann durch Aufklärung von Arbeitnehmern mit hohem Risiko, an dieser seltenen Krankheit zu erkranken, erleichtert werden. Eine Übertragung auf das Krankenhauspersonal ist möglich, und die Isolierung kann die Ausbreitung der Q-Fieber-Pneumonie in Krankenhäusern begrenzen.
Verschiedenes Bakterielle OAPS von Landarbeitern
Pseudomonas pseudomallei ist ein boden- und nagetierassoziierter Organismus, der hauptsächlich in Südostasien vorkommt und Melioidose verursacht. Die Krankheit ist mit Bodenexposition und einer potenziell langen Latenzzeit verbunden. Militärangehörige waren während und nach dem Vietnamkrieg die Hauptopfer von Melioidose in den Vereinigten Staaten. Multifokale, noduläre, eitrige oder granulomatöse Pneumonie charakterisieren die pulmonale Form der Melioidose.
Francisella tularensis, der Erreger der Tularämie, ist eine Zoonose, die mit wilden Nagetieren und Hasenartigen in Verbindung gebracht wird. Dies ist eine potenzielle Berufskrankheit von Wildbiologen, Mammologen, Arbeitern in der Nagetierbekämpfung, Jägern, Fallenstellern und Tierärzten. Tularämie kann durch Einatmen, direkte Inokulation, Hautkontakt oder Verschlucken entstehen oder durch Vektoren übertragen werden. Lungenerkrankungen resultieren entweder aus direkter Inhalationsexposition oder aus hämatogener Ausbreitung einer septischen Erkrankung. Die pulmonalen Läsionen der Tularämie sind akut, multifokal, eitrig und nekrotisierend.
Histoplasmose
Histoplasmose wurde ausgelöst durch Histoplasma capsulatum, ein frei lebender Schimmelpilz im Boden, der mit dem Kot von Vögeln oder Fledermäusen in Verbindung gebracht wird. Histoplasmose ist die wichtigste Ursache für Pilz-OAP bei Landarbeitern. Die verschiedenen Pilzpneumonien von Landarbeitern werden im nächsten Abschnitt beschrieben.
Klinische Präsentation
Nach der Exposition variieren die Angriffsraten und der Schweregrad der Histoplasmose als Ergebnis des infizierenden Inokulums und der Antikörperspiegel des Wirts, die durch eine vorherige Infektion übertragen wurden. Nach starker Exposition entwickeln bis zu 50 % der Personen eine selbstlimitierende Atemwegserkrankung, während andere asymptomatisch bleiben. Zu den am wenigsten schweren symptomatischen Syndromen gehören „grippeähnliche“ Symptome, unproduktiver Husten und Brustschmerzen. Die körperliche Untersuchung kann für Erythema nodosum oder Erythema multiforme auffällig sein. Röntgenaufnahmen des Brustkorbs zeigen fleckige, segmentale Infiltrate, aber keine Röntgenbefunde können die Histoplasmose spezifisch von anderen Lungeninfektionen unterscheiden. Hiläre oder mediastinale Lymphadenopathie ist in allen Stadien der primären Histoplasmose üblich.
Progressive primäre pneumonische Histoplasmose ist gekennzeichnet durch schwere systemische Beschwerden, Husten mit eitrigem Auswurf und Hämoptyse. Zu den fortschreitenden Röntgenveränderungen gehören multiple Knötchen, Lappenkonsolidierung und dichte, multilobäre interstitielle Infiltrate. Größere Expositionen verstärken die Schwere der Erkrankung und führen zu schweren Atemwegserkrankungen, dem akuten Atemnotsyndrom (ARDS) oder Atelektase aufgrund einer Obstruktion durch mediastinale Lymphadenopathie.
Etwa 20 % der Kranken entwickeln andere Histoplasmose-Syndrome, die idiosynkratisch sind und nicht das Ergebnis einer größeren Exposition oder eines Fortschreitens der Primärerkrankung sind. Zu den Syndromen gehören Arthritis-Erythema nodosum, Perikarditis und chronische pulmonale Histoplasmose (fibrotische apikale Lungeninfiltrate mit Kavitation). Eine disseminierte Histoplasmose entwickelt sich bei einem kleinen Prozentsatz der Patienten, insbesondere bei Immunsupprimierten.
Diagnosetest
Die definitive Diagnose erfolgt durch Isolierung oder histopathologischen Nachweis des Organismus in einem geeigneten klinischen Präparat. Leider ist der Organismus in geringen Konzentrationen vorhanden und die Empfindlichkeit dieser Methoden ist gering. Verdachtsdiagnosen werden oft auf der Grundlage der geografischen Lage, der Expositionsgeschichte und der Röntgenbefunde der Lunge oder Verkalkungen in der Milz gestellt.
Epidemiologie
H. capsulatum wird weltweit in Verbindung mit bestimmten Bodenbedingungen gefunden, aber Krankheiten werden hauptsächlich aus den Tälern des Ohio und des Mississippi in den Vereinigten Staaten gemeldet. Hohe Sporenkonzentrationen findet man in Vogelquartieren, Altbauten, Geflügelställen, Höhlen oder Schulhöfen; Sie werden durch die Arbeitstätigkeit gestört. Die Konzentration von Mikrokonidien ist in gestörten, geschlossenen Bereichen (z. B. beim Abriss von Gebäuden) höher und führt dort zu einem höheren Inokulum für die Arbeiter als an den meisten Standorten im Freien. In Endemiegebieten sind Personen, die Vogelquartiere säubern, ältere kontaminierte Gebäude abreißen oder Ausgrabungen für den Straßen- oder Hochbau durchführen, stärker gefährdet als die allgemeine Bevölkerung. In den Vereinigten Staaten werden jedes Jahr 15,000 bis 20,000 Personen mit Histoplasmose ins Krankenhaus eingeliefert, und ungefähr 3 % von ihnen sterben.
Andere betroffene Berufe
Berufsrisiko zuordnen für Histoplasma Eine Infektion ist schwierig, da der Organismus frei im Boden lebt und die Konzentration aerosolisierter Sporen durch Wind und Staub erhöht wird. Die Infektion ist hauptsächlich auf die geografische Lage zurückzuführen. In endemischen Gebieten haben Menschen auf dem Land, unabhängig von ihrem Beruf, eine Prävalenz von 60 bis 80 % positiver Hauttests H. capsulatum Antigene. Eine tatsächliche Krankheit resultiert aus einem großen Infektionsinokulum und ist normalerweise auf Arbeiter beschränkt, die an der Störung des Bodens oder der Zerstörung kontaminierter Gebäude beteiligt sind.
Behandlung
Eine antimykotische Behandlung der Histoplasmose und anderer beruflich erworbener Pilzinfektionen ist bei einer akuten selbstlimitierenden Lungenerkrankung nicht indiziert. Eine Therapie mit Amphotericin B (30 bis 35 mg/kg Gesamtdosis) oder Ketoconazol (400 mg/Tag für sechs Monate) oder Behandlungsschemata mit beiden Wirkstoffen ist indiziert bei disseminierter Histoplasmose, chronischer pulmonaler Histoplasmose, akuter pulmonaler Histoplasmose mit ARDS oder mediastinalem Granulom mit symptomatischer Obstruktion und kann bei anhaltender, mittelschwerer Primärerkrankung nützlich sein. Die Behandlung führt zu einer Ansprechrate von 80 bis 100 %, aber Rückfälle sind häufig und können bis zu 20 % bei Amphotericin B und 50 % bei Ketoconazol betragen. Die Wirksamkeit neuerer Azol-Medikamente (dh Itraconazol und Fluconazol) bei berufsbedingten Pilzinfektionen wurde nicht definiert.
Kontrollen der öffentlichen Gesundheit
Es wurde kein wirksamer Impfstoff entwickelt. Chemische Dekontamination mit 3 % Formaldehyd, Vornässen des Bodens oder kontaminierter Oberflächen zur Reduzierung der Aerosolisierung und persönlicher Atemschutz zur Reduzierung des Einatmens aerosolisierter Sporen können Infektionen reduzieren, aber die Wirksamkeit dieser Methoden wurde nicht bestimmt.
Verschiedene Pilzpneumonien
Zu den verschiedenen Pilzpneumonien von Landarbeitern gehören Aspergillose, Blastomykose, Kryptokokkose, Kokzidioidomykose und Parakokzidioidomykose (Tabelle 1). Diese Krankheiten werden verursacht durch Aspergillus spp., Blastomyces dermatitidis, Cryptococcus neoformans, Coccidioides immitis und Paracoccidioides brasiliensis, beziehungsweise. Obwohl diese Pilze geografisch weit verbreitet sind, wird die Krankheit normalerweise aus endemischen Gebieten gemeldet. Im Vergleich zu viralen und bakteriellen Ursachen einer Lungenentzündung sind diese Erkrankungen selten und werden oft zunächst nicht vermutet. T-Zell-Erkrankungen erhöhen die Anfälligkeit für Histoplasmose, Blastomykose, Kryptokokkose, Kokzidioidomykose und Parakokzidioidomykose. Eine große anfängliche Exposition kann jedoch bei immunkompetenten Arbeitern zu einer Erkrankung führen. Infektionen mit Aspergillus und verwandte Pilze neigen dazu, bei neutropenischen Patienten aufzutreten. Aspergillose ist am häufigsten eine OAP der Immunsupprimierten und wird im Abschnitt über Infektionen bei Immunsupprimierten diskutiert.
Kr. Neoformer, mögen H. capsulatum, ist ein häufiger Bewohner von Böden, die durch Vogelkot kontaminiert sind, und berufliche Exposition gegenüber solchen Stäuben oder anderen Stäuben, die mit kontaminiert sind Kr. Neoformer kann zu Krankheiten führen. Berufliche Blastomykose wird mit Nebentätigkeiten in Verbindung gebracht, insbesondere in den östlichen und zentralen Vereinigten Staaten. Kokzidioidomykose entsteht durch Kontakt mit kontaminierten Stäuben in endemischen Gebieten im Südwesten der Vereinigten Staaten (daher das Synonym San-Joaquin-Valley-Fieber). Berufliche Exposition gegenüber kontaminierten Böden Süd- und Mittelamerikas wird häufig mit Parakokzidioidomykose in Verbindung gebracht. Aufgrund der potenziell langen Latenzzeit bei Parakokzidioidomykose kann diese Exposition dem Auftreten von Symptomen lange vorausgehen.
Klinische Präsentation
Das klinische Erscheinungsbild der Kokzidioidomykose, Blastomykose oder Parakokzidioidomykose ähnelt dem der Histoplasmose. Aerosolexpositionen gegenüber diesen Pilzen können OAP erzeugen, wenn das anfängliche Inokulum hoch genug ist. Wirtsfaktoren, wie z. B. eine vorherige Exposition, begrenzen jedoch die Erkrankung bei den meisten Personen. Bei Kokzidioidomykose treten bei einem kleinen Prozentsatz der Infizierten pulmonale und systemische Krankheitszeichen auf; Fortschreitende Erkrankung mit Ausbreitung auf mehrere Organe ist ohne Immunsuppression selten. Obwohl die Infektionsquelle normalerweise die Lunge ist, kann sich die Blastomykose als Lungenerkrankung, Hauterkrankung oder systemische Erkrankung äußern. Das häufigste klinische Erscheinungsbild der Blastomykose ist ein chronischer Husten mit Lungenentzündung, der nicht von Tuberkulose zu unterscheiden ist. Die Mehrheit der Patienten mit klinisch offensichtlicher Blastomykose wird jedoch extrapulmonale Läsionen aufweisen, die die Haut, die Knochen oder das Urogenitalsystem betreffen. Parakokzidioidomykose ist eine Krankheit aus Mexiko, Mittel- und Südamerika, die sich am häufigsten als Reaktivierung einer früheren Infektion nach einer langen, aber variablen Latenzzeit zeigt. Die Krankheit kann mit dem Altern von infizierten Individuen assoziiert sein, und eine Reaktivierung kann durch Immunsuppression induziert werden. Das pulmonale Erscheinungsbild ähnelt anderen Pilzpneumonien, aber extrapulmonale Erkrankungen, insbesondere der Schleimhäute, sind bei Parakokzidioidomykose häufig.
Die Lunge ist der übliche Ort für die Primärinfektion mit Cryptococcus neoformans. Wie bei den zuvor diskutierten Pilzen können Lungeninfektionen asymptomatisch, selbstlimitierend oder fortschreitend sein. Eine Ausbreitung des Organismus, insbesondere auf die Hirnhäute und das Gehirn, kann jedoch auch ohne symptomatische Atemwegserkrankung erfolgen. Kryptokokken-Meningoenzephalitis ohne Nachweis einer pulmonalen Kryptokokkose ist zwar selten, aber die häufigste klinische Manifestation Kr. Neoformer Infektion.
Diagnosetest
Der direkte Nachweis der Gewebeform des Organismus erlaubt eine definitive Diagnose in Biopsien und zytologischen Präparaten. Immunfluoreszenz kann ein nützliches Bestätigungsverfahren sein, wenn morphologische Details nicht ausreichen, um den Erreger festzustellen. Diese Organismen können auch aus verdächtigen Läsionen kultiviert werden. Ein positiver Latex-Kryptokokken-Agglutinintest im Liquor cerebrospinalis weist auf eine Kryptokokken-Meningoenzephalitis hin. Der Nachweis von Organismen reicht jedoch für die Diagnose einer Krankheit möglicherweise nicht aus. Beispielsweise saprophytisches Wachstum von Cr. Neoformer ist in den Atemwegen möglich.
Andere betroffene Berufe
Labormitarbeiter, die diese Pilze isolieren, sind einem Infektionsrisiko ausgesetzt.
Behandlung
Die antimykotische Therapie ist ähnlich wie bei der Histoplasmose.
Kontrollen der öffentlichen Gesundheit
Technische Kontrollen sind angezeigt, um das Risiko für Labormitarbeiter zu verringern. Atemschutz beim Arbeiten mit Böden, die stark mit Vogelkot kontaminiert sind, reduziert die Exposition gegenüber Kr. Neoformer.
Beruflich erworbene Infektionen bei Beschäftigten im Gesundheitswesen und im Labor
Das Einatmen infektiöser Aerosole ist die häufigste Infektionsquelle bei Krankenhausmitarbeitern, und viele Arten viraler und bakterieller Pneumonien wurden einer arbeitsbedingten Übertragung zugeschrieben (Tabelle 26). Die meisten Infektionen sind viral und selbstlimitierend. Bei Krankenhausmitarbeitern wurde jedoch über potenziell schwerwiegende Ausbrüche von Tuberkulose, Masern, Keuchhusten und Pneumokokken-Pneumonie berichtet. Infektionen bei immungeschwächten Arbeitern werden am Ende dieses Abschnitts diskutiert.
Beschäftigte in diagnostischen Labors sind einem Risiko für beruflich erworbene Infektionen infolge einer Übertragung über die Luft ausgesetzt. Die Übertragung erfolgt, wenn Krankheitserreger während der anfänglichen Verarbeitung klinischer Proben von Patienten mit unsicheren Infektionskrankheiten aerosolisiert werden, und wird selten erkannt. Beispielsweise erkrankte bei einem kürzlichen Brucellose-Ausbruch in der Gemeinde ein Drittel der Laboranten an Brucellose. Die Beschäftigung im Labor war der einzige identifizierte Risikofaktor. Die Übertragung von Mensch zu Mensch zwischen Labormitarbeitern, die Übertragung durch Lebensmittel oder Wasser oder der Kontakt mit einer bestimmten klinischen Probe konnten nicht als Risikofaktoren nachgewiesen werden. Röteln, Tuberkulose, Varicella-Zoster und Respiratory-Syncytial-Virus sind Berufskrankheiten, die ebenfalls im Labor von Technikern erworben werden.
Trotz rigoroser tierärztlicher Versorgung, biologischer Sicherheitsmaßnahmen und der Verwendung kommerziell gezüchteter, pathogenfreier Labortiere bleibt die Inhalation die Hauptübertragungsart von Infektionskrankheiten im Zusammenhang mit biomedizinischen Forschern. Darüber hinaus können neu entdeckte Mikroorganismen oder bisher unerkannte zoonotische Reservoirs angetroffen werden und diese Strategien zur Krankheitsbekämpfung untergraben.
Masern
Masern, als berufsbedingte Krankheit, ist zu einem zunehmenden Problem unter Krankenhausmitarbeitern in Industrienationen geworden. Seit 1989 gibt es in den Vereinigten Staaten aufgrund der schlechten Einhaltung der Impfempfehlungen und des Versagens der Grundimmunisierung bei geimpften Empfängern ein Wiederaufleben der Masern. Aufgrund der hohen Morbidität und potenziellen Mortalität im Zusammenhang mit Masern bei anfälligen Arbeitnehmern sollte Masern in jedem Arbeitsschutzprogramm besondere Beachtung geschenkt werden. Von 1985 bis 1989 wurden in den Vereinigten Staaten mehr als 350 Fälle von beruflich erworbenen Masern gemeldet, was 1 % aller gemeldeten Fälle entspricht. Fast 30 % der Krankenhausmitarbeiter mit beruflich erworbenen Masern wurden ins Krankenhaus eingeliefert. Die größten Gruppen von Krankenhausmitarbeitern mit Masern waren Krankenschwestern und Ärzte, und 90 % von ihnen erkrankten an Masern von Patienten. Obwohl 50 % dieser Kranken für eine Impfung infrage kamen, war keiner geimpft worden. Die erhöhte Masernmorbidität und -sterblichkeit bei Erwachsenen hat die Besorgnis verstärkt, dass infizierte Arbeitnehmer Patienten und Mitarbeiter anstecken könnten.
Im Jahr 1989 empfahl der Beratungsausschuss für Immunisierungspraktiken zwei Impfdosen gegen Masern oder den Nachweis einer Masernimmunität zum Zeitpunkt der Anstellung in einer Gesundheitseinrichtung. Serologischer und Impfstatus der Arbeiter sollten dokumentiert werden. Darüber hinaus ist bei Patienten mit Masern eine Neubewertung des Immunstatus von HCWs angebracht. Die Umsetzung dieser Empfehlungen und die angemessene Isolierung von Patienten mit bekannten und vermuteten Masern schränkt die Übertragung von Masern in medizinischen Einrichtungen ein.
Klinische Präsentation
Zusätzlich zu der häufigen Maserndarstellung bei nicht immunisierten Erwachsenen müssen atypische und modifizierte Maserndarstellungen in Betracht gezogen werden, da viele Krankenhausmitarbeiter zuvor Totimpfstoffe erhalten hatten oder teilweise immun sind. Bei klassischen Masern folgt auf die Infektion eine zweiwöchige Inkubationszeit mit leichten Symptomen der oberen Atemwege. Während dieser Zeit ist der Arbeiter virämisch und ansteckend. Es folgen ein sieben- bis zehntägiger Verlauf mit Husten, Schnupfen und Konjunktivitis sowie die Entwicklung eines morbilliformen Ausschlags und Koplik-Flecken (erhabene weiße Läsionen auf der Wangenschleimhaut), die für Masern pathognomonisch sind. Im Röntgenbild sind diffuse retikulonoduläre Infiltrate mit bilateraler hilärer Lymphadenopathie, oft mit überlagerter bakterieller Bronchopneumonie, zu erkennen. Diese Anzeichen treten lange nachdem die Person Gelegenheit hatte, andere anfällige Personen zu infizieren, auf. Lungenkomplikationen machen 90 % der Masern-Todesfälle bei Erwachsenen aus. Keine spezifische antivirale Behandlung ist bei irgendeiner Form von Masern wirksam, obwohl hochtitriges Anti-Masern-Immunglobulin einige Symptome bei Erwachsenen lindern kann.
Bei atypischen Masern, die bei Personen auftreten, die mit einem in den 1960er Jahren entwickelten Totimpfstoff geimpft wurden, ist eine schwere Lungenbeteiligung häufig. Der Ausschlag ist atypisch und Koplik-Flecken sind selten. Bei modifizierten Masern, die bei Personen auftreten, die zuvor einen Lebendimpfstoff erhalten haben, aber eine partielle Immunität entwickeln, sind die Anzeichen und Symptome denen der klassischen Masern ähnlich, aber milder und bleiben oft unbemerkt. Personen mit atypischen und modifizierten Masern sind virämisch und können das Masernvirus verbreiten.
Diagnose
Masern bei Krankenhausangestellten sind oft modifiziert oder atypisch und werden selten vermutet. Masern sollten bei einer Person mit einem erythematösen makulopapulösen Ausschlag in Betracht gezogen werden, dem ein drei- bis viertägiges fieberhaftes Prodromal vorausgeht. Bei Personen mit einer Erstinfektion und ohne vorherige Immunisierung ist die Virusisolierung oder der Antigennachweis schwierig, aber enzymgebundene Immunadsorptions- oder fluoreszierende Antikörper-Assays können für eine schnelle Diagnose verwendet werden. Bei Personen mit früheren Immunisierungen ist die Interpretation dieser Assays schwierig, aber immunfluoreszierende Antikörperfärbungen exfolierter Zellen können hilfreich sein.
Epidemiologie
Anfällige Krankenschwestern und Ärzte erkranken fast neunmal häufiger an Masern als Personen im gleichen Alter, die keine HCWs sind. Wie bei allen Maserninfektionen erfolgt die Übertragung von Mensch zu Mensch durch Inhalation eines infektiösen Aerosols. Krankenhausangestellte übertragen Masern von Patienten und Mitarbeitern und übertragen Masern wiederum auf anfällige Patienten, Mitarbeiter und Familienmitglieder.
Andere betroffene Berufe
Epidemische Masern sind in akademischen Einrichtungen in Industrienationen und unter Landarbeitern aufgetreten, die auf Sammelunterkünfte auf Plantagen beschränkt sind.
Kontrollen der öffentlichen Gesundheit
Interventionsstrategien im Bereich der öffentlichen Gesundheit umfassen Impfprogramme sowie Infektionskontrollprogramme zur Überwachung der Masernerkrankung und des Antikörperstatus der Arbeitnehmer. Wenn eine natürliche Infektion oder eine geeignete Zwei-Dosen-Impfung nicht dokumentiert werden kann, sollten Antikörpertests durchgeführt werden. Die Impfung schwangerer Arbeiterinnen ist kontraindiziert. Die Impfung anderer gefährdeter Arbeitnehmer ist ein wichtiges Hilfsmittel zur Krankheitsprävention. Nach einer Exposition gegenüber Masern kann die Entfernung von anfälligen Arbeitern aus dem Patientenkontakt für 21 Tage die Ausbreitung der Krankheit verringern. Eine eingeschränkte Tätigkeit von Arbeitnehmern mit Masern für 7 Tage nach dem Auftreten des Hautausschlags kann die Übertragung der Krankheit ebenfalls einschränken. Leider haben entsprechend geimpfte Arbeiter Masern entwickelt, trotz schützender Antikörperspiegel, die vor der Krankheit dokumentiert wurden. Aus diesem Grund empfehlen viele einen persönlichen Atemschutz bei der Betreuung von Patienten mit Masern.
Verschiedene virale Atemwegsinfektionen
Eine Vielzahl von Viren, die nicht nur im Gesundheitswesen vorkommen, sind die häufigste Ursache für OAPs bei Mitarbeitern des Gesundheitswesens. Die ätiologischen Agenzien sind diejenigen, die ambulant erworbene OAPs verursachen, einschließlich Adenovirus, Cytomegalovirus, Influenzavirus, Parainfluenzavirus und Respiratory-Syncytial-Virus. Da diese Organismen auch in der Gemeinschaft vorkommen, ist es schwierig, sie als Ursache einer individuellen OAP zu bestimmen. Serologische Studien deuten jedoch darauf hin, dass Beschäftigte im Gesundheitswesen und Tagespflege einem erhöhten Risiko ausgesetzt sind, diesen Atemwegserregern ausgesetzt zu sein. Diese Viren sind auch für Krankheitsausbrüche in vielen Situationen verantwortlich, in denen Arbeiter auf engstem Raum zusammengebracht werden. Beispielsweise kommt es bei Militärrekruten häufig zu Ausbrüchen einer adenoviralen Infektion.
Pertussis
Keuchhusten, wie Masern, wurde zunehmend bei Krankenhauspersonal in Industrienationen gemeldet. 1993 wurden in den Vereinigten Staaten fast 6,000 Keuchhustenfälle gemeldet, eine Zunahme von 80 % gegenüber 1992. Anders als in den Vorjahren traten 25 % der gemeldeten Fälle bei Personen über zehn Jahren auf. Die Zahl der berufsbedingten Erkrankungen bei Krankenhausmitarbeitern ist unbekannt, wird aber in den Industrienationen als unzureichend gemeldet. Aufgrund der schwindenden Immunität bei Erwachsenen und der Möglichkeit, dass Krankenhausmitarbeiter anfällige Säuglinge infizieren, wird der Diagnose und Überwachung von Keuchhusten größere Bedeutung beigemessen.
Klinische Präsentation
Keuchhusten kann sechs bis zehn Wochen ohne Intervention bestehen bleiben. In der ersten Woche, wenn der Erkrankte am ansteckendsten ist, entwickeln sich trockener Husten, Schnupfen, Bindehautentzündung und Fieber. Bei zuvor geimpften Erwachsenen kann der anhaltende, produktive Husten mehrere Wochen andauern und Keuchhusten wird selten in Betracht gezogen. Die klinische Diagnose ist schwierig, und klinischer Verdacht sollte geweckt werden, wenn ein Arbeiter mit einem Husten konfrontiert wird, der länger als sieben Tage anhält. Ein weißer Blutkörperchen von mehr als 20,000 mit einem Überwiegen von Lymphozyten kann die einzige Laboranomalie sein, dies wird jedoch selten bei Erwachsenen festgestellt. Röntgenaufnahmen des Brustkorbs zeigen eine konfluierende Bronchopneumonie in den unteren Lappen, die vom Herzen ausstrahlen, um das charakteristische Zeichen eines „struppigen Herzens“ zu geben, und Atelektase ist in 50 % der Fälle vorhanden. Aufgrund der extremen Infektiosität dieses Mittels ist eine strenge Atemisolierung erforderlich, bis die Behandlung mit Erythromycin oder Trimethoprim/Sulfamethoxazol fünf Tage fortgesetzt wurde. Enge Kontakte von infizierten Personen und Krankenhausmitarbeitern, die keine Atemschutzmaßnahmen angewendet haben, sollten unabhängig vom Impfstatus eine 14-tägige Antibiotikaprophylaxe erhalten.
Diagnose
Isolierung von Bordetella pertussis, direkte Immunfluoreszenzfärbung von Nasensekreten oder Entwicklung von a B. Keuchhusten Antikörperantwort wird verwendet, um eine endgültige Diagnose zu stellen.
Epidemiologie
B. Keuchhusten ist hoch ansteckend, wird von Mensch zu Mensch durch Inhalation infektiöser Aerosole übertragen und hat eine Befallsrate von 70 bis 100 %. In der Vergangenheit war es keine Krankheit von Erwachsenen und wurde nicht als OAP geschätzt. Während eines Keuchhustenausbruchs im Westen der Vereinigten Staaten waren viele Krankenhausangestellte bei der Arbeit exponiert und entwickelten trotz Antibiotikaprophylaxe Keuchhusten. Aufgrund abnehmender schützender Antikörperspiegel bei Erwachsenen, die nie eine klinische Erkrankung hatten, aber nach 1940 einen zellulären Impfstoff erhalten haben, gibt es in Industrieländern eine wachsende Bevölkerung von Pertussis-anfälligen Krankenhausangestellten.
Kontrollen der öffentlichen Gesundheit
Identifizierung, Isolierung und Behandlung sind die wichtigsten Strategien zur Krankheitskontrolle in Krankenhäusern. Die Rolle des azellulären Pertussis-Impfstoffs für Krankenhausangestellte ohne ausreichende Konzentrationen an schützenden Antikörpern ist unklar. Während des jüngsten Ausbruchs im Westen der Vereinigten Staaten berichtete ein Drittel der geimpften Krankenhausangestellten von leichten bis mäßigen Nebenwirkungen des Impfstoffs, aber 1 % hatte „schwere“ systemische Symptome. Obwohl diese stärker betroffenen Arbeiter Arbeitstage verpassten, wurden keine neurologischen Symptome gemeldet.
Tuberkulose
In den 1950er Jahren wurde allgemein anerkannt, dass Beschäftigte im Gesundheitswesen in Industrienationen einem höheren Risiko für Tuberkulose (TB – granulomatöse Krankheit aufgrund von Tuberkulose) ausgesetzt waren Mycobacterium tuberculosis oder nahe verwandte Organismen M. bovis) als die allgemeine Bevölkerung. Von den 1970er bis Anfang der 1980er Jahre deuteten Umfragen darauf hin, dass dies nur zu einem leicht erhöhten Risiko geworden war. In den späten 1980er Jahren führte ein deutlicher Anstieg der Zahl der in US-Krankenhäuser eingelieferten TB-Fälle zu einer unerwarteten Übertragung von TB M. tuberculosis an Krankenhausmitarbeiter. Die hohe Hintergrundprävalenz positiver Tuberkulin-Hauttests (TST) in bestimmten sozioökonomischen Gruppen oder Einwanderergruppen, aus denen viele Krankenhausangestellte stammten, und die geringe Assoziation der TST-Konversion mit arbeitsbedingter TB-Exposition machten es schwierig, das Risiko zu quantifizieren Berufsbedingte Übertragung von Tuberkulose auf Arbeitnehmer. 1993 waren in den Vereinigten Staaten schätzungsweise 3.2 % der gemeldeten Personen mit TB im Gesundheitswesen tätig. Trotz Problemen bei der Definition des Risikos sollte eine arbeitsbedingte Infektion in Betracht gezogen werden, wenn Krankenhausmitarbeiter an TB erkranken oder ihren TST umwandeln.
M. tuberculosis wird fast ausschließlich von Mensch zu Mensch über infektiöse Partikel mit einem Durchmesser von 1 bis 5 mm übertragen, die beim Husten, Sprechen oder Niesen entstehen. Das Infektionsrisiko steht in direktem Zusammenhang mit der Intensität der Exposition gegenüber infektiösen Aerosolen – kleine gemeinsame Räume, erhöhte Dichte infektiöser Partikel, schlechte Entfernung infektiöser Partikel, Rückführung von Luft, die infektiöse Partikel enthält, und verlängerte Kontaktzeit. Im Gesundheitswesen erhöhen Verfahren wie Bronchoskopie, endotracheale Intubation und Behandlung mit vernebelten Aerosolen die Dichte infektiöser Aerosole. Ungefähr 30 % der engen Kontakte – Personen, die einen gemeinsamen Raum mit einer infektiösen Person teilen – infizieren sich und unterziehen sich einer Hauttest-Konvertierung. Nach der Infektion entwickeln 3 bis 10 % der Personen innerhalb von 12 Monaten TB (dh Primärerkrankung) und weitere 5 bis 10 % entwickeln TB im Laufe ihres Lebens (dh Reaktivierungserkrankung). Diese höheren Raten treten in Entwicklungsländern und in Situationen auf, in denen Unterernährung häufiger vorkommt. HIV-infizierte Personen reaktivieren TB häufiger, etwa 3 bis 8 % pro Jahr. CFR variiert; in Industrienationen liegt sie zwischen 5 und 10 %, in Entwicklungsländern jedoch zwischen 15 und 40 %.
Klinische Präsentation
Vor der HIV-Epidemie hatten 85 bis 90 % der Personen mit Tuberkulose eine Lungenbeteiligung. Chronischer Husten, Auswurf, Fieber und Gewichtsverlust bleiben die am häufigsten berichteten Symptome der Lungentuberkulose. Abgesehen von seltener amphorischer Atmung oder posttussivem Knistern über den Oberlappen ist eine körperliche Untersuchung nicht hilfreich. Eine auffällige Röntgenaufnahme des Brustkorbs wird in fast allen Fällen gefunden und ist normalerweise der erste Befund, der auf TB hindeutet. Bei primärer TB ist ein Infiltrat des unteren oder mittleren Lappens mit ipsilateraler hilärer Lymphadenopathie mit Atelektase üblich. Reaktivierung TB führt normalerweise zu einem Infiltrat und Kavitation in den oberen Lungenlappen. Röntgenaufnahmen des Brustkorbs sind zwar empfindlich, aber nicht spezifisch und geben keine endgültige Diagnose von TB.
Diagnose
Die definitive Diagnose einer Lungentuberkulose kann nur durch Isolierung gestellt werden M. tuberculosis aus Sputum oder Lungengewebe, obwohl eine Verdachtsdiagnose möglich ist, wenn säurefeste Bazillen (AFB) im Sputum von Personen mit kompatiblen klinischen Präsentationen gefunden werden. Die Diagnose einer TB sollte auf der Grundlage klinischer Anzeichen und Symptome erwogen werden; die Isolierung und Behandlung von Personen mit kompatiblen Krankheiten sollte nicht wegen des Ergebnisses eines TST hinausgezögert werden. In Entwicklungsländern, in denen TST-Reagenzien und Röntgenaufnahmen des Brustkorbs nicht verfügbar sind, schlägt die WHO vor, Personen mit Atemwegssymptomen von drei Wochen Dauer, Hämoptysen jeglicher Dauer oder signifikantem Gewichtsverlust auf TB zu untersuchen. Diese Personen sollten eine mikroskopische Untersuchung ihres Sputums auf AFB haben.
Andere betroffene Berufe
Arbeitnehmer-zu-Arbeiter- und Klient-zu-Arbeiter-Luftübertragung von M. tuberculosis wurde unter Krankenhausangestellten, Flugzeugbesatzungen, Bergleuten, Arbeitern in Justizvollzugsanstalten, Tierpflegern, Werftarbeitern, Schulangestellten und Arbeitern in Sperrholzfabriken dokumentiert. Bestimmte Berufe wie Landarbeiter, Tierpfleger, Arbeiter, Haushälter, Hausmeister und Arbeiter in der Lebensmittelzubereitung müssen besonders berücksichtigt werden, obwohl die meisten Risiken auf den sozioökonomischen Status oder den Einwanderungsstatus der Arbeiter zurückzuführen sind.
Besondere Aufmerksamkeit sollte der Lungentuberkulose bei Bergarbeitern und anderen Gruppen mit Kieselsäureexposition geschenkt werden. Zusätzlich zu einem erhöhten Risiko einer Primärinfektion durch andere Bergleute entwickeln Personen mit Silikose häufiger TB und haben eine höhere TB-spezifische Mortalität im Vergleich zu nicht silikotischen Arbeitern. Wie bei den meisten Personen reaktiviert sich TB bei langjährig silikotischen Personen M. tuberculosis Infektionen, die vor der Silica-Exposition entstanden sind. In experimentellen Systemen hat sich gezeigt, dass die Kieselsäureexposition den Infektionsverlauf dosisabhängig verschlechtert, aber es ist unklar, ob Kieselerde ausgesetzte, nicht silikotische Arbeiter einem größeren Risiko ausgesetzt sind, TB zu entwickeln. Silica-exponierte Gießereiarbeiter ohne radiologische Silikose haben ein dreimal höheres Risiko für TB-spezifische Mortalität im Vergleich zu ähnlichen Arbeitern ohne Silica-Exposition. Keine andere berufliche Staubexposition wurde mit einem verstärkten Fortschreiten von TB in Verbindung gebracht.
Landarbeiter mit Migrationshintergrund erkranken mit größerer Wahrscheinlichkeit an Reaktivierungstuberkulose als die allgemeine Bevölkerung. Schätzungen zu positiven TSTs bei landwirtschaftlichen Wanderarbeitern reichen von etwa 45 % bei 15- bis 34-jährigen Personen bis zu fast 70 % bei Arbeitern über 34 Jahren.
Klinische Labormitarbeiter sind einem erhöhten Risiko für beruflich erworbene TB durch Übertragung über die Luft ausgesetzt. In einer kürzlich durchgeführten zehnjährigen Umfrage in ausgewählten Krankenhäusern in Japan erkrankten 0.8 % der Labormitarbeiter an TB. Es wurden keine Quellen aus der Gemeinschaft identifiziert und arbeitsbedingte Expositionen wurden nur in 20 % der Fälle identifiziert. Die meisten Fälle traten bei den Arbeitern in den Labors für Pathologie und Bakteriologie und in den Autopsieräumen auf.
Behandlung
Mehrere Behandlungsschemata haben sich in verschiedenen ambulanten Einrichtungen als wirksam erwiesen. Unter den konformen Patienten in Industrienationen ist die tägliche Dosis von vier Medikamenten (einschließlich Isoniazid und Rifampin) für zwei Monate, gefolgt von täglichen Dosen von Isoniazid und Rifampin für die nächsten vier Monate, zu einem Standardbehandlungsschema geworden. Die direkt beobachtete, zweimal wöchentliche Verabreichung der gleichen Medikamente ist eine wirksame Alternative bei Patienten mit geringerer Compliance. In Entwicklungsländern und in Situationen, in denen Anti-Tuberkulose-Medikamente nicht ohne Weiteres verfügbar sind, wurde eine 9- bis 12-monatige tägliche Dosierung mit Isoniazid und Rifampin verwendet. Ein Behandlungsschema sollte mit der nationalen Politik übereinstimmen und die Anfälligkeit des Organismus für verfügbare Standardmedikamente gegen Tuberkulose und die Dauer der Therapie berücksichtigen. Aufgrund begrenzter Ressourcen zur Bekämpfung von TB in Entwicklungsländern können sich die Bemühungen auf die primären Infektionsquellen konzentrieren – Patienten mit Sputumabstrichen, die AFB zeigen.
Im Gesundheitswesen sind Arbeitsbeschränkungen für infektiöse Arbeiter mit Lungentuberkulose angezeigt. In anderen Umgebungen können infektiöse Arbeiter einfach von anderen Arbeitern isoliert werden. Im Allgemeinen gelten Personen nach zweiwöchiger Einnahme geeigneter Antituberkulose-Medikamente als nicht infektiös, wenn eine symptomatische Verbesserung und eine Abnahme der AFB-Dichte im Sputumabstrich eintritt.
Kontrollen der öffentlichen Gesundheit
Die wichtigste öffentliche Gesundheitskontrolle der beruflich oder ambulant erworbenen TB-Übertragung bleibt die Identifizierung, Isolierung und Behandlung von Personen mit Lungentuberkulose. Belüftung zur Verdünnung infektiöser Aerosole; Filterung und UV-Licht zur Dekontaminierung der das Aerosol enthaltenden Luft; oder persönlicher Atemschutz kann verwendet werden, wenn das Übertragungsrisiko bekanntermaßen außergewöhnlich hoch ist, die Wirksamkeit dieser Methoden jedoch noch unbekannt ist. Der Nutzen von BCG im Arbeitsschutz bleibt umstritten.
Verschiedene bakterielle Infektionen im Gesundheitswesen
Häufige bakterielle Infektionen der Lunge können von Patienten oder in der Gemeinschaft erworben werden. Arbeitsbedingte aerogene Übertragung von bakteriellen Krankheitserregern wie z Streptococcus pneumoniae, Haemophilus influenza, Neisseria meningitidis, Mycoplasma pneumoniae und Legionella spp (Tabelle 26) auftritt und die daraus resultierenden Erkrankungen in vielen Krankenhausüberwachungsprogrammen enthalten sind. Berufliche bakterielle Atemwegsinfektionen sind ebenfalls nicht auf medizinisches Personal beschränkt. Infektionen mit Streptococcus spp sind beispielsweise eine bekannte Ursache für Krankheitsausbrüche bei Militärrekruten. Für einen bestimmten Arbeitnehmer erschwert jedoch die Prävalenz dieser Erkrankungen außerhalb des Arbeitsplatzes die Unterscheidung zwischen berufsbedingten und ambulant erworbenen Infektionen. Das klinische Erscheinungsbild, die diagnostischen Tests, die Epidemiologie und die Behandlung dieser Erkrankungen sind in medizinischen Standardlehrbüchern beschrieben.
Infektionen beim immunsupprimierten Arbeiter
Immunsupprimierte Arbeitnehmer sind durch viele OAPs einem erhöhten Risiko ausgesetzt. Außerdem wird eine Reihe von Organismen, die bei normalen Personen keine Krankheit verursachen, bei Immunsupprimierten eine Krankheit hervorrufen. Auch die Art der Immunsuppression beeinflusst die Krankheitsanfälligkeit. Beispielsweise ist die invasive pulmonale Aspergillose eine häufigere Komplikation der Chemotherapie als die des erworbenen Immunschwächesyndroms (AIDS).
Eine invasive pulmonale Aspergillose wird normalerweise bei Immunsupprimierten beobachtet, insbesondere bei Personen mit Neutropenie. Allerdings wird gelegentlich von invasiver pulmonaler Aspergillose bei Personen ohne offensichtliche Prädisposition für die Erkrankung berichtet. Die invasive pulmonale Aspergillose zeigt sich normalerweise als schwere, nekrotisierende Pneumonie mit oder ohne systemische Beteiligung bei einem neutropenischen Patienten. Während invasive Aspergillose am häufigsten als nosokomiale Infektion bei Chemotherapiepatienten beobachtet wird, ist dies eine hochgradig tödliche Krankheit bei jedem neutropenischen Arbeiter. Techniken, die die nosokomiale Aspergillose reduzieren – beispielsweise die Kontrolle von Stäuben bei Bauprojekten – können ebenfalls anfällige Arbeitnehmer schützen.
Eine Vielzahl tierischer Krankheitserreger werden nur bei immunsupprimierten Patienten zu potenziellen Zoonosen. Zu den durch Aerosole übertragenen Zoonosen, die nur bei Immunsupprimierten beobachtet werden, gehören Enzephalitozoonose (aufgrund von Encephalitozoon cuniculi), Vogeltuberkulose (aufgrund von Mycobacterium avium) und Rhodococcus equi Infektionen. Solche Krankheiten sind von besonderer Bedeutung in der Landwirtschaft. Methoden zum Schutz von immunsupprimierten Arbeitern sind unvollständig untersucht.
Bei immunsupprimierten Arbeitern verursachen viele potenzielle Krankheitserreger invasive und schwere Erkrankungen, die bei normalen Patienten nicht beobachtet werden. Zum Beispiel schwere Infektionen mit Candida albicans und Pneumocystis carinii sind klassische Manifestationen von AIDS. Das Spektrum berufsbedingter Krankheitserreger bei immunsupprimierten Arbeitnehmern umfasst daher möglicherweise Störungen, die bei immunologisch gesunden Arbeitnehmern nicht vorhanden sind. Die Krankheiten von immunsupprimierten Personen wurden an anderer Stelle gründlich untersucht und werden in dieser Übersicht nicht weiter diskutiert.
Kontrollen der öffentlichen Gesundheit: Überblick
OAPs treten überwiegend bei fünf Gruppen von Arbeitnehmern auf: Krankenhauspersonal, Landarbeiter, Arbeiter in der Fleischproduktion, Militärpersonal und biomedizinisches Laborpersonal (Tabelle 1). Die Vermeidung von infektiösen Aerosolen ist in den meisten Situationen der effektivste Weg, Infektionen zu reduzieren, ist aber oft schwierig. Zum Beispiel, Coxiella burnetii, das ätiologische Agens für Q-Fieber, kann in jeder Umgebung vorhanden sein, die zuvor mit den biologischen Flüssigkeiten infizierter Tiere kontaminiert wurde, aber die Vermeidung aller potenziell infizierten Aerosole wäre in vielen Situationen mit geringem Risiko, wie Schafhaltung oder Rodeos, unpraktisch. Auch die Kontrolle von Begleiterkrankungen kann das OAP-Risiko verringern. Beispielsweise erhöht Silikose das Risiko einer Reaktivierung von TB, und eine Verringerung der Kieselsäurebelastung kann das TB-Risiko bei Bergleuten verringern. Für Rentner mit erheblicher Mortalität und Morbidität in der Allgemeinbevölkerung kann die Impfung die wichtigste Intervention im Bereich der öffentlichen Gesundheit sein. Die Aufklärung der Arbeitnehmer über ihr Risiko für OAPs hilft bei der Einhaltung von Programmen zur Bekämpfung von Berufskrankheiten durch die Arbeitnehmer und hilft auch bei der Früherkennung dieser Erkrankungen.
Unter Krankenhausmitarbeitern und Militärangehörigen ist die Übertragung von Mensch zu Mensch normalerweise der Hauptinfektionsweg. Die Impfung von Arbeitern kann Krankheiten vorbeugen und kann bei der Kontrolle von Krankheitserregern mit hoher Morbidität und/oder Mortalität nützlich sein. Denn es besteht ein Risiko für Personen, die möglicherweise nicht ausreichend immunisiert wurden; Das Erkennen, Isolieren und Behandeln kranker Personen bleibt Teil der Seuchenbekämpfung. Wenn Immunisierung und respiratorische Isolation versagen oder die damit verbundene Morbidität und Mortalität nicht tolerierbar sind, können persönliche Schutzmaßnahmen oder technische Kontrollen zur Verringerung der Dichte oder Infektiosität von Aerosolen in Betracht gezogen werden.
Für Arbeiter in der Landwirtschaft, in der Fleischproduktion und in biomedizinischen Laboren ist die Übertragung von Tier zu Mensch ein häufiges Übertragungsmuster. Neben der Immunisierung empfänglicher Personen, wenn möglich, können andere Seuchenbekämpfungsstrategien die Immunisierung der Tiere, die tierärztlich kontrollierte Antibiotikaprophylaxe bei gut aussehenden Tieren, die Quarantäne neu angekommener Tiere, die Isolierung und Behandlung kranker Tiere und den Kauf von Krankheitserregern umfassen. freie Tiere. Wenn diese Strategien versagt haben oder eine hohe Morbidität und Mortalität vorliegt, können Strategien wie Personenschutz oder technische Kontrollen in Betracht gezogen werden.
Die Übertragung von Infektionserregern von der Umwelt auf den Menschen ist unter Landarbeitern, einschließlich vieler Arbeiter, weit verbreitet. Die Impfung von Arbeitnehmern ist möglich, wenn ein Impfstoff verfügbar ist, aber bei vielen dieser Krankheitserreger ist die Krankheitsinzidenz in der Allgemeinbevölkerung gering und Impfstoffe sind selten durchführbar. In der Landwirtschaft sind die Infektionsquellen weit verbreitet. Infolgedessen sind technische Kontrollen zur Verringerung der Dichte oder Infektiosität von Aerosolen selten durchführbar. In diesen Umgebungen können Netzmittel oder andere Methoden zur Staubreduzierung, Dekontaminationsmittel und persönlicher Atemschutz in Betracht gezogen werden. Da die Kontrolle von OAP bei Landarbeitern oft schwierig ist und diese Krankheiten selten von medizinischem Personal gesehen werden, ist die Schulung der Arbeiter und die Kommunikation zwischen Arbeitern und medizinischem Personal unerlässlich.
Atemwegskrebs
Lungenkrebs
Lungenkrebs ist weltweit die häufigste Krebsart. 1985 traten schätzungsweise weltweit 676,500 Fälle bei Männern und 219,300 Fälle bei Frauen auf, was 11.8 % aller neuen Krebserkrankungen entspricht, und diese Zahl nimmt jährlich um etwa 0.5 % zu (Parkin, Pisani und Ferlay 1993). . Etwa 60 % dieser Fälle treten in Industrieländern auf, in denen Lungenkrebs häufig die häufigste Krebstodesursache bei Männern ist. Sowohl in den Industrie- als auch in den Entwicklungsländern haben Männer eine höhere Inzidenz als Frauen, wobei das Geschlechterverhältnis zwischen dem Zwei- und Zehnfachen liegt. Die internationalen Unterschiede zwischen den Geschlechtern bei der Inzidenz von Lungenkrebs lassen sich weitgehend durch die Unterschiede im aktuellen und früheren Rauchverhalten erklären.
In städtischen Gebieten wurde durchweg ein höheres Lungenkrebsrisiko beobachtet als in ländlichen Gebieten. In den Industrieländern zeigt sich bei Männern eine klare, umgekehrte Beziehung in der Inzidenz und Sterblichkeit von Lungenkrebs nach sozialer Klasse, während Frauen weniger klare und konsistente Muster zeigen. Unterschiede in der sozialen Schicht bei Männern spiegeln hauptsächlich ein unterschiedliches Rauchverhalten wider. In Entwicklungsländern scheint jedoch bei Männern aus der oberen sozialen Schicht ein höheres Risiko zu bestehen als bei anderen Männern: Dieses Muster spiegelt wahrscheinlich die frühere Übernahme westlicher Gewohnheiten durch wohlhabende Bevölkerungsgruppen wider.
Inzidenzdaten des SEER-Programms des United States National Cancer Institute für den Zeitraum 1980-86 zeigen, ähnlich wie in den Vorjahren, dass schwarze Männer eine höhere Inzidenz aufweisen als weiße Männer, während die Inzidenz bei Frauen nicht nach Rasse unterschiedlich ist. Diese Unterschiede zwischen den ethnischen Gruppen in den Vereinigten Staaten können tatsächlich auf sozioökonomische Unterschiede zwischen Schwarzen und Weißen zurückgeführt werden (Baquet et al. 1991).
Die Lungenkrebsinzidenz steigt fast linear mit dem Alter, wenn sie in einer Log-Log-Skala aufgetragen wird; nur in den ältesten Altersgruppen ist eine Abwärtskurve zu beobachten. Lungenkrebsinzidenz und -mortalität haben in diesem Jahrhundert rapide zugenommen und nehmen in den meisten Ländern weiter zu.
Es gibt vier histologische Haupttypen von Lungenkrebs: Plattenepithelkarzinom, Adenokarzinom, großzelliges Karzinom und kleinzelliges Karzinom (SCLC). Die ersten drei werden auch als nicht-kleinzelliger Lungenkrebs (NSCLC) bezeichnet. Die Proportionen jedes histologischen Typs ändern sich je nach Geschlecht und Alter.
Das Plattenepithelkarzinom wird sehr stark mit dem Rauchen in Verbindung gebracht und stellt in vielen Bevölkerungsgruppen die häufigste Form von Lungenkrebs dar. Es entsteht am häufigsten in den proximalen Bronchien.
Das Adenokarzinom ist weniger stark mit dem Rauchen assoziiert. Dieser Tumor ist peripheren Ursprungs und kann als einzelnes peripheres Knötchen, eine multifokale Erkrankung oder eine schnell fortschreitende pneumonische Form auftreten, die sich von Lappen zu Lappen ausbreitet.
Das großzellige Karzinom stellt einen kleineren Anteil aller Lungenkrebsarten dar und hat ein ähnliches Verhalten wie das Adenokarzinom.
SCLC macht einen kleinen Anteil (10 bis 15 %) aller Lungenkrebserkrankungen aus; es entsteht typischerweise in der zentralen endobronchialen Lokalisation und neigt dazu, frühe Metastasen zu entwickeln.
Die Anzeichen und Symptome von Lungenkrebs hängen von der Lage des Tumors, der Ausbreitung und den Auswirkungen des Metastasenwachstums ab. Viele Patienten stellen sich mit einer asymptomatischen Läsion vor, die zufällig beim Röntgen entdeckt wurde. Bei NSCLC-Patienten sind Müdigkeit, verminderte Aktivität, anhaltender Husten, Dyspnoe, verminderter Appetit und Gewichtsverlust häufig. Keuchen oder Stridor können sich auch in fortgeschrittenen Stadien entwickeln. Kontinuierliches Wachstum kann zu Atelektasie, Lungenentzündung und Abszessbildung führen. Klinische Symptome bei SCLC-Patienten sind weniger ausgeprägt als bei Patienten mit NSCLC und hängen normalerweise mit der endobronchialen Lokalisation zusammen.
Lungenkrebs kann in praktisch jedes Organ metastasieren. Die häufigsten Lokalisationen von Metastasen sind Pleura, Lymphknoten, Knochen, Gehirn, Nebennieren, Perikard und Leber. Zum Zeitpunkt der Diagnose hat die Mehrheit der Patienten mit Lungenkrebs Metastasen.
Die Prognose variiert mit dem Stadium der Erkrankung. Die 1983-Jahres-Gesamtüberlebensrate für Lungenkrebspatienten in Europa (85-7) lag zwischen 9 % und 1995 % (Berrino et al. XNUMX).
Für Lungenkrebs ist derzeit kein Populations-Screening-Verfahren verfügbar.
Nasopharynxkrebs
Nasen-Rachen-Krebs ist in den meisten Bevölkerungsgruppen selten, tritt jedoch in Gebieten wie Südostasien, Südchina und Nordafrika bei beiden Geschlechtern häufig auf. Migranten aus Südchina behalten das hohe Risiko weitgehend bei, aber chinesische Migranten der zweiten und dritten Generation in die Vereinigten Staaten haben weniger als die Hälfte des Risikos von Migranten der ersten Generation.
Krebserkrankungen des Nasopharynx sind überwiegend plattenepithelialen Ursprungs. Nach Angaben der WHO werden diese Tumoren wie folgt klassifiziert: Typ 1, verhornendes Plattenepithelkarzinom; Typ 2, nicht verhornendes Karzinom; und Typ 3, undifferenziertes Karzinom, das der häufigste histologische Typ ist. Typ 1 hat ein unkontrolliertes lokales Wachstum und eine Metastasierung wird bei 60 % der Patienten gefunden. Typ 2 und 3 weisen bei 80 bis 90 % der Patienten eine Metastasierung auf.
Bei etwa 90 % der Patienten mit Nasopharynxkarzinom wird eine Raumforderung im Nacken bemerkt. Veränderungen des Gehörs, seröse Mittelohrentzündung, Tinnitus, nasale Obstruktion, Schmerzen und Symptome im Zusammenhang mit dem Wachstum des Tumors in benachbarte anatomische Strukturen können bemerkt werden.
Das 1983-Jahres-Gesamtüberleben von Patienten mit Nasen-Rachen-Krebs in Europa lag zwischen 1985 und 35 bei etwa 1995 % und variierte je nach Tumorstadium und Lokalisation (Berrino et al. XNUMX)..
Der Verzehr von gesalzenem Fisch nach chinesischer Art ist ein Risikofaktor für Nasen-Rachen-Krebs; Die Rolle anderer Ernährungsfaktoren und von Viren, insbesondere des Epstein-Barr-Virus, wurde zwar vermutet, aber nicht bestätigt. Es sind keine beruflichen Faktoren bekannt, die Nasen-Rachen-Krebs verursachen. Gegenwärtig sind keine vorbeugenden Maßnahmen verfügbar (Higginson, Muir und Muñoz 1992).
Sinonasaler Krebs
Neubildungen der Nase und der Nasenhöhlen sind relativ selten. Zusammen machen Krebserkrankungen der Nase und der Nasennebenhöhlen – einschließlich Kiefer-, Siebbein-, Keilbein- und Stirnhöhlen – weniger als 1 % aller Krebserkrankungen aus. In den meisten Fällen werden diese Tumoren als Plattenepithelkarzinome klassifiziert. In westlichen Ländern ist Nasenkrebs häufiger als Nasennebenhöhlenkrebs (Higginson, Muir und Muñoz 1992).
Sie treten häufiger bei Männern und in der schwarzen Bevölkerung auf. Die höchste Inzidenz wird in Kuwait, Martinique und Indien beobachtet. Der Höhepunkt der Krankheitsentwicklung liegt im sechsten Lebensjahrzehnt. Die wichtigste bekannte Ursache von Nasennebenhöhlenkrebs ist die Exposition gegenüber Holzstaub, insbesondere von Hartholzarten. Tabakrauchen scheint nicht mit dieser Krebsart in Verbindung gebracht zu werden.
Die meisten Tumoren der Nasenhöhle und der Nasennebenhöhlen sind gut differenziert und wachsen langsam. Zu den Symptomen können nicht heilende Geschwüre, Blutungen, nasale Obstruktion und Symptome im Zusammenhang mit dem Wachstum in die Mundhöhle, die Orbita und die Fossa pterygoideus gehören. Zum Zeitpunkt der Diagnose ist die Krankheit in der Regel fortgeschritten.
Das 1983-Jahres-Gesamtüberleben von Patienten mit Nasen- und Nasennebenhöhlenkrebs betrug in Europa zwischen 1985 und 35 etwa 1995 %, je nach Größe der Läsion bei der Diagnose (Berrino et al. XNUMX)..
Kehlkopfkrebs
Die höchste Inzidenz von Kehlkopfkrebs wird in Sao Paolo (Brasilien), Navarra (Spanien) und Varese (Italien) gemeldet. Eine hohe Sterblichkeit wurde auch aus Frankreich, Uruguay, Ungarn, Jugoslawien, Kuba, dem Nahen Osten und Nordafrika gemeldet. Kehlkopfkrebs ist überwiegend eine männliche Krebsart: 120,500 traten schätzungsweise 20,700 Fälle bei Männern und 1985 Fälle bei Frauen auf (Parkin, Pisani und Ferlay 1993).. Im Allgemeinen ist die Inzidenz in der schwarzen Bevölkerung höher als in der weißen und in städtischen Gebieten im Vergleich zu ländlichen.
Fast alle Krebsarten des Kehlkopfes sind Plattenepithelkarzinome. Die meisten sind in der Glottis lokalisiert, sie können sich aber auch in der Supraglottis oder selten in der Subglottis entwickeln.
Symptome können nicht auftreten oder sehr subtil sein. Je nach Ort und Stadium der Läsion können Schmerzen, ein kratziges Gefühl, eine Veränderung der Toleranz gegenüber heißen oder kalten Speisen, eine Neigung zum Aspirieren von Flüssigkeiten, eine Veränderung der Atemwege, eine leichte Veränderung der Stimme über mehrere Wochen und eine zervikale Adenopathie vorhanden sein.
Die meisten Kehlkopfkrebsarten sind durch Kehlkopfinspektion oder Endoskopie sichtbar. Präneoplastische Läsionen können im Kehlkopf von Rauchern identifiziert werden (Higginson, Muir und Muñoz 1992).
Das 1983-Jahres-Gesamtüberleben von Kehlkopfkrebspatienten in Europa lag zwischen 1985 und 55 bei etwa 1995 % (Berrino et al. XNUMX).
Pleuramesotheliom
Mesotheliome können aus Pleura, Peritoneum und Perikard entstehen. Das maligne Mesotheliom stellt den wichtigsten Pleuratumor dar; sie tritt hauptsächlich zwischen dem fünften und siebten Lebensjahrzehnt auf.
Das Pleuramesotheliom war einst ein seltener Tumor und bleibt es in den meisten weiblichen Bevölkerungsgruppen, während es bei Männern in den Industrieländern in den letzten Jahrzehnten um 5 bis 10 % pro Jahr zugenommen hat. Im Allgemeinen sind Männer fünfmal so häufig betroffen wie Frauen. Genaue Schätzungen von Inzidenz und Mortalität sind problematisch aufgrund von Schwierigkeiten bei der histologischen Diagnose und Änderungen in der Internationalen Klassifikation der Krankheiten (ICD) (Higginson, Muir und Muñoz 1992). Die Inzidenzraten scheinen jedoch sehr wichtige lokale Schwankungen darzustellen: Sie sind sehr hoch in Gebieten, in denen Asbestabbau stattfindet (z. B. Provinz Nordwestkap in Südafrika), in großen Schiffswerftstädten und in Regionen mit umweltbedingter Faserkontamination, wie z wie bestimmte Gebiete der Zentraltürkei.
Die Patienten können asymptomatisch sein und ihre Krankheit wird zufällig auf Thorax-Röntgenaufnahmen diagnostiziert, oder sie können Dyspnoe und Brustschmerzen haben.
Mesotheliome neigen dazu, invasiv zu sein. Das mediane Überleben beträgt in verschiedenen Serien 4 bis 18 Monate.
Berufliche Risikofaktoren für Atemwegskrebs
Abgesehen vom Tabakrauch wurde laut International Agency for Research on Cancer (IARC) für 13 Wirkstoffe oder Gemische und neun Expositionsumstände ein kausaler Zusammenhang mit Atemwegskrebs nachgewiesen (siehe Tabelle 1).. Darüber hinaus gibt es acht Stoffe, Gemische oder Expositionsumstände, die laut IARC wahrscheinlich krebserzeugend für ein oder mehrere Organe im Respirationstrakt sind (Tabelle 2).. Alle außer Azathioprin, einem immunsuppressiven Medikament, sind hauptsächlich berufliche Expositionen (IARC 1971-94).
Tabelle 1. Etablierte menschliche Atemwegskarzinogene gemäß IARC
| Mitarbeiter Einzelne Agenten | Zielseiten |
| Asbest | Lunge, Kehlkopf, Pleura |
| Arsen und Arsenverbindungen | Lunge |
| Beryllium und Berylliumverbindungen | Lunge |
| Bis (chlormethyl) ether | Lunge |
| Cadmium und Cadmiumverbindungen | Lunge |
| Chlormethylmethylether (technisch) | Lunge |
| Chrom(VI)-Verbindungen | Nase, Lunge |
| Senfgas | Lunge, Kehlkopf |
| Nickelverbindungen | Nase, Lunge |
| Talk, der asbestiforme Fasern enthält | Lunge, Rippenfell |
| Komplexe Mischungen | |
| Kohle-Teere | Lunge |
| Kohle-Teer-Plätze | Lunge |
| Ruß | Lunge |
| Tabakrauch | Nase, Lunge, Kehlkopf |
| Expositionsumstände | |
| Aluminiumproduktion | Lunge |
| Herstellung und Reparatur von Stiefeln und Schuhen | Nase |
| Kohlevergasung | Lunge |
| Cola-Produktion | Lunge |
| Eisen- und Stahlgießen | Lunge |
| Möbel- und Kunsttischlerei | Nase |
| Starke anorganische Säurenebel, die Schwefelsäure enthalten (berufliche Exposition gegenüber) | Larynx |
| Maler (berufliche Exposition als) | Lunge |
| Radon und seine Zerfallsprodukte | Lunge |
| Untertägiger Hämatitabbau (mit Radonexposition) | Lunge |
Quelle: IARC, 1971-1994.
Tabelle 2. Wahrscheinliche Karzinogene der menschlichen Atemwege gemäß IARC
| Mitarbeiter Einzelne Agenten | Verdächtige Zielseiten |
| Acrylnitril | Lunge |
| Azathioprin | Lunge |
| Formaldehyd | Nase, Kehlkopf |
| Kieselsäure (kristallin) | Lunge |
| Komplexe Mischungen | |
| Auspuff des Dieselmotors | Lunge |
| Schweißrauch | Lunge |
| Expositionsumstände | |
| Gummiindustrie | Lunge |
| Versprühen und Ausbringen von Insektiziden (berufliche Expositionen in) | Lunge |
Quelle: IARC, 1971-1994.
Zu den Berufsgruppen, die nach Exposition gegenüber Arsenverbindungen ein erhöhtes Lungenkrebsrisiko aufweisen, gehören Arbeiter in Nichteisenhütten, Pelzverarbeiter, Hersteller von Schaftauchmitteln und Weinbauern (IARC 1987)..
Eine große Anzahl epidemiologischer Studien wurde zum Zusammenhang zwischen Chrom(VI)-Verbindungen und dem Auftreten von Lungen- und Nasenkrebs in der Chromat-, Chromatpigment- und Verchromungsindustrie durchgeführt (IARC 1990a).. Die Übereinstimmung der Befunde und das Ausmaß der Überschreitungen haben das krebserzeugende Potenzial von Chrom(VI)-Verbindungen belegt.
Arbeiter in Nickelraffinerien aus vielen Ländern haben ein erheblich erhöhtes Risiko für Lungen- und Nasenkrebs gezeigt; Andere Nickel-exponierte Berufsgruppen, bei denen ein erhöhtes Lungenkrebsrisiko festgestellt wurde, sind Bergbauarbeiter in Sulfidnickelerzen und Arbeiter in der Herstellung von Nickellegierungen (IARC 1990b)..
Beryllium-exponierte Arbeiter haben ein erhöhtes Lungenkrebsrisiko (IARC 1994a). Die aussagekräftigsten Daten stammen aus dem US Beryllium Case Registry, in dem Fälle von Beryllium-bedingten Lungenerkrankungen aus verschiedenen Branchen gesammelt wurden.
Eine Zunahme des Auftretens von Lungenkrebs wurde in Kohorten von Cadmiumhütten und Nickel-Cadmium-Batteriearbeitern festgestellt (IARC 1994b).. Die gleichzeitige Exposition gegenüber Arsen bei Hüttenwerken und gegenüber Nickel bei Batteriearbeitern kann einen solchen Anstieg nicht erklären.
Asbest ist ein wichtiges berufsbedingtes Karzinogen. Lungenkrebs und Mesotheliom sind die wichtigsten asbestbedingten Neubildungen, aber auch Krebserkrankungen an anderen Stellen, wie dem Magen-Darm-Trakt, Kehlkopf und Niere, wurden bei Asbestarbeitern berichtet. Alle Formen von Asbest stehen in ursächlichem Zusammenhang mit Lungenkrebs und Mesotheliom. Darüber hinaus wurde gezeigt, dass talkhaltige asbestiforme Fasern krebserzeugend für die menschliche Lunge sind (IARC 1987).. Ein charakteristisches Merkmal von Asbest-induziertem Lungenkrebs ist seine synergistische Beziehung zum Zigarettenrauchen.
Eine Reihe von Studien unter Bergleuten, Steinbrucharbeitern, Gießereiarbeitern, Keramikarbeitern, Granitarbeitern und Steinmetzarbeiten haben gezeigt, dass Personen, bei denen Silikose diagnostiziert wurde, nachdem sie Staub mit kristallinem Siliziumdioxid ausgesetzt waren, ein erhöhtes Lungenkrebsrisiko haben (IARC 1987)..
Mehrkernige aromatische Kohlenwasserstoffe (PAK) entstehen hauptsächlich durch pyrolytische Prozesse, insbesondere die unvollständige Verbrennung organischer Materialien. Der Mensch ist jedoch ausschließlich PAK-Mischungen wie Ruß, Steinkohlenteer und Steinkohlenteerpech ausgesetzt. Kohortenstudien zur Sterblichkeit bei Schornsteinfegern haben ein erhöhtes Lungenkrebsrisiko gezeigt, das auf die Rußbelastung zurückgeführt wurde. Mehrere epidemiologische Studien haben exzessives Auftreten von Atemwegskrebs bei Arbeitern gezeigt, die Pechdämpfen in der Aluminiumproduktion, der Calciumcarbidproduktion und Dachdeckern ausgesetzt waren. In diesen Industriezweigen kommt es auch zu einer Exposition gegenüber Teer und insbesondere Kohlenteer. Andere Industrien, in denen ein Übermaß an Atemwegskrebs auf die Exposition gegenüber Kohlenteerdämpfen zurückzuführen ist, sind die Kohlevergasung und die Koksproduktion (IARC 1987).. In einigen Studien wurde ein erhöhtes Risiko für Atemwegskrebs (hauptsächlich Lungenkrebs) festgestellt, aber nicht alle Studien versuchten, die Abgasbelastung von Dieselmotoren getrennt von anderen Verbrennungsprodukten zu analysieren; zu den untersuchten Berufsgruppen gehören Eisenbahner, Hafenarbeiter, Busgaragenarbeiter, Angestellte von Busunternehmen und Berufskraftfahrer (IARC 1989a). Andere Mischungen von PAKs, die auf ihre Karzinogenität für den Menschen untersucht wurden, sind Ruße, Benzinmotorabgase, Mineralöle, Schieferöle und Bitumen. Schieferöle und unbehandelte und leicht behandelte Mineralöle sind für den Menschen krebserzeugend, während Benzinmotorabgase möglicherweise krebserzeugend sind und hochraffinierte Mineralöle, Bitumen und Ruße hinsichtlich ihrer krebserzeugenden Wirkung für den Menschen nicht klassifizierbar sind (IARC 1987, 1989a).. Obwohl diese Gemische PAK enthalten, wurde für keines davon eine krebserzeugende Wirkung auf die menschliche Lunge nachgewiesen, und der Nachweis der Karzinogenität für unbehandelte und leicht behandelte Mineralöle und für Schieferöle basiert auf einem erhöhten Krebsrisiko von anderen Standorten als Atmungsorgane (hauptsächlich Haut und Hodensack) bei exponierten Arbeitern.
Bis(b-chlorethyl)sulfid, bekannt als Senfgas, war während des Ersten Weltkriegs weit verbreitet, und die Studien von Soldaten, die Senfgas ausgesetzt waren, sowie von Arbeitern, die bei seiner Herstellung beschäftigt waren, haben eine spätere Entwicklung von Lungen- und Nasenkrebs ergeben (IARC 1987).
Zahlreiche epidemiologische Studien haben gezeigt, dass Arbeiter, die Chlormethylmethylether und/oder Bis(chlormethyl)-ether ausgesetzt waren, ein erhöhtes Risiko für Lungenkrebs haben, hauptsächlich für SCLC (IARC 1987).
In einigen, aber nicht allen Studien, die mit Arbeitern in der Textilfaserherstellung, der Acrylnitrilpolymerisation und der Gummiindustrie durchgeführt wurden, wurde festgestellt, dass Arbeiter, die Acrylnitril ausgesetzt waren, ein höheres Lungenkrebsrisiko haben (IARC 1987)..
Übermäßiges Auftreten wurde bei Arbeitern berichtet, die Formaldehyd ausgesetzt waren, einschließlich Chemiearbeitern, Holzarbeitern und Herstellern und Benutzern von Formaldehyd (IARC 1987).. Die Beweise sind am stärksten für Nasen- und Nasenrachenkrebs: Das Auftreten dieser Krebsarten zeigte in mehr als einer Studie einen Dosis-Wirkungs-Gradient, obwohl die Anzahl der exponierten Fälle oft gering war. Andere Neubildungen mit möglicherweise erhöhtem Risiko sind Lungen- und Hirnkrebs und Leukämie.
Ein erhöhtes Risiko für Kehlkopfkrebs wurde in mehreren Studien an Arbeitern festgestellt, die Nebeln und Dämpfen von Schwefelsäure und anderen starken anorganischen Säuren ausgesetzt waren, wie z.. Das Lungenkrebsrisiko war in einigen, aber nicht allen dieser Studien ebenfalls erhöht. Darüber hinaus wurde bei einer Kohorte von Arbeitern in der Isopropanolherstellung nach dem Starksäureverfahren ein Übermaß an Nasennebenhöhlenkrebs festgestellt.
Holzarbeiter haben ein erhöhtes Risiko für Nasenkrebs, insbesondere Adenokarzinom (IARC 1987). Für Möbel- und Schreiner bestätigt sich das Risiko; Studien an Arbeitern in Tischlereien und Tischlereien deuteten auf ein ähnliches übermäßiges Risiko hin, einige Studien ergaben jedoch negative Ergebnisse. Andere Holzindustrien wie Sägewerke und die Zellstoff- und Papierherstellung waren hinsichtlich ihres krebserzeugenden Risikos nicht einstufbar. Obwohl die Karzinogenität von Holzstaub nicht von der IARC bewertet wurde, ist es plausibel anzunehmen, dass Holzstaub für zumindest einen Teil des erhöhten Risikos für nasales Adenokarzinom bei Holzarbeitern verantwortlich ist. Holzarbeiter scheinen kein erhöhtes Krebsrisiko in anderen Atmungsorganen zu haben.
Nasales Adenokarzinom wurde auch durch Beschäftigung in der Stiefel- und Schuhherstellung und -reparatur verursacht (IARC 1987). Andererseits gibt es keine eindeutigen Beweise dafür, dass Arbeiter, die in der Herstellung von Lederprodukten und in der Gerbung und Verarbeitung von Leder beschäftigt sind, einem erhöhten Risiko für Atemwegskrebs ausgesetzt sind. Ob das vermehrte Auftreten von Adenokarzinomen der Nase in der Stiefel- und Schuhindustrie auf Lederstaub oder auf andere Expositionen zurückzuführen ist, ist derzeit nicht bekannt. Die Karzinogenität von Lederstaub wurde von der IARC nicht bewertet.
Lungenkrebs ist unter Uranbergleuten, Untertage-Hämatit-Bergleuten und mehreren anderen Gruppen von Metallbergarbeitern weit verbreitet (IARC 1988; BEIR IV Committee on the Biological Effects of Ionizing Radiation 1988). Allen diesen Berufsgruppen gemeinsam ist die Exposition gegenüber a-Strahlung, die durch eingeatmete Radonpartikel emittiert wird. Die Hauptdatenquelle zu Krebs nach Exposition gegenüber ionisierender Strahlung stammt aus der Nachsorge von Atombombenüberlebenden (Preston et al. 1986; Shimizu et al. 1987).. Das Lungenkrebsrisiko ist bei den Atombombenüberlebenden sowie bei Personen, die eine Strahlentherapie erhalten haben, erhöht (Smith und Doll 1982). Es gibt jedoch derzeit keine überzeugenden Beweise für das Bestehen eines erhöhten Lungenkrebsrisikos bei Arbeitern, die schwacher ionisierender Strahlung ausgesetzt sind, wie sie beispielsweise in der Nuklearindustrie auftreten (Beral et al. 1987; BEIR V, Ausschuss für die biologischen Auswirkungen ionisierender Strahlung 1990). Die Karzinogenität ionisierender Strahlung wurde von der IARC nicht bewertet.
Ein erhöhtes Lungenkrebsrisiko bei Malern wurde in drei großen Kohortenstudien und in acht kleinen Kohorten- und Zensusstudien sowie elf Fall-Kontroll-Studien aus verschiedenen Ländern festgestellt. Andererseits wurden bei Arbeitern, die an der Herstellung von Farben beteiligt waren, kaum Hinweise auf ein erhöhtes Lungenkrebsrisiko gefunden (IARC 1989b)..
Bei einer Reihe anderer Chemikalien, Gemische, Berufe und Industriezweige, die von der IARC als krebserzeugend für den Menschen (IARC-Gruppe 1) eingestuft wurden, ist die Lunge nicht das primäre Zielorgan. Dennoch wurde die Möglichkeit eines erhöhten Lungenkrebsrisikos für einige dieser Chemikalien wie Vinylchlorid (IARC 1987) und Berufe wie das Sprühen und Ausbringen von Insektiziden (IARC 1991a) angesprochen, aber die Beweise sind nicht konsistent .
Darüber hinaus wurden mehrere Wirkstoffe, bei denen die Lunge eines der Hauptziele ist, aufgrund ihrer krebserzeugenden Aktivität bei Versuchstieren und/oder begrenzter epidemiologischer Beweise als mögliche Karzinogene für den Menschen (IARC-Gruppe 2B) angesehen. Dazu gehören anorganische Bleiverbindungen (IARC 1987), Kobalt (IARC 1991b), künstliche Glasfasern (Steinwolle, Schlackenwolle und Glaswolle) (IARC 1988b) und Schweißrauch (IARC 1990c).
Gesundheitliche Auswirkungen von Chemiefasern
Die industrielle Verwendung verschiedener Arten von Chemiefasern hat zugenommen, insbesondere seit die Verwendung von Asbest im Hinblick auf seine bekannten Gesundheitsgefahren eingeschränkt wurde. Das Potenzial für gesundheitsschädliche Auswirkungen im Zusammenhang mit der Herstellung und Verwendung von Chemiefasern wird noch untersucht. Dieser Artikel gibt einen Überblick über die allgemeinen Grundsätze bezüglich des Toxizitätspotenzials solcher Fasern, einen Überblick über die verschiedenen Arten von Fasern in der Produktion (wie in Tabelle 1 aufgeführt) und einen Überblick über bestehende und laufende Studien zu ihren potenziellen gesundheitlichen Auswirkungen .
Tabelle 1. Synthetische Fasern
| Synthetische Fasern |
Aluminium Oxid Kohlenstoff/Graphit Kevlar® Para-Aramid Fasern aus Siliciumcarbid u |
|
| Künstliche glasartige Fasern |
Glasfasern
Mineralwolle
Feuerfeste Keramikfaser |
Glaswolle Steinwolle |
Toxizitätsdeterminanten
Die Hauptfaktoren im Zusammenhang mit dem Toxizitätspotenzial aufgrund der Exposition gegenüber Fasern sind:
- Faserdimension
- Faserhaltbarkeit u
- Dosis zum Zielorgan.
Im Allgemeinen haben Fasern, die lang und dünn sind (aber eine lungengängige Größe haben) und haltbar sind, das größte Potenzial, nachteilige Wirkungen zu verursachen, wenn sie in ausreichender Konzentration an die Lunge abgegeben werden. Die Fasertoxizität wurde in Kurzzeit-Inhalationsstudien an Tieren mit Entzündung, Zytotoxizität, veränderter Makrozytenfunktion und Biopersistenz korreliert. Das krebserzeugende Potenzial hängt höchstwahrscheinlich mit zellulären DNA-Schäden über die Bildung freier Sauerstoffradikale, die Bildung klastogener Faktoren oder die Fehlsegregation von Chromosomen in Zellen in der Mitose zusammen – allein oder in Kombination. Fasern mit lungengängiger Größe sind solche mit einem Durchmesser von weniger als 3.0 bis 3.5 mm und einer Länge von weniger als 200 μm. Gemäß der „Stanton-Hypothese“ hängt das krebserzeugende Potenzial von Fasern (bestimmt durch pleurale Implantationsstudien an Tieren) mit ihrer Größe (das größte Risiko ist mit Fasern mit einem Durchmesser von weniger als 0.25 μm und einer Länge von mehr als 8 mm verbunden) und ihrer Haltbarkeit zusammen (Stanton et al. 1981). Natürlich vorkommende Mineralfasern wie Asbest liegen in einer polykristallinen Struktur vor, die dazu neigt, entlang Längsebenen zu spalten, wodurch dünnere Fasern mit höheren Längen-zu-Breiten-Verhältnissen entstehen, die ein größeres Toxizitätspotential aufweisen. Die überwiegende Mehrheit der Chemiefasern ist nicht kristallin oder amorph und bricht senkrecht zu ihrer Längsebene in kürzere Fasern. Dies ist ein wichtiger Unterschied zwischen Asbest- und Nicht-Asbest-Fasersilikaten und künstlichen Fasern. Die Haltbarkeit von in der Lunge abgelagerten Fasern hängt von der Fähigkeit der Lunge ab, die Fasern zu entfernen, sowie von den physikalischen und chemischen Eigenschaften der Fasern. Die Haltbarkeit von Chemiefasern kann im Produktionsprozess entsprechend den Anforderungen des Endverbrauchs durch Zugabe bestimmter Stabilisatoren wie Al verändert werden2O3. Aufgrund dieser Variabilität der chemischen Bestandteile und der Größe von Chemiefasern muss ihre potenzielle Toxizität Fasertyp für Fasertyp bewertet werden.
Synthetische Fasern
Fasern aus Aluminiumoxid
Die Toxizität von kristallinen Aluminiumoxidfasern wurde durch einen Fallbericht über Lungenfibrose bei einem Arbeiter nahegelegt, der 19 Jahre lang in der Aluminiumschmelze beschäftigt war (Jederlinic et al. 1990). Sein Röntgenbild des Brustkorbs zeigte eine interstitielle Fibrose. Die Analyse des Lungengewebes durch elektronenmikroskopische Techniken zeigte 1.3 × 109 kristalline Fasern pro Gramm trockenes Lungengewebe oder zehnmal mehr Fasern als die Anzahl von Asbestfasern, die im Lungengewebe von Chrysotil-Asbestbergleuten mit Asbestose gefunden wurden. Weitere Studien sind erforderlich, um die Rolle von kristallinen Aluminiumoxidfasern (Abbildung 1) und Lungenfibrose zu bestimmen. Dieser Fallbericht weist jedoch darauf hin, dass es möglicherweise zu einer Faserbildung kommen kann, wenn geeignete Umgebungsbedingungen vorliegen, wie z. B. ein erhöhter Luftstrom über geschmolzene Materialien. Sowohl Phasenkontrast-Lichtmikroskopie als auch Elektronenmikroskopie mit Energiedispersions-Röntgenanalyse sollten verwendet werden, um potenzielle luftgetragene Fasern in der Arbeitsumgebung und in Lungengewebeproben zu identifizieren, wenn klinische Befunde vorliegen, die mit einer faserinduzierten Pneumokoniose übereinstimmen.
Abbildung 1. Rasterelektronenmikroskopische Aufnahme (SEM) von Aluminiumoxidfasern.
Mit freundlicher Genehmigung von T. Hesterberg.
Kohle-/Graphitfasern
Auf 1,200 °C erhitzte kohlenstoffhaltige Pech-, Kunstseide- oder Polyacrylnitrilfasern bilden amorphe Kohlenstoffasern, und wenn sie über 2,20 °C erhitzt werden, bilden sie kristalline Graphitfasern (Abbildung 2). Harzbindemittel können hinzugefügt werden, um die Festigkeit zu erhöhen und das Formen und Bearbeiten des Materials zu ermöglichen. Im Allgemeinen haben diese Fasern einen Durchmesser von 7 bis 10 μm, aber aufgrund des Herstellungsprozesses und der mechanischen Manipulation treten Größenabweichungen auf. Kohlenstoff/Graphit-Verbundwerkstoffe werden in der Flugzeug-, Automobil- und Sportartikelindustrie eingesetzt. Die Exposition gegenüber Kohlenstoff-/Graphitpartikeln in lungengängiger Größe kann während des Herstellungsprozesses und bei mechanischer Manipulation erfolgen. Darüber hinaus können beim Erhitzen von Verbundwerkstoffen auf 900 bis 1,10 °C kleine Mengen lungengängig geschlichteter Fasern erzeugt werden. Das vorhandene Wissen über diese Fasern reicht nicht aus, um eindeutige Antworten auf ihr Potenzial für gesundheitsschädliche Auswirkungen zu geben. Studien mit intratrachealer Injektion verschiedener Graphitfaser-Verbundstäube bei Ratten ergaben heterogene Ergebnisse. Drei der getesteten Staubproben erzeugten eine minimale Toxizität, und zwei der Proben erzeugten eine konsistente Toxizität, die sich durch Zytotoxizität für Alveolarmakrophagen und Unterschiede in der Gesamtzahl der aus der Lunge gewonnenen Zellen manifestierte (Martin, Meyer und Luchtel 1989). Klastogene Wirkungen wurden in Mutagenitätsstudien von Fasern auf Pechbasis beobachtet, nicht jedoch von Kohlefasern auf Polyacrylnitrilbasis. Eine zehnjährige Studie an Arbeitern in der Kohlefaserproduktion, die Fasern mit einem Durchmesser von 8 bis 10 mm herstellten, zeigte keine Anomalien (Jones, Jones und Lyle 1982). Bis weitere Studien verfügbar sind, wird empfohlen, dass die Exposition gegenüber lungengängigen Kohlenstoff-/Graphitfasern 1 Faser/ml (f/ml) oder weniger beträgt und die Exposition gegenüber lungengängigen Verbundpartikeln unter dem aktuellen Grenzwert für lungengängigen Staub gehalten wird lästiger Staub.
Abbildung 2. SEM von Kohlenstofffasern.
Kevlar-Para-Aramid-Fasern
Kevlar Para-Aramid-Fasern haben einen Durchmesser von etwa 12 μm und die gekrümmten, bandartigen Fibrillen auf der Oberfläche der Fasern sind weniger als 1 mm breit (Abbildung 3). Die Fibrillen schälen sich teilweise von den Fasern ab und verzahnen sich mit anderen Fibrillen, um Klumpen zu bilden, die eine nicht lungengängige Größe haben. Die physikalischen Eigenschaften von Kevlar Fasern weisen eine beträchtliche Hitzebeständigkeit und Zugfestigkeit auf. Sie haben viele verschiedene Anwendungen und dienen als Verstärkungsmittel in Kunststoffen, Stoffen und Gummi sowie als Reibmaterial für Autobremsen. Der achtstündige zeitgewichtete Durchschnitt (TWA) der Fibrillenkonzentrationen während der Herstellung und Endanwendung reicht von 0.01 bis 0.4 f/ml (Merriman 1989). Sehr niedrige Werte von Kevlar Aramidfasern werden in Staub erzeugt, wenn sie in Reibungsmaterialien verwendet werden. Die einzigen verfügbaren Daten zu gesundheitlichen Auswirkungen stammen aus Tierversuchen. Inhalationsstudien an Ratten über einen Zeitraum von ein bis zwei Jahren und Expositionen gegenüber Fibrillen bei 25, 100 und 400 f/ml zeigten eine dosisabhängige alveoläre Bronchiolarisierung. Leichte Fibrose und fibrotische Veränderungen der Alveolargänge wurden bei den höheren Expositionsniveaus ebenfalls festgestellt. Die Fibrose könnte mit einer Überlastung der pulmonalen Clearance-Mechanismen zusammenhängen. Ein für Ratten einzigartiger Tumortyp, zystischer keratinisierender Plattenepitheltumor, entwickelte sich bei einigen der Versuchstiere (Lee et al. 1988). Kurzfristige Inhalationsstudien an Ratten weisen darauf hin, dass die Fibrillen im Lungengewebe nur eine geringe Haltbarkeit haben und schnell ausgeschieden werden (Warheit et al. 1992). Es liegen keine Studien zu den Auswirkungen der Exposition auf die menschliche Gesundheit vor Kevlar Para-Aramidfaser. Angesichts des Nachweises einer verminderten Biopersistenz und angesichts der physikalischen Struktur von Kevlar, sollten die Gesundheitsrisiken minimal sein, wenn die Exposition gegenüber Fibrillen bei 0.5 f/ml oder weniger gehalten wird, wie es derzeit bei kommerziellen Anwendungen der Fall ist.
Abbildung 3. SEM von Kevlar-Para-Aramidfasern.
Fasern und Whisker aus Siliciumcarbid
Siliziumkarbid (Carborundum) ist ein weit verbreitetes Schleif- und Feuerfestmaterial, das durch die Kombination von Siliziumdioxid und Kohlenstoff bei 2,400 °C hergestellt wird. Fasern und Whisker aus Siliciumcarbid – Abbildung 4 (Harper et al. 1995) – können als Nebenprodukte bei der Herstellung von Siliciumcarbidkristallen anfallen oder gezielt als polykristalline Fasern oder monokristalline Whisker hergestellt werden. Die Fasern haben im Allgemeinen einen Durchmesser von weniger als 1 bis 2 μm und eine Länge im Bereich von 3 bis 30 μm. Die Whisker haben einen durchschnittlichen Durchmesser von 0.5 μm und eine Länge von 10 μm. Der Einbau von Siliciumcarbidfasern und -whiskern verleiht Produkten wie Metallmatrix-Verbundwerkstoffen, Keramik und keramischen Komponenten Festigkeit. Die Exposition gegenüber Fasern und Whiskern kann während der Produktions- und Herstellungsprozesse und möglicherweise während der Bearbeitungs- und Veredelungsverfahren auftreten. Beispielsweise wurde gezeigt, dass eine kurzfristige Exposition beim Umgang mit recycelten Materialien Werte von bis zu 5 f/ml erreicht. Die maschinelle Bearbeitung von Verbundwerkstoffen mit Metall- und Keramikmatrix hat zu achtstündigen TWA-Expositionskonzentrationen von 0.031 f/ml bzw. bis zu 0.76 f/ml geführt (Scansetti, Piolatto und Botta 1992; Bye 1985).
Abbildung 4. SEMs von Siliziumkarbidfasern (A) und Whiskers (B).
A.
Vorhandene Daten aus Tier- und Humanstudien weisen auf ein eindeutiges fibrogenes und möglicherweise kanzerogenes Potential hin. In vitro Zellkulturstudien an Mäusen mit Siliciumcarbid-Whiskern ergaben eine Zytotoxizität, die gleich oder größer ist als die von Krokydolith-Asbest (Johnson et al. 1992; Vaughan et al. 1991). In einer subakuten Inhalationsstudie wurde eine persistierende adenomatöse Hyperplasie der Rattenlunge nachgewiesen (Lapin et al. 1991). Inhalationsstudien von Schafen mit Siliciumcarbidstaub zeigten, dass die Partikel inert waren. Die Exposition gegenüber Siliciumcarbidfasern führte jedoch zu einer fibrosierenden Alveolitis und einer erhöhten Fibroblasten-Wachstumsaktivität (Bégin et al. 1989). Untersuchungen von Lungengewebeproben von Arbeitern in der Herstellung von Siliziumkarbid zeigten silikotische Knötchen und eisenhaltige Körper und deuteten darauf hin, dass Siliziumkarbidfasern haltbar sind und in hohen Konzentrationen im Lungenparenchym vorkommen können. Röntgenaufnahmen des Brustkorbs stimmten auch mit nodulären und unregelmäßigen interstitiellen Veränderungen und pleuralen Plaques überein.
Siliciumcarbidfasern und -whisker haben eine lungengängige Größe, sind haltbar und haben ein definitives fibrogenes Potential in Lungengewebe. Ein Hersteller von Siliciumcarbid-Whiskers hat einen internen Standard von 0.2 f/ml als 1991-Stunden-TWA festgelegt (Beaumont XNUMX). Dies ist eine vorsichtige Empfehlung auf der Grundlage der derzeit verfügbaren Gesundheitsinformationen.
Künstliche Glasfasern
Synthetische Glasfasern (MMVFs) werden im Allgemeinen klassifiziert als:
- Glasfaser (Glaswolle oder Glasfaser, Endlosglasfilament und Spezialglasfaser)
- Mineralwolle (Steinwolle und Schlackenwolle) und
- Keramikfaser (keramische Textilfaser und feuerfeste Keramikfaser).
Der Herstellungsprozess beginnt mit dem Schmelzen von Rohstoffen mit anschließender schneller Abkühlung, was zur Herstellung von nichtkristallinen (oder glasartigen) Fasern führt. Einige Herstellungsverfahren lassen große Variationen in Bezug auf die Fasergröße zu, wobei die untere Grenze bei 1 mm oder weniger im Durchmesser liegt (Abbildung 5). Stabilisatoren (wie Al2O3TiO2 und ZnO) und Modifikatoren (wie MgO, Li2O, BaO, CaO, Na2O und K2O) hinzugefügt werden, um die physikalischen und chemischen Eigenschaften wie Zugfestigkeit, Elastizität, Dauerhaftigkeit und thermische Nichtübertragung zu verändern.
Abbildung 5. SEM von Schlackenwolle.
Steinwolle, Glasfasern und feuerfeste Keramikfasern sind im Aussehen identisch.
Glasfasern werden aus Siliziumdioxid und verschiedenen Konzentrationen von Stabilisatoren und Modifikatoren hergestellt. Die meiste Glaswolle wird in einem Rotationsverfahren hergestellt, was zu diskontinuierlichen Fasern mit einem durchschnittlichen Durchmesser von 3 bis 15 μm und Schwankungen im Durchmesser von 1 μm oder weniger führt. Die Glaswollefasern werden miteinander verbunden, am häufigsten mit Phenol-Formaldehyd-Harzen, und dann einem wärmehärtenden Polymerisationsprozess unterzogen. Je nach Herstellungsverfahren können auch andere Mittel, einschließlich Gleit- und Netzmittel, zugesetzt werden. Der kontinuierliche Glasfilament-Produktionsprozess führt zu geringeren Abweichungen vom durchschnittlichen Faserdurchmesser im Vergleich zu Glaswolle und Spezialglasfasern. Kontinuierliche Glasfasern haben einen Durchmesser von 3 bis 25 μm. Die Herstellung von Spezialglasfasern beinhaltet einen Flammdämpfungs-Fibrisierungsprozess, der Fasern mit einem durchschnittlichen Durchmesser von weniger als 3 μm produziert.
Die Produktion von Schlackenwolle und Steinwolle umfasst das Schmelzen und Zerfasern von Schlacke aus metallischem Erz bzw. Eruptivgestein. Der Produktionsprozess umfasst ein tellerförmiges Rad und einen Radzentrifugenprozess. Es erzeugt diskontinuierliche Fasern mit einem durchschnittlichen Durchmesser von 3.5 bis 7 μm, deren Größe bis weit in den lungengängigen Bereich reichen kann. Mineralwolle kann je nach Endanwendung mit oder ohne Bindemittel hergestellt werden.
Feuerfeste Keramikfasern werden durch ein Schleuderradzentrifugen- oder Dampfstrahl-Zerfaserungsverfahren unter Verwendung von geschmolzenem Kaolinton, Aluminiumoxid/Siliziumdioxid oder Aluminiumoxid/Siliziumdioxid/Zirkonoxid hergestellt. Durchschnittliche Faserdurchmesser reichen von 1 bis 5 μm. Beim Erhitzen auf Temperaturen über 1,000 °C können feuerfeste Keramikfasern in Cristobalit (ein kristallines Siliziumdioxid) umgewandelt werden.
MMVFs mit unterschiedlichen Faserdurchmessern und chemischer Zusammensetzung werden in über 35,000 Anwendungen eingesetzt. Glaswolle wird in Wohn- und Gewerbeanwendungen zur Schall- und Wärmedämmung sowie in Lüftungssystemen verwendet. Endlosglasfilamente werden in Geweben und als Verstärkungsmittel in Kunststoffen, wie sie in Automobilteilen verwendet werden, verwendet. Spezialglasfasern werden in Spezialanwendungen eingesetzt, beispielsweise in Flugzeugen, die hohe Wärme- und Schalldämmeigenschaften erfordern. Stein- und Schlackenwolle ohne Bindemittel wird als Einblasdämmung und in Deckenplatten verwendet. Stein- und Schlackenwolle mit einem Phenolharz-Bindemittel wird in Isoliermaterialien wie Isoliermatten und -matten verwendet. Feuerfeste Keramikfasern machen 1 bis 2 % der weltweiten Produktion von MMVF aus. Feuerfeste Keramikfasern werden in spezialisierten industriellen Hochtemperaturanwendungen wie Öfen und Brennöfen verwendet. Glaswolle, Endlosglasfaser und Mineralwolle werden in den größten Mengen hergestellt.
Es wird angenommen, dass MMVF aufgrund ihres nicht-kristallinen Zustands und ihrer Neigung, in kürzere Fasern zu zerbrechen, ein geringeres Potenzial als natürlich vorkommende faserige Silikate (wie Asbest) haben, nachteilige Auswirkungen auf die Gesundheit zu haben. Vorhandene Daten deuten darauf hin, dass das am häufigsten verwendete MMVF, Glaswolle, das geringste Risiko für gesundheitsschädliche Auswirkungen aufweist, gefolgt von Stein- und Schlackenwolle und dann sowohl Spezialglasfasern mit erhöhter Haltbarkeit als auch feuerfeste Keramikfasern. Glasfasern für Spezialzwecke und feuerfeste Keramikfasern haben das größte Potenzial, als Fasern mit lungengängiger Größe zu existieren, da sie im Allgemeinen einen Durchmesser von weniger als 3 mm haben. Spezialglasfaser (mit erhöhter Konzentration an Stabilisatoren wie Al2O3) und feuerfeste Keramikfasern sind auch in physiologischen Flüssigkeiten haltbar. Kontinuierliche Glasfilamente haben eine nicht lungengängige Größe und stellen daher kein potenzielles Risiko für die Lungengesundheit dar.
Verfügbare Gesundheitsdaten stammen aus Inhalationsstudien an Tieren und Morbiditäts- und Mortalitätsstudien von Arbeitern, die an der MMVF-Herstellung beteiligt sind. Inhalationsstudien, bei denen Ratten zwei handelsüblichen Isoliermaterialien aus Glaswolle mit einem durchschnittlichen Durchmesser von 1 μm und einer Länge von 20 μm ausgesetzt wurden, zeigten eine leichte Lungenzellreaktion, die sich nach Absetzen der Exposition teilweise umkehrte. Ähnliche Ergebnisse ergaben sich aus einer tierexperimentellen Inhalationsstudie mit einer Art Schlackenwolle. Eine minimale Fibrose wurde bei der Inhalationsexposition von Tieren gegenüber Steinwolle nachgewiesen. Inhalationsstudien mit feuerfester Keramikfaser führten bei Ratten zu Lungenkrebs, Mesotheliom und Pleura- und Lungenfibrose und bei Hamstern zu Mesotheliom und Pleura- und Lungenfibrose bei einer maximal tolerierten Dosis von 250 f/ml. Bei 75 f/ml und 120 f/ml wurde bei Ratten ein Mesotheliom und minimale Fibrose nachgewiesen, und bei 25 f/ml gab es eine Lungenzellreaktion (Bunn et al. 1993).
Haut-, Augen- und obere und untere Atemwegsreizungen können auftreten und hängen von der Expositionshöhe und den Arbeitspflichten ab. Hautirritationen waren die am häufigsten festgestellten gesundheitlichen Auswirkungen und können dazu führen, dass bis zu 5 % der neuen Mitarbeiter in den MMVF-Produktionsanlagen ihre Beschäftigung innerhalb weniger Wochen aufgeben. Sie wird durch mechanisches Trauma der Haut durch Fasern mit einem Durchmesser von mehr als 4 bis 5 μm verursacht. Dies kann durch geeignete Umweltschutzmaßnahmen verhindert werden, einschließlich Vermeidung von direktem Hautkontakt mit den Fasern, Tragen von locker sitzender, langärmliger Kleidung und getrenntem Waschen von Arbeitskleidung. Symptome der oberen und unteren Atemwege können in ungewöhnlich staubigen Situationen auftreten, insbesondere bei der Herstellung von MMVF-Produkten und Endanwendungen sowie in Wohnumgebungen, wenn MMVFs nicht ordnungsgemäß gehandhabt, installiert oder repariert werden.
Studien zur respiratorischen Morbidität, gemessen anhand von Symptomen, Röntgenaufnahmen des Brustkorbs und Lungenfunktionstests bei Arbeitern in Produktionsanlagen, haben im Allgemeinen keine nachteiligen Auswirkungen festgestellt. Eine laufende Studie an Arbeitern in der Fabrik für feuerfeste Keramikfasern hat jedoch eine erhöhte Prävalenz von Pleuraplaques gezeigt (Lemasters et al. 1994). Studien an Arbeitern in der Sekundärproduktion und Endverbrauchern von MMVF sind begrenzt und wurden durch die Wahrscheinlichkeit des Störfaktors früherer Asbestexpositionen behindert.
Sterblichkeitsstudien von Arbeitern in Fabriken zur Herstellung von Glasfasern und Mineralwolle werden in Europa und den Vereinigten Staaten fortgesetzt. Die Daten aus der Studie in Europa zeigten einen allgemeinen Anstieg der Lungenkrebssterblichkeit auf der Grundlage nationaler, aber nicht lokaler Sterblichkeitsraten. In den Glas- und Mineralwolle-Kohorten zeigte sich ein zunehmender Lungenkrebstrend mit der Zeit seit der ersten Beschäftigung, aber nicht mit der Beschäftigungsdauer. Unter Verwendung lokaler Sterblichkeitsraten ergab sich für die früheste Phase der Mineralwolleproduktion ein Anstieg der Lungenkrebsmortalität (Simonato, Fletcher und Cherrie 1987; Boffetta et al. 1992). Die Daten aus der Studie in den Vereinigten Staaten zeigten ein statistisch signifikant erhöhtes Risiko für Atemwegskrebs, konnten jedoch keinen Zusammenhang zwischen der Krebsentstehung und verschiedenen Faserexpositionsindizes finden (Marsh et al. 1990). Dies steht im Einklang mit anderen Fall-Kontroll-Studien an Arbeitern in Fabriken, die Schlackenwolle und Glasfaser herstellen, die ein erhöhtes Lungenkrebsrisiko im Zusammenhang mit dem Zigarettenrauchen gezeigt haben, jedoch nicht in dem Ausmaß der MMVF-Exposition (Wong, Foliart und Trent 1991; Chiazze, Watkins und Fryar 1992). Eine Sterblichkeitsstudie an Arbeitern in der Endlosglasfaden-Fertigung zeigte kein erhöhtes Sterblichkeitsrisiko (Shannon et al. 1990). In den Vereinigten Staaten wird derzeit eine Sterblichkeitsstudie durchgeführt, an der Arbeiter aus feuerfesten Keramikfasern beteiligt sind. Sterblichkeitsstudien von Arbeitern, die an der Produktherstellung beteiligt sind, und Endverbrauchern von MMVF sind sehr begrenzt.
1987 stufte die Internationale Agentur für Krebsforschung (IARC) Glaswolle, Steinwolle, Schlackenwolle und Keramikfasern als mögliche menschliche Karzinogene (Gruppe 2B) ein. Laufende Tierversuche sowie Morbiditäts- und Mortalitätsstudien von Arbeitern, die mit MMVF zu tun haben, werden dazu beitragen, mögliche Risiken für die menschliche Gesundheit genauer zu definieren. Auf der Grundlage verfügbarer Daten ist das Gesundheitsrisiko durch die Exposition gegenüber MMVF sowohl hinsichtlich der Morbidität als auch der Mortalität wesentlich geringer als das, was mit einer Asbestexposition in Verbindung gebracht wurde. Die überwiegende Mehrheit der Studien am Menschen stammen jedoch aus MMVF-Produktionsanlagen, in denen die Expositionswerte im Allgemeinen über einen achtstündigen Arbeitstag unter einem Wert von 0.5 bis 1 f/ml gehalten wurden. Der Mangel an Morbiditäts- und Mortalitätsdaten von Sekundär- und Endverbrauchern von MMVF macht es ratsam, die Exposition gegenüber lungengängigen Fasern auf oder unter diesen Werten durch Umweltkontrollmaßnahmen, Arbeitspraktiken, Arbeiterschulung und Atemschutzprogramme zu kontrollieren. Dies gilt insbesondere bei Exposition gegenüber haltbarer feuerfester Keramik und Spezialglas MMVF und jeder anderen Art von lungengängiger Kunstfaser, die in biologischen Medien haltbar ist und daher im Lungenparenchym abgelagert und zurückgehalten werden kann.
Chronisch obstruktive Lungenerkrankung
Chronische Atemwegserkrankungen, gekennzeichnet durch Dyspnoe unterschiedlichen Grades, Husten, Schleimauswurf und funktionelle Atembeeinträchtigung, werden in die allgemeine Kategorie der chronischen unspezifischen Lungenerkrankung (CNSLD) aufgenommen. Die ursprüngliche Definition von CNSLD, die 1959 auf dem Ciba-Symposium akzeptiert wurde, umfasste chronische Bronchitis, Emphyseme und Asthma. Anschließend wurde die diagnostische Terminologie der chronischen Bronchitis gemäß dem Konzept neu definiert, dass die Deaktivierung der Luftstrombegrenzung das letzte Stadium des fortschreitenden Prozesses darstellt, der mit einem gutartigen Auswurf beginnt, der durch längeres oder wiederholtes Einatmen von bronchialen Reizstoffen verursacht wird (die „britische Hypothese“). . Das Konzept wurde 1977 in Frage gestellt und seitdem werden Hypersekretion und Atemwegsobstruktion als voneinander unabhängige Prozesse angesehen. Die alternative Hypothese, bekannt als „niederländische Hypothese“, akzeptiert zwar die Rolle des Rauchens und der Luftverschmutzung in der Ätiologie der chronischen Einschränkung des Luftstroms, weist aber auf die Schlüssel- und möglicherweise ursächliche Rolle der Anfälligkeit des Wirts hin, die sich beispielsweise manifestiert als: eine asthmatische Neigung. Nachfolgende Studien haben gezeigt, dass beide Hypothesen zum Verständnis des natürlichen Verlaufs chronischer Atemwegserkrankungen beitragen können. Obwohl die Schlussfolgerung über den unbedeutenden prognostischen Wert des hypersekretorischen Syndroms allgemein als gut begründet akzeptiert wurde, haben die jüngsten Studien einen signifikanten Zusammenhang zwischen der hypersekretorischen Störung und dem erhöhten Risiko für die Entwicklung einer Atemwegsbeschränkung und respiratorischer Mortalität gezeigt.
Gegenwärtig kombiniert der Begriff CNSLD zwei Hauptkategorien chronischer Atemwegserkrankungen, Asthma (das in einem separaten Artikel dieses Kapitels erörtert wird) und chronisch obstruktive Lungenerkrankung (COPD).
Definition
In einem von der American Thoracic Society (ATS) (1987) veröffentlichten Dokument wird COPD als eine Störung definiert, die durch abnorme Tests des Ausatmungsflusses gekennzeichnet ist, die sich über einen Beobachtungszeitraum von mehreren Monaten nicht merklich ändern. Unter Berücksichtigung der funktionellen und strukturellen Ursachen der Einschränkung des Luftstroms umfasst die Definition die folgenden nicht-asthmatischen Atemwegserkrankungen: chronische Bronchitis, Emphysem und periphere Atemwegserkrankung. Die wichtigen gemeinsamen Merkmale der COPD sind ausgeprägte pathophysiologische Anomalien, die sich meist als chronische Luftflussbeschränkung (CAL) in unterschiedlichem Ausmaß zeigen. Eine chronische Einschränkung des Luftstroms kann bei einem Subjekt mit irgendeiner Krankheit gefunden werden, die unter die Rubrik COPD fällt.
Chronische Bronchitis ist definiert als ein abnormer Zustand der Atemwege, der durch anhaltenden und übermäßig produktiven Husten gekennzeichnet ist, der die Schleimhypersekretion in den Atemwegen widerspiegelt. Aus epidemiologischen Gründen basiert die Diagnose einer chronischen Bronchitis auf Antworten auf eine Reihe von Standardfragen, die im Fragebogen des Medical Research Council (MRC) oder ATS zu respiratorischen Symptomen enthalten sind. Die Störung ist definiert als Husten- und Schleimauswurf, der an den meisten Tagen für mindestens drei Monate im Jahr während mindestens zwei aufeinanderfolgenden Jahren auftritt.
Ein Emphysem ist definiert als eine anatomische Veränderung der Lunge, gekennzeichnet durch eine abnormale Vergrößerung der Lufträume distal der terminalen Bronchiole, begleitet von einer Zerstörung der Azinusarchitektur. Ein Emphysem tritt häufig zusammen mit einer chronischen Bronchitis auf.
Die periphere Atemwege Gedächtnisverlust und Demenz (z.B. Alzheimer) erhöhen or Krankheit der kleinen Atemwege wird verwendet, um den abnormalen Zustand von Atemwegen mit einem Durchmesser von weniger als 2 bis 3 mm zu beschreiben. Entzündung, Obstruktion und übermäßige Schleimproduktion in diesem Teil des Bronchialbaums wurden bei einer Vielzahl von klinischen Entitäten beobachtet, einschließlich chronischer Bronchitis und Emphysem. Der pathologische Nachweis lokaler struktureller Anomalien und das Konzept, dass die beobachteten Veränderungen ein frühes Stadium im natürlichen Verlauf einer chronischen Atemwegserkrankung darstellen können, haben in den späten 1960er und den 1970er Jahren eine rasche Entwicklung von Funktionstests angeregt, die zur Untersuchung physiologischer Eigenschaften entwickelt wurden periphere Atemwege. Folglich der Begriff periphere Atemwegserkrankung wird im Allgemeinen so verstanden, dass es sich auf strukturelle Anomalien oder funktionelle Defekte bezieht.
CAL ist ein funktionelles Kennzeichen von COPD. Der Begriff bezieht sich auf einen erhöhten Widerstand gegen den Luftstrom, der zu einer anhaltenden Verlangsamung während der forcierten Ausatmung führt. Ihre Definition und das zugrunde liegende klinische und pathophysiologische Wissen implizieren zwei wichtige diagnostische Hinweise. Erstens muss ein chronischer Verlauf nachgewiesen werden, und die frühe Empfehlung von 1958 erforderte das Vorhandensein von CAL für mehr als ein Jahr, um die diagnostischen Kriterien zu erfüllen. Der zuletzt vorgeschlagene Zeitrahmen ist weniger streng und bezieht sich auf den Nachweis eines Mangels über einen Zeitraum von drei Monaten. Bei der Überwachung arbeitsbedingter CAL bietet die standardmäßige spirometrische Auswertung ausreichende Mittel zur Identifizierung von CAL, basierend auf der Verringerung des forcierten Exspirationsvolumens in einer Sekunde (FEV1) und/oder im Verhältnis von FEV1 zur forcierten Vitalkapazität (FVC).
Normalerweise wird CAL diagnostiziert, wenn das FEV1 Wert unter 80 % des vorhergesagten Werts reduziert wird. Gemäß der von der American Thoracic Society empfohlenen funktionellen Klassifikation von CAL:
- leichte Beeinträchtigung tritt auf, wenn der Wert von FEV1 unter 80 % und über 60 % des vorhergesagten Werts liegt
- Eine mäßige Beeinträchtigung tritt auf, wenn FEV1 liegt im Bereich von 40 % bis 59 % des vorhergesagten Werts
- schwere Beeinträchtigung tritt auf, wenn FEV1 unter 40 % des vorhergesagten Werts liegt.
Wenn der Grad der Beeinträchtigung durch den Wert des FEV beurteilt wird1/FVC-Verhältnis wird ein leichter Defekt diagnostiziert, wenn das Verhältnis zwischen 60 % und 74 % fällt; moderate Beeinträchtigung, wenn das Verhältnis zwischen 41 % und 59 % liegt; und schwere Beeinträchtigung, wenn das Verhältnis 40 % oder weniger beträgt.
Prävalenz von COPD
Gehäufte Beweise deuten darauf hin, dass COPD in vielen Ländern ein häufiges Problem ist. Die Prävalenz ist bei Männern höher als bei Frauen und nimmt mit dem Alter zu. Chronische Bronchitis, eine gut standardisierte diagnostische Form der COPD, ist bei Männern zwei- bis dreimal häufiger als bei Frauen. Große Erhebungen belegen, dass in der Regel zwischen 10 % und 20 % der erwachsenen Männer in der Allgemeinbevölkerung die diagnostischen Kriterien einer chronischen Bronchitis erfüllen (Tabelle 18). Die Krankheit tritt bei Rauchern viel häufiger auf, sowohl bei Männern als auch bei Frauen. Das Auftreten von COPD in Berufsgruppen wird weiter unten diskutiert.
Tabelle 1. Prävalenz von COPD in ausgewählten Ländern – Ergebnisse großer Erhebungen
| Land | Jahr | Grundgesamtheit | Males | Frauen | ||||
| SMK (%) | CB (%) | COPD/CAL (%) | SMK (%) | CB (%) | COPD/CAL (%) | |||
| USA | 1978 | 4,699 | 56.6 | 16.5 | nr | 36.2 | 5.9 | nr |
| USA | 1982 | 2,540 | 52.8 | 13.0 | 5.2 | 32.2 | 4.1 | 2.5 |
| UK | 1961 | 1,569 | 17.0 | nr | nr | 8.0 | nr | |
| Italien | 1988 | 3,289 | 49.2 | 13.1 | nr | 26.9 | 2.8 | nr |
| Polen | 1986 | 4,335 | 59.6 | 24.2 | 8.5 | 26.7 | 10.4 | 4.9 |
| Nepal | 1984 | 2,826 | 78.3 | 17.6 | nr | 58.9 | 18.9 | nr |
| Japan | 1977 | 22,590 | nr | 5.8 | nr | nr | 3.1 | nr |
| Australien | 1968 | 3,331 | nr | 6.3 | nr | nr | 2.4 | nr |
Legende: SMK = Rauchgewohnheit; CB = chronische Bronchitis; COPD/CAL = chronisch obstruktive Lungenerkrankung/chronische Einschränkung der Atemwege; nr = nicht gemeldet.
Modifiziert mit Genehmigung von: Woolcock 1989.
Risikofaktoren von COPD, einschließlich Auswirkungen beruflicher Expositionen
COPD ist eine Erkrankung multifaktorieller Ätiologie. Zahlreiche Studien belegen eine ursächliche Abhängigkeit der COPD von vielen Risikofaktoren, kategorisiert als Wirts- und Umweltfaktoren. Die Rolle berufsbedingter Expositionen unter den umweltbedingten Risikofaktoren bei der Entstehung von COPD wurde nach der Häufung epidemiologischer Beweise, die im Zeitraum 1984 bis 1988 veröffentlicht wurden, anerkannt. Kürzlich wurden unabhängige Wirkungen des Rauchens und berufsbedingter Expositionen bestätigt, basierend auf den Ergebnissen der veröffentlichten Studien von 1966 bis 1991. Tabelle 2 fasst den aktuellen Wissensstand zur multifaktoriellen Ätiologie der COPD zusammen.
Tabelle 2. Risikofaktoren im Zusammenhang mit COPD
| Faktor Ähnliche |
Etabliert | Vermutlich |
| Gastgeber | Geschlechtsalter Antitrypsinmangel | Atopie Familiäre Faktoren Erhöhte Reaktivität der Atemwege Frühere Gesundheit |
| Arbeitsumfeld | Tabakrauch (persönlich) | Tabakrauch (Umwelt-) Luftverschmutzung Berufliche Exposition |
Wiedergabe mit freundlicher Genehmigung von: Becklake et al. 1988.
Das Auftreten einer chronischen Bronchitis in Berufsgruppen ist ein potenzieller Marker für eine signifikante Exposition gegenüber berufsbedingten Reizstoffen. Bei Arbeitern im Kohlebergbau, in der Eisen- und Stahlindustrie sowie in der Textil-, Bau- und Landwirtschaftsindustrie wurde ein signifikanter Effekt der Exposition gegenüber Industriestaub auf die Entwicklung einer chronischen Bronchitis dokumentiert. Im Allgemeinen sind staubigere Umgebungen mit einer höheren Prävalenz der Symptome des chronischen Auswurfs verbunden. Die Prävalenzstudien unterliegen jedoch dem „Healthy-Worker-Effekt“, einer Verzerrung, die zu einer Unterschätzung der gesundheitlichen Auswirkungen schädlicher Expositionen am Arbeitsplatz führt. Aussagekräftiger, aber weniger verfügbar, sind Daten zur Häufigkeit der Krankheit. In bestimmten Berufen ist die Inzidenzrate von chronischer Bronchitis hoch und reicht von 197-276/10,000 bei Landwirten bis zu 380/10,000 bei Ingenieurarbeitern und 724/10,000 bei Bergleuten und Steinbrucharbeitern, verglichen mit 108/10,000 bei Angestellten.
Dieses Muster und auch die ursächliche Wirkung des Rauchens stehen im Einklang mit dem Konzept, dass chronische Bronchitis eine häufige Reaktion auf das chronische Einatmen von Reizstoffen der Atemwege darstellt.
Es wird angenommen, dass eine schädliche Wirkung der Lungenstaubbelastung zu einer chronischen unspezifischen Bronchialwandentzündung führt. Diese Art von Entzündungsreaktion wurde bei Arbeitern dokumentiert, die organischem Staub und seinen Bestandteilen ausgesetzt waren, wie zum Beispiel Getreide und Endotoxin, die beide für neutrophile Entzündungen verantwortlich sind. Die Rolle der individuellen Anfälligkeit kann nicht ausgeschlossen werden, und bekannte wirtsbezogene Faktoren umfassen frühere Atemwegsinfektionen, die Effizienz von Clearance-Mechanismen und schlecht bestimmte genetische Faktoren, während Zigarettenrauchen eine der stärksten umweltbedingten Ursachen für chronische Bronchitis bleibt.
Der Beitrag beruflicher Expositionen zur Ätiologie des Emphysems ist nicht eindeutig geklärt. Zu den mutmaßlichen ursächlichen Faktoren zählen Stickoxide, Ozon und Cadmium, wie experimentelle Beobachtungen vermuten lassen. Die von der Berufsepidemiologie gelieferten Daten sind weniger überzeugend und aufgrund der normalerweise geringen beruflichen Expositionen und einer vorherrschenden Wirkung des Rauchens möglicherweise schwer zu erhalten. Dies ist besonders wichtig bei sog zentriazinäres Emphysem. Die andere pathologische Form der Krankheit, das panazinäre Emphysem, gilt als erblich und mit Alpha verwandt1-Antitrypsinmangel.
Bronchioläre und peribronchioläre Entzündungen, begleitet von einer fortschreitenden Verengung des betroffenen Segments des Bronchialbaums (periphere Atemwegserkrankung oder konstriktive Bronchiolitis), können bei einer Vielzahl von Erkrankungen beobachtet werden, die COPD-Symptomen in verschiedenen Stadien des natürlichen Verlaufs zugrunde liegen. Im beruflichen Umfeld folgt die Krankheit in der Regel auf eine akute Lungenschädigung durch Einatmen giftiger Dämpfe wie Schwefeldioxid, Ammoniak, Chlor und Stickoxide. Die Berufsepidemiologie der konstriktiven Bronchiolitis ist jedoch noch weitgehend ungeklärt. Anscheinend sind seine frühen Stadien aufgrund der unspezifischen Symptomatik und der Einschränkung des diagnostischen Verfahrens schwer zu identifizieren. Mehr ist über die Fälle nach Arbeitsunfällen bekannt. Andernfalls kann die Krankheit unentdeckt bleiben, bis sich eine offensichtliche Symptomatologie und eine objektive Beeinträchtigung der Atmung (dh eine chronische Einschränkung des Luftstroms) entwickeln.
CAL ist nicht selten in verschiedenen Berufsgruppen anzutreffen und kann, wie kontrollierte Studien belegen, bei Arbeitern die Prävalenz von Angestellten übertreffen. Aufgrund der komplexen Ätiologie von CAL, einschließlich der Wirkung des Rauchens und wirtsbezogener Risikofaktoren, waren frühe Studien zum Zusammenhang zwischen chronischer Atemwegsbeschränkung und beruflicher Exposition nicht schlüssig. Die moderne Berufsepidemiologie, die zielgerichtetes Design und Modellierung von Expositions-Wirkungs-Beziehungen verwendet, hat Hinweise auf einen Zusammenhang zwischen der Luftstromkapazität und der Exposition gegenüber sowohl mineralischen als auch organischen Stäuben, Dämpfen und Gasen geliefert.
Arbeitsbezogene Längsschnittstudien, die an Arbeitern durchgeführt wurden, die mineralischen und organischen Stäuben sowie Dämpfen und Gasen ausgesetzt waren, zeigen, dass der Verlust der Lungenfunktion mit berufsbedingter Exposition verbunden ist. Die in Tabelle 3 zusammengefassten Ergebnisse belegen einen signifikanten Effekt der Staubexposition im Kohle- und Eisenbergbau, in der Asbestzementindustrie, bei Stahl- und Hüttenarbeitern sowie Arbeitern in Zellstofffabriken. Eine Reihe von analysierten Expositionen setzt sich aus der Exposition gegenüber Staub und Rauch (z. B. nichthalogenierte Kohlenwasserstoffe, Farben, Harze oder Lacke) sowie Gasen (z. B. Schwefeldioxid oder Stickoxiden) zusammen. Nach den Ergebnissen einer umfassenden Überprüfung, die sich auf die validesten und systematisch analysierten Artikel zu COPD und beruflicher Staubbelastung beschränkt, kann geschätzt werden, dass bei 80 von 1,000 nicht rauchenden Bergleuten ein FEV-Verlust von mindestens 20 % zu erwarten ist1 nach 35 Jahren Arbeit mit einer mittleren Atemstaubkonzentration von 2 mg/m3, und für nicht rauchende Goldgräber könnte das entsprechende Risiko dreimal so groß sein.
Tabelle 3. Verlust der Atmungsfunktion in Bezug auf berufliche Expositionen: Ergebnisse ausgewählter arbeitsplatzbezogener Längsschnittstudien
| Land (Jahr) | Themen und Expositionen | Prüfung verwendet | Jährlicher Funktionsverlust* | |||
| NE | E | NS | S | |||
| UK (1982) | 1,677 Bergleute | FEV ml | 37 | 41 57 (max) |
37 | 48 |
| USA (1985) | 1,072 Bergleute | FEV ml | 40 | 47 | 40 | 49 |
| Italien (1984) | 65 Asbestzementarbeiter | FEV ml | 9 | 49 | Nicht gegeben | Nicht gegeben |
| Schweden (1985) | 70 Asbestzementarbeiter | FEV% | 4.2 | 9.2 | 3.7 | 9.4 |
| Frankreich (1986) | 871 Eisenbergleute | FEV% | 6 | 8 | 5 | 7 |
| Frankreich (1979) | 159 Stahlarbeiter | FEV% | 0.6 | 7.4 | Nicht gegeben | Nicht gegeben |
| Kanada (1984) | 179 Minen- und Hüttenarbeiter | FEV/FVC % | 1.6 | 3.1 | 2.0 | 3.4 |
| Frankreich (1982) | 556 Arbeiter in Fabriken | FEV ml | 42 | 50 52 (Staub) 47 (Gase) 55 (Hitze) |
40 | 48 |
| Finnland (1982) | 659 Arbeiter in Zellstofffabriken | FEV ml | keine Wirkung | keine Wirkung | 37 | 49 |
| Kanada (1987) | 972 Minen- und Hüttenarbeiter | FEV ml | 69 (Bräter) 49 (Ofen) 33 (Bergbau) |
41 | 54 | |
* Die Tabelle zeigt den durchschnittlichen jährlichen Verlust der Lungenfunktion bei Exponierten (E) im Vergleich zu Nicht-Exponierten (NE) und bei Rauchern (S) im Vergleich zu Nichtrauchern (NS). Unabhängige Wirkungen des Rauchens (S) und/oder der Exposition (E) erwiesen sich in den von den Autoren durchgeführten Analysen in allen Studien außer der finnischen Studie als signifikant.
Modifiziert mit Genehmigung von: Becklake 1989.
Ausgewählte Studien, die mit Getreidearbeitern durchgeführt wurden, zeigen die Wirkung einer beruflichen Exposition gegenüber organischem Staub auf longitudinale Veränderungen der Lungenfunktion. Obwohl in Anzahl und Dauer der Nachbeobachtung begrenzt, dokumentieren die Befunde einen unabhängigen Zusammenhang des Rauchens mit dem jährlichen Lungenfunktionsverlust (gegenüber der Exposition gegenüber Getreidestaub).
Pathogenese
Die zentrale pathophysiologische Störung der COPD ist die chronische Einschränkung des Luftstroms. Die Störung resultiert aus einer Verengung der Atemwege – ein Zustand, der bei chronischer Bronchitis einen komplexen Mechanismus hat – während bei einem Emphysem die Obstruktion der Atemwege hauptsächlich auf eine geringe elastische Rückfederung des Lungengewebes zurückzuführen ist. Beide Mechanismen koexistieren oft.
Die strukturellen und funktionellen Anomalien, die bei chronischer Bronchitis beobachtet werden, schließen Hypertrophie und Hyperplasie der submukösen Drüsen ein, die mit Schleimhypersekretion verbunden sind. Die entzündlichen Veränderungen führen zu einer Hyperplasie der glatten Muskulatur und Schleimhautschwellungen. Die Schleimübersekretion und Atemwegsverengung begünstigen bakterielle und virale Infektionen der Atemwege, die die Atemwegsobstruktion weiter verstärken können.
Die Einschränkung des Luftstroms beim Emphysem spiegelt den Verlust des elastischen Rückstoßes als Folge der Zerstörung von Elastinfasern und des Kollabierens der Bronchiolenwand aufgrund hoher Lungencompliance wider. Es wird angenommen, dass die Zerstörung von Elastinfasern aus einem Ungleichgewicht im proteolytisch-antiproteolytischen System resultiert, in einem Prozess, der auch als bekannt ist Protease-Inhibitor-Mangel. Alpha1-Antitrypsin ist die stärkste Protease, die die Elastase-Wirkung auf Alveolen beim Menschen hemmt. Neutrophile und Makrophagen, die Elastase freisetzen, reichern sich als Reaktion auf lokale Entzündungsmediatoren und das Einatmen verschiedener respiratorischer Reizstoffe, einschließlich Tabakrauch, an. Die anderen, weniger starken Inhibitoren sind a2-Makroglobulin und Elastasehemmer mit niedrigem Gewicht, die aus submukösen Drüsen freigesetzt werden.
Vor kurzem wurde die Antioxidans-Mangel-Hypothese auf ihre Rolle in den pathogenetischen Mechanismen von Emphysemen untersucht. Die Hypothese besagt, dass Oxidantien, wenn sie nicht durch Antioxidantien gehemmt werden, das Lungengewebe schädigen und zu einem Lungenemphysem führen. Bekannte Oxidationsmittel umfassen exogene Faktoren (Ozon, Chlor, Stickoxide und Tabakrauch) und endogene Faktoren wie freie Radikale. Zu den wichtigsten antioxidativen Faktoren gehören natürliche Antioxidantien wie die Vitamine E und C, Katalase, Superoxiddysmutase, Glutathion, Ceruloplasmin und synthetische Antioxidantien wie N-Acetylcystein und Allopurinol. Es gibt immer mehr Beweise für einen Synergismus in Bezug auf Antioxidans-Mangel- und Protease-Inhibitor-Mangel-Mechanismen in der Pathogenese von Emphysemen.
Pathologie
Pathologisch ist die chronische Bronchitis durch Hypertrophie und Hyperplasie der Drüsen in der Submukosa der großen Atemwege gekennzeichnet. Dadurch wird das Verhältnis der Bronchialdrüsendicke zur Bronchialwanddicke (sog Reid-Index) erhöht sich. Andere pathologische Anomalien umfassen Metaplasie des Ziliarepithels, Hyperplasie der glatten Muskulatur und neutrophile und lymphozytäre Infiltrationen. Die Veränderungen in den großen Atemwegen werden oft von pathologischen Anomalien in den kleinen Bronchiolen begleitet.
Pathologische Veränderungen in kleinen Bronchiolen wurden durchweg als unterschiedliche Grade des entzündlichen Prozesses der Atemwegswände dokumentiert. Nach der Einführung des Konzepts der Erkrankung der kleinen Atemwege lag der Fokus auf der Morphologie einzelner Bronchiolensegmente. Die histologische Beurteilung der häutigen Bronchiolen, später erweitert auf die respiratorischen Bronchiolen, zeigt Wandentzündung, Fibrose, Muskelhypertrophie, Pigmentablagerungen, epitheliale Kelch- und Plattenepithelmetaplasie und intraluminale Makrophagen. Pathologische Anomalien des oben beschriebenen Typs wurden als „Mineralstaub-induzierte Atemwegserkrankung“ bezeichnet. Eine assoziierte Erkrankung, die in diesem Abschnitt des Respirationstrakts nachgewiesen wurde, ist die peribronchioläre fibrosierende Alveolitis, von der angenommen wird, dass sie die frühe Reaktion des Lungengewebes auf das Einatmen von Mineralstaub darstellt.
Pathologische Veränderungen beim Emphysem können kategorisiert werden als zentriazinäres Emphysem or Panacinäres Emphysem. Die erstgenannte Entität ist weitgehend auf das Zentrum des Acinus beschränkt, während die letztere Form Veränderungen in allen Strukturen des Acinus beinhaltet. Obwohl angenommen wird, dass das panazinäre Emphysem einen erblichen Mangel an Protease-Inhibitoren widerspiegelt, können beide Formen koexistieren. Beim Emphysem zeigen die terminalen Bronchiolen Anzeichen einer Entzündung und die distalen Lufträume sind abnormal erweitert. Die strukturelle Zerstörung betrifft Alveolen, Kapillaren und kann zur Bildung großer abnormaler Lufträume führen (Emphysema bullosum). Das zentriazinäre Emphysem befindet sich in der Regel in den oberen Lungenlappen, während das panazinäre Emphysem normalerweise in den unteren Lungenlappen zu finden ist.
Klinische Symptome
Chronischer Husten und Schleimauswurf sind zwei Hauptsymptome einer chronischen Bronchitis, während Dyspnoe (Kurzatmigkeit) ein klinisches Merkmal eines Emphysems ist. In fortgeschrittenen Fällen treten die Symptome des chronischen Auswurfs und der Dyspnoe gewöhnlich gleichzeitig auf. Der Beginn und das Fortschreiten der Dyspnoe deuten auf die Entwicklung einer chronischen Einschränkung des Atemflusses hin. Entsprechend den Symptomen und dem physiologischen Status umfasst das klinische Erscheinungsbild der chronischen Bronchitis drei Krankheitsformen: einfache, schleimig-eitrige und obstruktive Bronchitis.
Bei chronischer Bronchitis können die Ergebnisse der Thoraxauskultation normale Atemgeräusche zeigen. In fortgeschrittenen Fällen kann es während der Exspiration zu einer verlängerten Exspirationszeit, Keuchen und Rasseln kommen. Zyanose ist bei fortgeschrittener obstruktiver Bronchitis häufig.
Die klinische Diagnose eines Emphysems ist im Frühstadium schwierig. Dyspnoe kann ein Einzelbefund sein. Der Patient mit fortgeschrittenem Emphysem kann einen Brustkorb und Anzeichen einer Hyperventilation haben. Als Folge der Lungenüberblähung sind weitere Befunde Hyperresonanz, Abnahme der Zwerchfellexkursion und verminderte Atemgeräusche. Zyanose ist selten.
Aufgrund ähnlicher ursächlicher Faktoren (überwiegend die Wirkung von Tabakrauch) und ähnlicher Präsentation kann die Diagnose einer chronischen Bronchitis gegenüber einem Emphysem schwierig sein, insbesondere wenn eine chronische Einschränkung des Atemflusses das Bild dominiert. Tabelle 4 enthält einige Anhaltspunkte, die für die Diagnose hilfreich sind. Die fortgeschrittene Form der COPD kann zwei extreme Formen annehmen: überwiegende Bronchitis („blauer Blähbauch“) oder überwiegendes Lungenemphysem („rosa Kugelfisch“).
Tabelle 4. Diagnostische Klassifikation von zwei klinischen COPD-Typen, chronische Bronchitis und Emphysem
| Anzeichen / Symptome | Vorherrschende Bronchitis („Blauer Bläser“) |
Vorherrschendes Emphysem („Rosa Puffer“) |
| Körpermasse | Mehr | Verringert |
| Zyanose | Häufig | Selten |
| Husten | Vorherrschendes Symptom | Intermittierend |
| Sputum | Große Menge | Selten |
| Dyspnoe | Normalerweise während des Trainings markiert | Vorherrschendes Symptom |
| Atemgeräusche | Normal oder leicht vermindert, zufällige Lungengeräusche |
Verringert |
| Cor pulmonale | Häufig | Selten |
| Infektionen der Atemwege | Häufig | Selten |
Die Thoraxradiologie hat einen begrenzten diagnostischen Wert bei chronischer Bronchitis und frühen Stadien eines Lungenemphysems. Fortgeschrittenes Emphysem zeigt ein radiologisches Muster einer erhöhten Aufhellung (Hyperinflation). Die Computertomographie bietet einen besseren Einblick in den Ort und das Ausmaß emphysematöser Veränderungen, einschließlich der Unterscheidung zwischen zentriazinärem und panazinärem Emphysem.
Lungenfunktionstests haben einen etablierten Stellenwert in der COPD-Diagnostik (Tabelle 5). Die Reihe von Tests, die bei der funktionellen Beurteilung von chronischer Bronchitis und Emphysemen von praktischer Bedeutung sind, umfasst die funktionelle Residualkapazität (FRC), das Residualvolumen (RV), die Gesamtlungenkapazität (TLC) und das FEV1 und FEV1/VC, Atemwegswiderstand (Raw), statische Nachgiebigkeit (Cst), elastischer Rückstoß (SL,el), Blutgase (PaO2, PaCO2) und Diffusionsvermögen (DLCO).
Tabelle 5. Lungenfunktionstests in der Differentialdiagnose von zwei klinischen Typen von COPD, chronischer Bronchitis und Emphysem
| Lungenfunktionstest | Vorherrschende Bronchitis („Blauer Bläser“) |
Vorherrschendes Emphysem („Rosa Puffer“) |
| RV, FRC, TLC | Normal oder leicht erhöht | Deutlich erhöht |
| FEV1 , FEV1 /VK | Verringert | Verringert |
| Raw | Deutlich erhöht | Leicht erhöht |
| Cst | Normal | Deutlich erhöht |
| PL,el | Normal | Deutlich erhöht |
| PaO2 | Deutlich erhöht | Leicht verringert |
| PaCO2 | Mehr | Normal |
| DLCO | Normal oder leicht vermindert | Verringert |
RV = Residualvolumen; FRC = funktionelle Restkapazität; TLC = Gesamtlungenkapazität; FEV1 = forciertes Exspirationsvolumen in der ersten Sekunde und VC = Vitalkapazität; Raw = Atemwegswiderstand; Cst = statische Nachgiebigkeit; PL,el = elastischer Rückstoß; PaO2 und PaCO2 = Blutgase; DLCO = Diffusionskapazität.
Eine klinische Diagnose einer peripheren Atemwegserkrankung ist nicht möglich. Sehr oft begleitet die Erkrankung eine chronische Bronchitis oder ein Emphysem oder geht sogar der klinischen Präsentation der beiden letztgenannten Formen oder der COPD voraus. Die isolierte Form der peripheren Atemwegserkrankung kann durch Lungenfunktionstests untersucht werden, obwohl der Funktionsstatus der peripheren Atemwege schwer zu beurteilen ist. Dieser Teil des Bronchialbaums trägt zu weniger als 20 % des gesamten Luftstromwiderstands bei, und isolierte, leichte Anomalien in den kleinen Atemwegen liegen unterhalb der Nachweisgrenze der konventionellen Spirometrie. Zu den empfindlicheren Methoden zur Messung der Funktion der peripheren Atemwege gehören eine Reihe von Tests, von denen die folgenden am häufigsten verwendet werden: maximale mittelexspiratorische Flussrate (FEF25-75), Flussraten bei niedrigen Lungenvolumina (MEF50, MEF25), Stickstoffindex für einen einzelnen Atemzug (SBN2/l), Schließvermögen (CC), Leitwert des stromaufwärtigen Luftstroms (Gus) und frequenzabhängige Compliance (Cfd). Im Allgemeinen wird angenommen, dass diese Tests eine geringe Spezifität haben. Aus theoretischen Gründen FEF25-75 und MEF50,25 sollte in erster Linie kaliberbegrenzende Mechanismen widerspiegeln, während SBN2Es wird angenommen, dass /l spezifischer für die mechanischen Eigenschaften von Lufträumen ist. Die erstgenannten Indizes werden am häufigsten in der Berufsepidemiologie verwendet.
Differenzialdiagnose
Grundlegende Unterschiede zwischen chronischer Bronchitis und Emphysem sind in den Tabellen 4 und 5 dargestellt. In Einzelfällen ist die Differentialdiagnose jedoch schwierig und manchmal nicht mit einiger Sicherheit durchzuführen. In manchen Fällen ist es auch schwierig, COPD von Asthma zu unterscheiden. In der Praxis sind Asthma und COPD keine eindeutigen Entitäten, und es gibt ein hohes Maß an Überschneidungen zwischen den beiden Krankheiten. Bei Asthma ist die Atemwegsobstruktion normalerweise intermittierend, während sie bei COPD konstant ist. Der Verlauf der Luftstrombegrenzung ist bei Asthma variabler als bei COPD.
Case Management
Die klinische Behandlung von COPD beinhaltet die Raucherentwöhnung, die wirksamste Einzelmaßnahme. Berufliche Exposition gegenüber Reizstoffen der Atemwege sollte eingestellt oder vermieden werden. Das klinische Management sollte sich auf die richtige Behandlung von Atemwegsinfektionen konzentrieren und regelmäßige Influenza-Impfungen umfassen. Eine bronchodilatatorische Therapie ist bei Patienten mit eingeschränktem Luftstrom gerechtfertigt und sollte umfassen b2-adrenerge Agonisten und Anticholinergika, verabreicht als Monotherapie oder in Kombination, vorzugsweise als Aerosol. Theophyllin wird immer noch verwendet, obwohl seine Rolle bei der Behandlung von COPD umstritten ist. In einigen Fällen kann eine Langzeittherapie mit Kortikosteroiden wirksam sein. Die bronchiale Hypersekretion wird oft durch mukoaktive Medikamente behandelt, die die Schleimproduktion, die Schleimstruktur oder die mukozilliäre Clearance beeinflussen. Die Beurteilung der Wirkung einer mukolytischen Therapie ist schwierig, da diese Medikamente nicht als Monotherapie der COPD eingesetzt werden. Patienten mit Hypoxämie (PaO2 kleiner oder gleich 55 mmHg) sind für eine Langzeit-Sauerstofftherapie geeignet, eine Behandlung, die durch den Zugang zu tragbaren Oxygenatoren erleichtert wird. Augmentationstherapie mit alpha1-Antitrypsin kann bei Emphysemen mit bestätigtem Alpha in Betracht gezogen werden1-Antitrypsinmangel (Phänotyp PiZZ). Die Wirkung von Antioxidantien (wie Vitamin E und C) auf das Fortschreiten des Emphysems wird derzeit untersucht.
abwehr
Die COPD-Prävention sollte mit Anti-Raucher-Kampagnen beginnen, die sich sowohl an die allgemeine Bevölkerung als auch an gefährdete Berufsgruppen richten. Im beruflichen Umfeld sind die Kontrolle und Vermeidung von Expositionen gegenüber Reizstoffen der Atemwege von wesentlicher Bedeutung und haben immer Priorität. Diese Aktivitäten sollten auf eine wirksame Reduzierung der Luftverschmutzung auf sichere Werte abzielen, die normalerweise durch sogenannte zulässige Expositionswerte definiert werden. Da die Anzahl der Luftschadstoffe nicht oder nicht ausreichend reguliert ist, sind alle Anstrengungen zur Reduzierung der Belastung gerechtfertigt. In Fällen, in denen eine solche Reduzierung nicht erreicht werden kann, ist ein persönlicher Atemschutz erforderlich, um das Risiko einer individuellen Exposition gegenüber schädlichen Stoffen zu verringern.
Die medizinische Prävention von COPD im beruflichen Umfeld umfasst zwei wichtige Schritte: ein Programm zur Überwachung der Atemwegsgesundheit und ein Schulungsprogramm für Mitarbeiter.
Das Programm zur Überwachung der Atemwegsgesundheit umfasst eine regelmäßige Bewertung der Gesundheit der Atemwege; Sie beginnt mit der Eingangsbeurteilung (Anamnese, körperliche Untersuchung, Röntgen-Thorax und Standard-Lungenfunktionstest) und wird während der Beschäftigungsdauer regelmäßig durchgeführt. Das Programm soll die grundlegende Atemgesundheit von Arbeitern vor Beginn der Arbeit beurteilen (und Arbeiter mit subjektiver und/oder objektiver Atemwegsbeeinträchtigung identifizieren) und während der laufenden Überwachung der Arbeiter frühe Anzeichen einer Atemwegsbeeinträchtigung erkennen. Arbeiter mit positiven Befunden sollten von der Exposition abgezogen und zur weiteren diagnostischen Abklärung überwiesen werden.
Das Mitarbeiterschulungsprogramm sollte auf der zuverlässigen Erkennung von Atemwegsgefahren in der Arbeitsumgebung basieren und von Gesundheitsexperten, Arbeitshygienikern, Sicherheitsingenieuren und dem Management konzipiert werden. Das Programm sollte Arbeitnehmer mit angemessenen Informationen über Gefahren für die Atemwege am Arbeitsplatz, mögliche Auswirkungen der Exposition auf die Atemwege und einschlägige Vorschriften versorgen. Es sollte auch die Förderung sicherer Arbeitspraktiken und einer gesunden Lebensweise beinhalten.
Atmungssystem: Die Vielfalt der Pneumokoniosen
Dieser Artikel widmet sich einer Erörterung von Pneumokoniosen im Zusammenhang mit einer Vielzahl spezifischer nicht-faseriger Substanzen; Expositionen gegenüber diesen Stäuben werden an anderer Stelle in diesem Band nicht behandelt. Für jedes Material, das bei Exposition eine Pneumokoniose hervorrufen kann, folgt eine kurze Erörterung der Mineralogie und kommerziellen Bedeutung, gefolgt von Informationen zur Lungengesundheit von exponierten Arbeitern.
Aluminium
Aluminium ist ein Leichtmetall mit vielen kommerziellen Anwendungen sowohl im metallischen als auch im kombinierten Zustand. (Abramson et al. 1989; Kilburn und Warshaw 1992; Kongerud et al. 1994.) Aluminiumhaltige Erze, hauptsächlich Bauxit und Kryolith, bestehen aus Verbindungen des Metalls mit Sauerstoff, Fluor und Eisen. Eine Verunreinigung der Erze mit Kieselsäure ist üblich. Aluminiumoxid (Al2O3) wird aus Bauxit gewonnen und kann zur Verwendung als Schleifmittel oder als Katalysator verarbeitet werden. Metallisches Aluminium wird aus Tonerde durch elektrolytische Reduktion in Gegenwart von Fluorid gewonnen. Die Elektrolyse der Mischung wird unter Verwendung von Kohleelektroden bei einer Temperatur von etwa 1,000 °C in als Töpfe bekannten Zellen durchgeführt. Das metallische Aluminium wird dann zum Gießen abgezogen. Die Staub-, Rauch- und Gasexposition in Topfräumen, einschließlich Kohlenstoff, Aluminiumoxid, Fluoride, Schwefeldioxid, Kohlenmonoxid und aromatische Kohlenwasserstoffe, wird während des Krustenbrechens und anderer Wartungsarbeiten verstärkt. Zahlreiche Produkte werden aus Aluminiumplatten, -flocken, -granulaten und -gussstücken hergestellt, was zu einem umfangreichen Potenzial für berufliche Expositionen führt. Metallisches Aluminium und seine Legierungen finden Verwendung in der Flugzeug-, Boots- und Automobilindustrie, bei der Herstellung von Behältern und von elektrischen und mechanischen Geräten sowie in einer Vielzahl von Konstruktions- und Konstruktionsanwendungen. Kleine Aluminiumpartikel werden in Farben, Sprengstoffen und Brandsätzen verwendet. Zur Aufrechterhaltung der Partikeltrennung werden Mineralöle oder Stearin zugesetzt; Eine erhöhte Lungentoxizität von Aluminiumflocken wurde mit der Verwendung von Mineralöl in Verbindung gebracht.
Lungengesundheit
Das Einatmen von aluminiumhaltigen Stäuben und Dämpfen kann bei Arbeitern auftreten, die an der Gewinnung, Gewinnung, Verarbeitung, Herstellung und Endverwendung von aluminiumhaltigen Materialien beteiligt sind. Lungenfibrose, die zu Symptomen und Röntgenbefunden führte, wurde bei Arbeitern mit mehreren unterschiedlichen Expositionen gegenüber aluminiumhaltigen Stoffen beschrieben. Die Shaver-Krankheit ist eine schwere Pneumokoniose, die bei Arbeitern beschrieben wird, die an der Herstellung von Schleifmitteln aus Aluminiumoxid beteiligt sind. Eine Reihe von Todesfällen aufgrund der Erkrankung wurde gemeldet. Am häufigsten sind die oberen Lungenlappen betroffen und das Auftreten eines Pneumothorax ist eine häufige Komplikation. Bei der Autopsie wurden hohe Konzentrationen von Siliziumdioxid in der Topfraumumgebung sowie in den Lungen von Arbeitern gefunden, was darauf hindeutet, dass Siliziumdioxid möglicherweise zum klinischen Bild der Shaver-Krankheit beiträgt. Es wurden auch hohe Konzentrationen von Aluminiumoxidpartikeln beobachtet. Die Lungenpathologie kann Blasen und Bullae zeigen, und gelegentlich wird eine Pleuraverdickung gesehen. Die Fibrose ist diffus, mit Entzündungsbereichen in der Lunge und den zugehörigen Lymphknoten.
Aluminiumpulver werden zur Herstellung von Sprengstoffen verwendet, und es gibt eine Reihe von Berichten über eine schwere und fortschreitende Fibrose bei Arbeitern, die an diesem Verfahren beteiligt sind. Eine Lungenbeteiligung wurde gelegentlich auch bei Arbeitern beschrieben, die beim Schweißen oder Polieren von Aluminium und beim Einsacken von Katzenstreu mit Aluminiumsilikat (Alunit) beschäftigt waren. Es gab jedoch erhebliche Unterschiede bei der Meldung von Lungenerkrankungen in Bezug auf Expositionen gegenüber Aluminium. Epidemiologische Studien an Arbeitern, die einer Aluminiumreduktion ausgesetzt waren, haben im Allgemeinen eine geringe Prävalenz von pneumokoniotischen Veränderungen und eine leichte mittlere Verringerung der Lungenfunktion gezeigt. In verschiedenen Arbeitsumgebungen können Aluminiumoxidverbindungen in mehreren Formen vorkommen, und in Tierversuchen scheinen diese Formen unterschiedliche Lungentoxizitäten aufzuweisen. Kieselsäure und andere gemischte Stäube können ebenfalls zu dieser unterschiedlichen Toxizität beitragen, ebenso wie die Materialien, die zum Beschichten der Aluminiumpartikel verwendet werden. Ein Arbeiter, der nach Exposition gegenüber Oxiden und metallischem Aluminium eine granulomatöse Lungenerkrankung entwickelte, zeigte eine Transformation seiner Blutlymphozyten nach Exposition gegenüber Aluminiumsalzen, was darauf hindeutet, dass immunologische Faktoren eine Rolle spielen könnten.
Ein asthmatisches Syndrom wurde häufig bei Arbeitern festgestellt, die Dämpfen in Räumen zur Aluminiumreduktion ausgesetzt waren. Fluoride, die in der Potroom-Umgebung gefunden wurden, wurden damit in Verbindung gebracht, obwohl das spezifische Mittel oder die spezifischen Mittel, die mit dem asthmatischen Syndrom assoziiert sind, nicht bestimmt wurden. Wie bei anderen berufsbedingten Asthmaerkrankungen treten die Symptome oft 4 bis 12 Stunden nach der Exposition auf und umfassen Husten, Dyspnoe, Engegefühl in der Brust und Keuchen. Es kann auch eine sofortige Reaktion festgestellt werden. Atopie und Asthma in der Familie scheinen keine Risikofaktoren für die Entwicklung von Potroom-Asthma zu sein. Nach Beendigung der Exposition kann davon ausgegangen werden, dass die Symptome in den meisten Fällen verschwinden, obwohl zwei Drittel der betroffenen Arbeiter eine anhaltende unspezifische bronchiale Reaktion zeigen und bei einigen Arbeitern die Symptome und die Hyperreaktivität der Atemwege noch Jahre nach Beendigung der Exposition anhalten. Die Prognose für Pot-Room-Asthma scheint bei denjenigen am besten zu sein, die sofort von der Exposition entfernt werden, wenn sich die asthmatischen Symptome manifestieren. Behobene Luftstrombehinderungen wurden auch mit Topfraumarbeiten in Verbindung gebracht.
Kohlenstoffelektroden werden im Aluminiumreduktionsprozess verwendet, und in der Potroom-Umgebung wurden bekannte menschliche Karzinogene identifiziert. Mehrere Sterblichkeitsstudien haben Lungenkrebsexzesse unter exponierten Arbeitern in dieser Branche aufgedeckt.
Kieselgur
Ablagerungen von Diatomeenerde resultieren aus der Akkretion von Skeletten mikroskopisch kleiner Organismen. (Cooper und Jacobson 1977; Checkoway et al. 1993.) Diatomeenerde kann in Gießereien und bei der Wartung von Filtern, Schleifmitteln, Schmiermitteln und Sprengstoffen verwendet werden. Bestimmte Ablagerungen enthalten bis zu 90 % freies Siliziumdioxid. Exponierte Arbeiter können Lungenveränderungen mit einfacher oder komplizierter Pneumokoniose entwickeln. Das Todesrisiko sowohl durch gutartige Atemwegserkrankungen als auch durch Lungenkrebs wurde mit der Beschäftigung der Arbeiter in staubiger Arbeit sowie mit der kumulativen Exposition gegenüber kristallinem Siliziumdioxid während des Abbaus und der Verarbeitung von Diatomeenerde in Verbindung gebracht.
Elementarer Kohlenstoff
Abgesehen von Kohle sind die beiden üblichen Formen von elementarem Kohlenstoff Graphit (kristalliner Kohlenstoff) und Ruß. (Hanoa 1983; Petsonk et al. 1988.) Graphit wird zur Herstellung von Bleistiften, Gießereiauskleidungen, Farben, Elektroden, Trockenbatterien und Tiegeln für metallurgische Zwecke verwendet. Fein gemahlener Graphit hat Schmiereigenschaften. Ruß ist eine teilweise zersetzte Form, die in Autoreifen, Pigmenten, Kunststoffen, Tinten und anderen Produkten verwendet wird. Ruß wird aus fossilen Brennstoffen durch eine Vielzahl von Prozessen hergestellt, die teilweise Verbrennung und thermische Zersetzung umfassen.
Beim Abbau und Mahlen von natürlichem Graphit sowie bei der Herstellung von künstlichem Graphit kann es zum Einatmen von Kohlenstoff und damit verbundenen Stäuben kommen. Künstlicher Graphit wird durch das Erhitzen von Kohle oder Petrolkoks hergestellt und enthält im Allgemeinen keine freie Kieselsäure.
Lungengesundheit
Pneumokoniose resultiert aus der Exposition von Arbeitern sowohl gegenüber natürlichem als auch künstlichem Graphit. Klinisch zeigen Arbeiter mit Kohlenstoff- oder Graphitpneumokoniose ähnliche radiologische Befunde wie Kohlearbeiter. In der Vergangenheit wurden schwere symptomatische Fälle mit massiver Lungenfibrose gemeldet, insbesondere im Zusammenhang mit der Herstellung von Kohlenstoffelektroden für die Metallurgie, obwohl neuere Berichte betonen, dass die Materialien, die an Expositionen beteiligt sind, die zu dieser Art von Krankheit führen, wahrscheinlich gemischte Stäube sind.
Gilsonit
Gilsonit, auch Uintait genannt, ist ein verfestigter Kohlenwasserstoff. (Keimig et al. 1987.) Es kommt in Venen im Westen der Vereinigten Staaten vor. Gegenwärtige Verwendungen umfassen die Herstellung von Nahtabdichtungen, Tinten, Farben und Lacken für Automobilkarosserien. Es ist ein Bestandteil von Ölbohrflüssigkeiten und Zementen; es ist ein Additiv in Sandformen in der Gießereiindustrie; es ist als Bestandteil von Asphalt, Bauplatten und Sprengstoffen zu finden; und es wird bei der Herstellung von Graphit in Nuklearqualität eingesetzt. Arbeiter, die Gilsonit-Staub ausgesetzt waren, haben Symptome von Husten und Schleimproduktion gemeldet. Fünf von neunundneunzig befragten Arbeitern zeigten röntgenologische Anzeichen einer Pneumokoniose. Es wurden keine Anomalien der Lungenfunktion in Bezug auf Exposition gegenüber Gilsonit-Staub festgestellt.
Gips
Gips ist hydratisiertes Calciumsulfat (CaSO4· 2H2O) (Oakes et al. 1982). Es wird als Bestandteil von Gipskartonplatten, Gips und Portlandzement verwendet. Ablagerungen werden in verschiedenen Formen gefunden und sind oft mit anderen Mineralien wie Quarz verbunden. Pneumokoniose wurde bei Gipsminenarbeitern beobachtet und auf eine Verunreinigung mit Kieselsäure zurückgeführt. Atmungsstörungen wurden nicht mit Gipsstaubexpositionen in Verbindung gebracht.
Öle und Schmierstoffe
Kohlenwasserstoffhaltige Flüssigkeiten werden als Kühl-, Schneid- und Schmiermittel verwendet (Cullen et al. 1981). Pflanzenöle sind in einigen kommerziellen Produkten und in einer Vielzahl von Lebensmitteln enthalten. Diese Öle können zerstäubt und eingeatmet werden, wenn mit Ölen beschichtete Metalle gefräst oder bearbeitet werden oder wenn ölhaltige Sprays zum Zweck der Reinigung oder Schmierung verwendet werden. Umgebungsmessungen in Maschinenhallen und Fabriken haben Ölwerte in der Luft von bis zu 9 mg/m dokumentiert3. Ein Bericht implizierte die Exposition gegenüber Öl in der Luft durch das Verbrennen von tierischen und pflanzlichen Fetten in einem geschlossenen Gebäude.
Lungengesundheit
Bei Arbeitern, die diesen Aerosolen ausgesetzt waren, wurde gelegentlich berichtet, dass sie Anzeichen von a Lipoid-Pneumonie, ähnlich wie bei Patienten, die Mineralöl-Nasentropfen oder andere ölige Materialien aspiriert haben. Der Zustand ist mit Symptomen von Husten und Dyspnoe, inspiratorischem Lungenknacken und Beeinträchtigungen der Lungenfunktion verbunden, die im Allgemeinen leicht ausgeprägt sind. Es wurden einige Fälle mit ausgedehnteren röntgenologischen Veränderungen und schweren Lungenfunktionsstörungen berichtet. Die Exposition gegenüber Mineralölen wurde in mehreren Studien auch mit einem erhöhten Risiko für Atemwegskrebs in Verbindung gebracht.
Portland-Zement
Portlandzement wird aus hydratisierten Calciumsilikaten, Aluminiumoxid, Magnesiumoxid, Eisenoxid, Calciumsulfat, Ton, Schiefer und Sand hergestellt (Abrons et al. 1988; Yan et al. 1993). Die Mischung wird zerkleinert und bei hohen Temperaturen unter Zugabe von Gips kalziniert. Zement findet zahlreiche Anwendungen im Straßen- und Hochbau.
Lungengesundheit
Silikose scheint das größte Risiko bei Zementarbeitern zu sein, gefolgt von einer Mischstaubpneumokoniose. (In der Vergangenheit wurde Zement Asbest zugesetzt, um seine Eigenschaften zu verbessern.) Abnormale Röntgenbefunde des Brustkorbs, einschließlich kleiner runder und unregelmäßiger Trübungen und Pleuraveränderungen, wurden festgestellt. Bei Arbeitern wurde gelegentlich berichtet, dass sie nach Einatmen von Zementstaub eine pulmonale alveoläre Proteinose entwickelt haben. Luftstrombehindernde Veränderungen wurden in einigen, aber nicht allen Umfragen unter Zementarbeitern festgestellt.
Seltenerdmetalle
Seltenerdmetalle oder „Lanthanide“ haben Ordnungszahlen zwischen 57 und 71. Lanthan (Ordnungszahl 57), Cer (58) und Neodym (60) sind die häufigsten der Gruppe. Die anderen Elemente in dieser Gruppe umfassen Praseodym (59), Promethium (61), Samarium (62), Europium (63), Gadolinium (64), Terbium (65), Dysprosium (66), Holmium (67), Erbium (68). ), Thulium (69), Ytterbium (70) und Lutetium (71). (Hussain, Dick und Kaplan 1980; Sabbioni, Pietra und Gaglione 1982; Vocaturo, Colombo und Zanoni 1983; Sulotto, Romano und Berra 1986; Waring und Watling 1990; Deng et al. 1991.) Die Elemente der Seltenen Erden kommen natürlicherweise in Monazit vor Sand, aus dem sie gewonnen werden. Sie werden in einer Vielzahl von legierten Metallen, als Schleifmittel zum Polieren von Spiegeln und Linsen, für Hochtemperaturkeramik, in Feuerwerkskörpern und in Feuersteinen für Zigarettenanzünder verwendet. In der Elektronikindustrie werden sie beim Elektroschweißen verwendet und sind in verschiedenen elektronischen Komponenten zu finden, darunter Fernsehleuchtstoffe, Röntgenschirme, Laser, Mikrowellengeräte, Isolatoren, Kondensatoren und Halbleiter.
Kohlebogenlampen werden häufig in der Druck-, Fotogravur- und Lithografieindustrie verwendet und wurden vor der breiten Einführung von Argon- und Xenonlampen für Flutlicht, Scheinwerfer und Filmprojektion verwendet. Die Seltenerdmetalloxide wurden in den zentralen Kern von Kohlelichtbogenstäben eingebaut, wo sie den Lichtbogenstrom stabilisieren. Dämpfe, die von den Lampen emittiert werden, sind eine Mischung aus gasförmigem und partikelförmigem Material, das zu etwa 65 % aus Seltenerdoxiden, zu 10 % aus Fluoriden und unverbranntem Kohlenstoff und Verunreinigungen besteht.
Lungengesundheit
Pneumokoniose bei Arbeitern, die seltenen Erden ausgesetzt waren, wurde hauptsächlich als bilaterale knötchenförmige röntgenologische Infiltrate des Brustkorbs nachgewiesen. Die Lungenpathologie bei Seltenerd-Pneumokoniosen wurde als interstitielle Fibrose beschrieben, die von einer Ansammlung feinkörniger Staubpartikel oder granulomatösen Veränderungen begleitet wird.
Es wurden unterschiedliche Lungenfunktionsstörungen beschrieben, von restriktiv bis gemischt restriktiv-obstruktiv. Das Spektrum der Lungenerkrankungen im Zusammenhang mit der Inhalation von Seltenerdelementen ist jedoch noch nicht definiert, und Daten über Krankheitsbild und -verlauf sowie histologische Veränderungen liegen primär nur aus wenigen Fallberichten vor.
Ein neoplastisches Potenzial der Seltenerd-Isotope wurde durch einen Fallbericht über Lungenkrebs nahegelegt, der möglicherweise mit ionisierender Strahlung von den natürlich vorkommenden Seltenerd-Radioisotopen zusammenhängt.
Sedimentäre Verbindungen
Sedimentgesteinsablagerungen entstehen durch physikalische und chemische Verwitterung, Erosion, Transport, Ablagerung und Diagenese. Diese können in zwei große Klassen eingeteilt werden: Klastik, die mechanisch abgelagerten Erosionsschutt umfassen, und chemische Niederschläge, zu denen Karbonate, Schalen organischer Skelette und Salzablagerungen gehören. Sedimentäre Karbonate, Sulfate und Halogenide liefern relativ reine Mineralien, die aus konzentrierten Lösungen kristallisiert sind. Aufgrund der hohen Löslichkeit vieler Sedimentverbindungen werden sie schnell aus der Lunge entfernt und sind im Allgemeinen mit geringer Lungenpathologie verbunden. Im Gegensatz dazu zeigten Arbeiter, die bestimmten Sedimentverbindungen, hauptsächlich Klastika, ausgesetzt waren, pneumokoniotische Veränderungen.
Phosphate
Phosphaterz, Ca5(F,Cl)(PO4)3, wird bei der Herstellung von Düngemitteln, Nahrungsergänzungsmitteln, Zahnpasta, Konservierungsmitteln, Waschmitteln, Pestiziden, Nagetiergiften und Munition verwendet (Dutton et al. 1993). Die Gewinnung und Verarbeitung des Erzes kann zu einer Vielzahl von Reizbelastungen führen. Umfragen unter Arbeitern im Phosphatbergbau und -abbau haben vermehrte Symptome von Husten und Schleimproduktion sowie röntgenologische Hinweise auf eine Pneumokoniose, aber wenig Hinweise auf eine abnormale Lungenfunktion dokumentiert.
Schiefer
Schiefer ist eine Mischung aus organischem Material, das hauptsächlich aus Kohlenstoff, Wasserstoff, Sauerstoff, Schwefel und Stickstoff besteht (Rom, Lee und Craft 1981; Seaton et al. 1981). Die mineralische Komponente (Kerogen) befindet sich im Sedimentgestein namens Mergelstein, das eine graubraune Farbe und eine geschichtete Konsistenz hat. Ölschiefer wird seit den 1850er Jahren in Schottland als Energiequelle genutzt. Größere Vorkommen gibt es in den Vereinigten Staaten, Schottland und Estland. Staub in der Atmosphäre von unterirdischen Ölschieferminen ist relativ fein verteilt, wobei bis zu 80 % der Staubpartikel kleiner als 2 mm sind.
Lungengesundheit
Pneumokoniose im Zusammenhang mit der Ablagerung von Schieferstaub in der Lunge wird als Pneumokoniose bezeichnet Schalose. Der Staub erzeugt eine granulomatöse und fibrotische Reaktion in der Lunge. Diese Pneumokoniose ähnelt klinisch der Pneumokoniose und Silikose von Kohlenarbeitern und kann sich zu einer massiven Fibrose entwickeln, selbst nachdem der Arbeiter die Industrie verlassen hat.
Pathologische Veränderungen, die in Lungen mit Shalose identifiziert wurden, sind durch vaskuläre und bronchiale Deformation mit unregelmäßiger Verdickung der interalveolären und interlobulären Septen gekennzeichnet. Zusätzlich zur interstitiellen Fibrose haben Lungenproben mit Schieferpneumokoniose vergrößerte Hilusschatten gezeigt, die mit dem Transport von Schieferstaub und der anschließenden Entwicklung gut definierter sklerotischer Veränderungen in den Hiluslymphknoten zusammenhängen.
Es wurde festgestellt, dass Schieferarbeiter eine Prävalenz von chronischer Bronchitis haben, die zweieinhalb Mal höher ist als bei gleichaltrigen Kontrollpersonen. Die Wirkung von Schieferstaubbelastungen auf die Lungenfunktion wurde nicht systematisch untersucht.
Schiefer
Schiefer ist ein metamorphes Gestein, das aus verschiedenen Mineralien, Tonen und kohlenstoffhaltigen Stoffen besteht (McDermott et al. 1978). Zu den Hauptbestandteilen von Schiefer gehören Muskovit, Chlorit, Calcit und Quarz sowie Graphit, Magnetit und Rutil. Diese haben eine Metamorphose durchlaufen, um ein dichtes kristallines Gestein zu bilden, das Festigkeit besitzt, aber leicht zu spalten ist, Eigenschaften, die seine wirtschaftliche Bedeutung erklären. Schiefer wird in Bedachungen, Natursteinen, Bodenfliesen, Fliesen, Baukörpern wie Paneelen und Fensterbänken, Tafeln, Bleistiften, Billardtischen und Labortischplatten verwendet. Brechschiefer wird im Straßenbau, Tennisplatzbelägen und leichten Dachgranulaten eingesetzt.
Lungengesundheit
Pneumokoniose wurde bei einem Drittel der untersuchten Arbeiter in der Schieferindustrie in Nordwales und bei 54 % der Hersteller von Schieferstiften in Indien festgestellt. Bei Schieferarbeitern wurden verschiedene röntgenologische Veränderungen der Lunge festgestellt. Aufgrund des hohen Quarzgehaltes einiger Tonschiefer und der angrenzenden Gesteinsschichten kann die Schiefer-Pneumokoniose Merkmale einer Silikose aufweisen. Die Prävalenz von Atemwegssymptomen bei Schieferarbeitern ist hoch, und der Anteil der Arbeiter mit Symptomen steigt mit der Pneumokoniose-Kategorie, unabhängig vom Raucherstatus. Verringerte Werte des forcierten Exspirationsvolumens in einer Sekunde (FEV1) und forcierte Vitalkapazität (FVC) sind mit zunehmender Pneumokoniose-Kategorie verbunden.
Die Lungen von Bergleuten, die Schieferstaub ausgesetzt waren, zeigen lokalisierte Bereiche perivaskulärer und peribronchialer Fibrose, die sich bis zur Makulabildung und ausgedehnter interstitieller Fibrose erstrecken. Typische Läsionen sind fibrotische Flecken unterschiedlicher Konfiguration, die eng mit kleinen Lungenblutgefäßen verbunden sind.
Talk
Talk besteht aus Magnesiumsilikaten und kommt in einer Vielzahl von Formen vor. (Vallyathan und Craighead 1981; Wegman et al. 1982; Stille und Tabershaw 1982; Wergeland, Andersen und Baerheim 1990; Gibbs, Pooley und Griffith 1992.)
Talkablagerungen sind häufig mit anderen Mineralien verunreinigt, einschließlich sowohl faserigem als auch nicht faserigem Tremolit und Quarz. Auswirkungen auf die Lungengesundheit von Arbeitern, die Talk ausgesetzt sind, können sowohl mit dem Talk selbst als auch mit den anderen assoziierten Mineralien zusammenhängen.
Die Talkproduktion findet hauptsächlich in Australien, Österreich, China, Frankreich und den Vereinigten Staaten statt. Talk wird als Komponente in Hunderten von Produkten verwendet und wird bei der Herstellung von Farben, Pharmazeutika, Kosmetika, Keramik, Autoreifen und Papier verwendet.
Lungengesundheit
Diffuse abgerundete und unregelmäßige parenchymale Lungentrübungen und pleurale Anomalien sind auf Röntgenaufnahmen des Brustkorbs von Talkarbeitern in Verbindung mit der Talkexposition zu sehen. Abhängig von den erfahrenen spezifischen Expositionen können die Röntgenschatten dem Talk selbst oder Verunreinigungen im Talk zugeschrieben werden. Die Exposition gegenüber Talk wurde in Lungenfunktionsstudien mit Symptomen von Husten, Dyspnoe und Schleimproduktion sowie mit Hinweisen auf eine Obstruktion des Luftstroms in Verbindung gebracht. Die Lungenpathologie hat verschiedene Formen der Lungenfibrose aufgedeckt: granulomatöse Veränderungen und eisenhaltige Körper wurden berichtet, und staubbeladene Makrophagen, die sich um die respiratorischen Bronchiolen angesammelt haben, vermischt mit Kollagenbündeln. Die mineralogische Untersuchung von Lungengewebe von Talkarbeitern ist ebenfalls variabel und kann Silica, Glimmer oder gemischte Silikate zeigen.
Da Talkablagerungen mit Asbest und anderen Fasern assoziiert sein können, ist es nicht verwunderlich, dass bei Talkminenarbeitern und Müllern über ein erhöhtes Risiko für Bronchialkarzinome berichtet wurde. Jüngste Untersuchungen von Arbeitern, die Talk ohne assoziierte Asbestfasern ausgesetzt waren, zeigten Trends für eine höhere Sterblichkeit durch nicht bösartige Atemwegserkrankungen (Silikose, Silico-Tuberkulose, Emphysem und Pneumonie), aber das Risiko für Bronchialkrebs wurde nicht als erhöht festgestellt.
Hairspray
Die Exposition gegenüber Haarsprays erfolgt sowohl im häuslichen Umfeld als auch in gewerblichen Friseurbetrieben (Rom 1992b). Umweltmessungen in Schönheitssalons haben das Potenzial für lungengängige Aerosolbelastungen aufgezeigt. Mehrere Fallberichte haben die Exposition gegenüber Haarspray mit dem Auftreten einer Pneumonitis in Verbindung gebracht. Thesaurose, bei stark exponierten Personen. Die klinischen Symptome waren in den Fällen im Allgemeinen mild und verschwanden mit Beendigung der Exposition. Die Histologie zeigte normalerweise einen granulomatösen Prozess in der Lunge und vergrößerte Hilus-Lymphknoten mit einer Verdickung der Alveolarwände und zahlreichen granulären Makrophagen in den Lufträumen. Makromoleküle in Haarsprays, darunter Schellacke und Polyvinylpyrrolidon, wurden als potentielle Wirkstoffe vorgeschlagen. Im Gegensatz zu den klinischen Fallberichten wurden bei radiologischen Untersuchungen von gewerblichen Friseuren beobachtete erhöhte Lungenparenchym-Röntgenschatten nicht schlüssig mit der Haarspray-Exposition in Verbindung gebracht. Obwohl die Ergebnisse dieser Studien keine endgültigen Schlussfolgerungen zulassen, scheint eine klinisch bedeutsame Lungenerkrankung durch typische Haarspray-Exposition ein ungewöhnliches Ereignis zu sein.
Hartmetallkrankheit
Kurz nach dem Ende des Ersten Weltkriegs, während er nach einem Material suchte, das Diamant in Metallziehdüsen ersetzen könnte, patentierte Karl Schoeter in Berlin ein Sinterverfahren (Druckbeaufschlagung plus Erhitzen auf 1,500 °C) einer Mischung aus feinem Wolfram Hartmetallpulver (WC) mit 10 % Kobalt zur Herstellung von „Hartmetall“. Die Hauptmerkmale dieses Sinters sind die extreme Härte, die der von Diamant nur geringfügig unterlegen ist, und die Beibehaltung seiner mechanischen Eigenschaften bei hohen Temperaturen; Diese Eigenschaften machen es geeignet zum Ziehen von Metall, für geschweißte Einsätze und für Hochgeschwindigkeitswerkzeuge zur Bearbeitung von Metallen, Stein, Holz und Materialien mit hoher Verschleiß- oder Hitzebeständigkeit in den Bereichen Mechanik, Luftfahrt und Ballistik. Die Verwendung von Hartmetall nimmt weltweit kontinuierlich zu. 1927 dehnte Krupp die Verwendung von Hartmetall auf den Bereich der Schneidwerkzeuge aus und nannte es „Widia“ (wie Diamant—wie Diamant), ein Name, der heute noch verwendet wird.
Das Sintern bleibt die Grundlage aller Hartmetallherstellung: Die Techniken werden durch die Einführung anderer Metallkarbide – Titankarbid (TiC) und Tantalkarbid (TaC) – und durch die Behandlung von Hartmetallteilen für mobile Schneideinsätze mit einer oder mehreren Schichten von verbessert Titannitrid oder Aluminiumoxid und andere sehr harte Verbindungen, die durch chemische Gasphasenabscheidung (CVD) oder physikalische Gasphasenabscheidung (PVD) aufgebracht werden. Die mit den Werkzeugen verschweißten festen Einsätze können nicht galvanisiert werden, sondern werden durch eine Diamantschleifscheibe immer wieder geschärft (Bilder 1 und 2).
Abbildung 1. (A) Beispiele einiger beweglicher Einsätze aus Hartmetall, die mit goldgelbem Wolframnitrid plattiert sind; (B) Einsatz an das Werkzeug geschweißt und in Stahlzeichnung bearbeitet.
Abbildung 2. Feste Einsätze, die an (A) Steinbohrer und (B) Sägeblatt geschweißt sind.
Der Hartmetallsinter wird durch Teilchen aus metallischen Carbiden gebildet, die in eine aus Kobalt gebildete Matrix eingebaut sind, die während des Sinterns schmilzt, wechselwirkt und die Zwischenräume einnimmt. Kobalt ist somit der Strukturklebstoff, der metallkeramische Eigenschaften annimmt (Bilder 3, 4 und 5).
Abbildung 3. Mikrostruktur einer WC/Co-Sinterung; WC-Partikel werden in die Co-Lichtmatrix eingebaut (1,500x).
Abbildung 4. Mikrostruktur einer WC + TiC + TaC + Co-Sinterung. Zusammen mit prismatischen WC-Partikeln werden kugelförmige Partikel beobachtet, die durch eine feste Lösung von TiC + TaC gebildet werden. Die Lichtmatrix wird durch Co (1,500x) gebildet.
Abbildung 5. Sintermikrostruktur, plattiert mit mehreren sehr harten Schichten (2,000x).
Der Sinterprozess verwendet sehr feine Metallkarbidpulver (durchschnittlicher Durchmesser von 1 bis 9 μm) und Kobaltpulver (durchschnittlicher Durchmesser von 1 bis 4 μm), die gemischt, mit Paraffinlösung behandelt, formgepresst, bei niedriger Temperatur entwachst, vorbehandelt gesintert bei 700 bis 750°C und gesintert bei 1,500°C (Brookes 1992).
Wenn das Sintern mit unangemessenen Methoden, unsachgemäßen Techniken und schlechter Industriehygiene durchgeführt wird, können die Pulver die Atmosphäre der Arbeitsumgebung verschmutzen: Arbeiter sind daher dem Risiko ausgesetzt, Metallkarbidpulver und Kobaltpulver einzuatmen. Neben dem primären Prozess gibt es andere Tätigkeiten, die die Arbeiter dem Risiko einer Aerosol-Inhalation von Hartmetall aussetzen können. Das Schärfen von festen Einsätzen, die mit Werkzeugen verschweißt sind, wird normalerweise durch Diamanttrockenschleifen oder häufiger durch Kühlen mit Flüssigkeiten unterschiedlicher Art durchgeführt, wodurch Pulver oder Nebel entstehen, die aus sehr kleinen Tropfen bestehen, die Metallpartikel enthalten. Hartmetallpartikel werden auch zur Herstellung einer hochbeständigen Schicht auf verschleißbeanspruchten Stahloberflächen verwendet, die durch Verfahren (Plasmabeschichtungsverfahren und andere) aufgebracht werden, die auf der Kombination eines Pulversprühens mit einem elektrischen Lichtbogen oder einer kontrollierten Explosion von basieren ein Gasgemisch bei hoher Temperatur. Der Lichtbogen oder die explosionsartige Strömung des Gases bestimmen das Aufschmelzen der metallischen Partikel und deren Aufprall auf die zu beschichtende Oberfläche.
Erste Beobachtungen zu „Hartmetallkrankheiten“ wurden in Deutschland in den 1940er Jahren beschrieben. Sie berichteten von einer diffusen, fortschreitenden Lungenfibrose, genannt Hartmetallungenfibrose. In den nächsten 20 Jahren wurden in allen Industrieländern parallele Fälle beobachtet und beschrieben. Die betroffenen Arbeiter waren in den meisten Fällen mit dem Sintern beauftragt. Von 1970 bis heute deuten mehrere Studien darauf hin, dass die Pathologie des Atemgeräts durch das Einatmen von Hartmetallpartikeln verursacht wird. Es betrifft nur anfällige Personen und besteht aus den folgenden Symptomen:
- akuten: Schnupfen, Asthma
- subakut: fibrosierende Alveolitis
- chronisch: diffuse und fortschreitende interstitielle Fibrose.
Betroffen sind nicht nur Sinterarbeiter, sondern jeder, der Aerosole mit Hartmetall und insbesondere Kobalt einatmet. Es wird hauptsächlich und vielleicht ausschließlich durch Kobalt verursacht.
Die Definition der Hartmetallerkrankung umfasst nun eine Gruppe von Pathologien des Atemapparats, die sich in klinischer Schwere und Prognose voneinander unterscheiden, aber eine variable individuelle Reaktivität auf den ätiologischen Faktor Kobalt gemeinsam haben.
Neuere epidemiologische und experimentelle Erkenntnisse stimmen in der ursächlichen Rolle von Cobalt für akute Beschwerden in den oberen Atemwegen (Rhinitis, Asthma) sowie für subakute und chronische Beschwerden im Bronchialparenchym (fibrosierende Alveolitis und chronische interstitielle Fibrose) überein.
Der pathogene Mechanismus beruht auf der Induktion einer überempfindlichen Immunreaktion durch Co: Tatsächlich zeigen nur einige der Probanden Pathologien nach kurzer Exposition gegenüber relativ niedriger Konzentration oder sogar nach längerer und intensiverer Exposition. Co-Konzentrationen in biologischen Proben (Blut, Urin, Haut) unterscheiden sich nicht signifikant zwischen denen, die die Pathologie haben, und denen, die dies nicht tun; es gibt keine Korrelation von Dosis und Reaktion auf Gewebeebene; bei Asthmatikern wurden spezifische Antikörper (Immunglobuline IgE und IgG) gegen eine Co-Albumin-Verbindung identifiziert, und der Co-Patch-Test ist bei Personen mit Alveolitis oder Fibrose positiv; die zytologischen Aspekte der riesenzelligen Alveolitis sind mit einer Immunreaktion vereinbar, und akute oder subakute Symptome neigen dazu, zurückzugehen, wenn die Patienten von der Exposition gegenüber Co entfernt werden (Parkes 1994).
Die immunologischen Grundlagen der Co-Überempfindlichkeit sind noch nicht zufriedenstellend geklärt; Es ist daher nicht möglich, einen zuverlässigen Marker für die individuelle Anfälligkeit zu identifizieren.
Identische Pathologien wie bei den Hartmetall-exponierten Probanden wurden auch bei Diamantschleifern beobachtet, die Scheiben aus mit Co zementierten Mikrodiamanten verwenden und daher nur Co und Diamantpartikel einatmen.
Es ist noch nicht vollständig nachgewiesen, dass reines Co (alle anderen inhalierten Partikel ausgenommen) allein in der Lage ist, die Pathologien und vor allem die diffuse interstitielle Fibrose hervorzurufen: Die mit Co inhalierten Partikel könnten eine synergistische sowie modulierende Wirkung haben. Experimentelle Studien scheinen zu zeigen, dass die biologische Reaktivität gegenüber einer Mischung aus Co-Partikeln und Wolfram stärker ist als die, die durch Co allein verursacht wird, und signifikante Pathologien sind bei den Arbeitern, die für die Herstellung von reinem Co-Pulver verantwortlich sind, nicht zu beobachten (Science of Gesamtumwelt 1994).
Klinische Symptome der Hartmetallerkrankung, die nach heutigem ätiopathogenetischen Wissen genauer als „Cobalt-Krankheit“ bezeichnet werden müsste, sind, wie bereits erwähnt, akut, subakut und chronisch.
Zu den akuten Symptomen gehören eine spezifische Reizung der Atemwege (Rhinitis, Laryngotracheitis, Lungenödem), die durch die Exposition gegenüber hohen Konzentrationen von Co-Pulver oder Co-Rauch verursacht wird; sie sind nur in Ausnahmefällen beobachtbar. Asthma wird häufiger beobachtet. Es tritt bei 5 bis 10 % der Arbeiter auf, die gegenüber 0.05 mg Cobalt/m exponiert waren3, dem aktuellen US-Schwellenwert (TLV). Symptome einer Thoraxverengung mit Atemnot und Husten treten eher am Ende der Arbeitsschicht oder in der Nacht auf. Die Diagnose eines berufsbedingten allergischen Asthma bronchiale aufgrund von Kobalt kann aufgrund anamnestischer Kriterien vermutet werden, wird jedoch durch einen spezifischen Bronchialstimulationstest bestätigt, der das Auftreten einer sofortigen, verzögerten oder dualen bronchospastischen Reaktion feststellt. Auch Atemkapazitätstests zu Beginn und am Ende der Arbeitsschicht können bei der Diagnose helfen. Asthmatische Symptome aufgrund von Kobalt verschwinden in der Regel, wenn die Person von der Exposition befreit wird, aber ähnlich wie bei allen anderen Formen von berufsbedingtem allergischem Asthma können die Symptome chronisch und irreversibel werden, wenn die Exposition trotz des Vorhandenseins von Kobalt über einen langen Zeitraum (Jahre) andauert Atemstörungen. Hochgradig bronchoreaktive Personen können nicht-allergische ätiologische asthmatische Symptome zeigen, mit einer unspezifischen Reaktion auf die Inhalation von Kobalt und anderen irritierenden Pulvern. In einem hohen Prozentsatz der Fälle mit allergischem Asthma bronchiale wurde im IgE-Serum eine spezifische Reaktion auf eine humane Co-Seroalbumin-Verbindung gefunden. Der radiologische Befund variiert nicht: Nur in seltenen Fällen finden sich Mischformen von Asthma plus Alveolitis mit radiologischen Veränderungen, die spezifisch durch eine Alveolitis verursacht werden. Die bronchodilatatorische Therapie führt zusammen mit einer sofortigen Beendigung der Arbeitsbelastung zu einer vollständigen Genesung bei Fällen, die erst vor kurzem aufgetreten und noch nicht chronisch sind.
Zu den subakuten und chronischen Symptomen gehören die fibrosierende Alveolitis und die chronisch diffuse und progressive interstitielle Fibrose (DIPF). Die klinische Erfahrung scheint darauf hinzudeuten, dass der Übergang von Alveolitis zu interstitieller Fibrose ein Prozess ist, der sich allmählich und langsam entwickelt: Man kann Fälle von reiner anfänglicher Alveolitis finden, die nach Absetzen der Exposition plus Kortikosteroidtherapie reversibel sind; oder Fälle mit einer bereits vorhandenen Fibrosekomponente, die sich verbessern, aber keine vollständige Genesung erreichen kann, indem das Subjekt aus der Exposition genommen wird, selbst mit zusätzlicher Therapie; und schließlich Fälle, in denen die vorherrschende Situation die eines irreversiblen DIPF ist. Das Auftreten solcher Fälle ist bei den exponierten Arbeitern gering, sehr viel geringer als der Prozentsatz der Fälle von allergischem Asthma.
Alveolitis ist heute in ihren zytologischen Komponenten durch bronchoalveoläre Lavage (BAL) leicht zu untersuchen; sie ist gekennzeichnet durch eine starke Zunahme der Gesamtzellzahl, hauptsächlich gebildet durch Makrophagen, mit zahlreichen mehrkernigen Riesenzellen und dem typischen Erscheinungsbild von Fremdkörper-Riesenzellen, die zeitweise zytoplasmatische Zellen enthalten (Abbildung 6); sogar eine absolute oder relative Zunahme von Lymphozyten ist häufig, mit einem verringerten CD4/CD8-Verhältnis, verbunden mit einer starken Zunahme von Eosinophilen und Mastzellen. Selten ist die Alveolitis hauptsächlich lymphozytär, mit umgekehrtem CD4/CD8-Verhältnis, wie es bei Pneumopathien aufgrund von Überempfindlichkeit auftritt.
Abbildung 6. Zytologische BAL bei einem durch Hartmetall verursachten Fall einer makrophagischen mononukleären Riesenzellalveolitis. Zwischen den mononukleären Makrophagen und dem Lymphozyten wird ein riesiger Fremdkörperzellentyp (400x) beobachtet.
Patienten mit Alveolitis berichten von Dyspnoe in Verbindung mit Müdigkeit, Gewichtsverlust und trockenem Husten. In der unteren Lunge besteht eine Krepitation mit funktioneller Veränderung restriktiver Art und diffuser runder oder unregelmäßiger radiologischer Trübung. Der Epikutantest auf Kobalt ist in den meisten Fällen positiv. Bei anfälligen Personen zeigt sich eine Alveolitis nach einer relativ kurzen Expositionszeit am Arbeitsplatz von einem oder wenigen Jahren. In der Anfangsphase ist diese Form durch einfaches Entfernen aus der Exposition bis zur vollständigen Genesung reversibel, mit besseren Ergebnissen, wenn dies mit einer Kortisontherapie kombiniert wird.
Die Entwicklung einer diffusen interstitiellen Fibrose verschlimmert die klinischen Symptome mit einer Verschlechterung der Dyspnoe, die bereits bei geringer Belastung und dann auch in Ruhe auftritt, mit einer Verschlechterung der restriktiven Atemstörung, die mit einer Verringerung der kapillar-alveolären Diffusion verbunden ist, und mit dem Auftreten von röntgenologischen Trübungen linearen Typs und Wabenbildung (Abbildung 7). Die histologische Situation ist die einer fibrosierenden Alveolitis vom „wandartigen Typ“.
Abbildung 7. Thorax-Röntgenaufnahme eines Patienten, der an durch Hartmetall verursachter interstitieller Fibrose leidet. Lineare und diffuse Opazität und wabenartige Aspekte werden beobachtet.
Die Entwicklung ist schnell fortschreitend; Therapien sind unwirksam und die Prognose zweifelhaft. Einer der vom Autor diagnostizierten Fälle erforderte schließlich eine Lungentransplantation.
Die Berufsdiagnostik basiert auf der Anamnese, dem zytologischen BAL-Muster und dem Cobalt-Patch-Test.
Die Prävention der Hartmetallkrankheit, genauer gesagt der Kobaltkrankheit, ist heute hauptsächlich technischer Art: Schutz der Arbeiter durch die Beseitigung von Pulver, Rauch oder Nebel mit ausreichender Belüftung der Arbeitsbereiche. Tatsächlich macht der Mangel an Wissen über die Faktoren, die die individuelle Überempfindlichkeit gegenüber Kobalt bestimmen, die Identifizierung empfindlicher Personen unmöglich, und es müssen die größtmöglichen Anstrengungen unternommen werden, um die atmosphärischen Konzentrationen zu reduzieren.
Die Zahl der gefährdeten Personen wird unterschätzt, da viele Schleiftätigkeiten in kleinen Industrien oder von Handwerkern durchgeführt werden. An solchen Arbeitsplätzen beträgt der US-TLV 0.05 mg/m3 wird häufig überschritten. Es gibt auch einige Zweifel hinsichtlich der Angemessenheit des TLV zum Schutz von Arbeitnehmern vor einer Kobaltkrankheit, da die Dosis-Wirkungs-Beziehungen für Krankheitsmechanismen, die eine Überempfindlichkeit beinhalten, nicht vollständig verstanden sind.
Die routinemäßige Überwachung muss genau genug sein, um Kobaltpathologien in ihren frühesten Stadien zu erkennen. Eine jährliche Befragung, die hauptsächlich auf vorübergehende Symptome abzielt, muss durchgeführt werden, zusammen mit einer medizinischen Untersuchung, die eine Lungenfunktionsprüfung und andere geeignete medizinische Untersuchungen umfasst. Da nachgewiesen wurde, dass eine gute Korrelation zwischen Kobaltkonzentrationen im Arbeitsumfeld und der Ausscheidung des Metalls über den Urin besteht, ist es angebracht, halbjährliche Messungen von Kobalt im Urin (CoU) an Proben durchzuführen, die am Ende des Jahres entnommen wurden die Arbeitswoche. Wenn die Exposition auf dem TLV-Niveau liegt, wird der biologische Expositionsindex (BEI) auf 30 μg Co/Liter Urin geschätzt.
Ärztliche Untersuchungen vor der Exposition auf das Vorhandensein von vorbestehenden Atemwegserkrankungen und Überempfindlichkeit der Bronchien können bei der Beratung und Vermittlung von Arbeitnehmern hilfreich sein. Metacholin-Tests sind ein nützlicher Indikator für eine unspezifische bronchiale Hyperreaktivität und können in einigen Situationen nützlich sein.
Eine internationale Standardisierung von umweltbezogenen und medizinischen Überwachungsmethoden für Arbeitnehmer, die Kobalt ausgesetzt sind, wird dringend empfohlen.
Asbestbedingte Krankheiten
Historische Perspektive
Asbest ist ein Begriff, der verwendet wird, um eine Gruppe von natürlich vorkommenden Fasermineralien zu beschreiben, die in Felsaufschlüssen und Ablagerungen auf der ganzen Welt sehr weit verbreitet sind. Die Ausnutzung der zug- und hitzebeständigen Eigenschaften von Asbest für den menschlichen Gebrauch stammt aus der Antike. So wurde beispielsweise im dritten Jahrhundert v. Chr. Asbest zur Verstärkung von Tongefäßen in Finnland verwendet. In klassischen Zeiten wurden aus Asbest gewebte Leichentücher verwendet, um die Asche der berühmten Toten aufzubewahren. Marco Polo kehrte von seinen Reisen in China mit Beschreibungen eines magischen Materials zurück, das zu einem flammfesten Stoff verarbeitet werden konnte. In den frühen Jahren des 1860. Jahrhunderts waren Lagerstätten in mehreren Teilen der Welt bekannt, darunter im Uralgebirge, in Norditalien und anderen Mittelmeergebieten, in Südafrika und in Kanada, aber die kommerzielle Ausbeutung begann erst in der zweiten Hälfte des Jahres das neunzehnte Jahrhundert. Zu diesem Zeitpunkt schuf die industrielle Revolution nicht nur die Nachfrage (z. B. die Isolierung der Dampfmaschine), sondern erleichterte auch die Produktion, wobei die Mechanisierung das manuelle Ausstanzen von Fasern aus dem Muttergestein ersetzte. Die moderne Industrie begann nach 1880 in Italien und im Vereinigten Königreich und wurde durch die Erschließung und Ausbeutung der umfangreichen Lagerstätten von Chrysotil (weißem) Asbest in Quebec (Kanada) in den 1920er Jahren angekurbelt. Die Ausbeutung der ebenfalls umfangreichen Chrysotilvorkommen im Uralgebirge war bis in die 1918er Jahre bescheiden. Die langen, dünnen Chrysotilfasern eigneten sich besonders zum Spinnen zu Stoffen und Filzen, einer der frühen kommerziellen Anwendungen für das Mineral. Die Ausbeutung der Krokydolith- (blauen) Asbestvorkommen am Nordwestkap, Südafrika, einer Faser, die wasserbeständiger als Chrysotil und besser für den Einsatz im Meer geeignet ist, und der Amosit- (braunen) Asbestvorkommen, die ebenfalls in Südafrika zu finden sind, begann in den frühen Jahren dieses Jahrhunderts. Die Ausbeutung der finnischen Vorkommen von Anthophyllit-Asbest, der einzigen wichtigen kommerziellen Quelle dieser Faser, fand zwischen 1966 und 1937 statt, während die Vorkommen von Krokydolith in Wittenoom, Westaustralien, von 1966 bis XNUMX abgebaut wurden.
Fasertypen
Die Asbestminerale fallen in zwei Gruppen, die Serpentinengruppe, zu der Chrysotil gehört, und die Amphibole, zu denen Krokydolith, Tremolit, Amosit und Anthophyllit gehören (Abbildung 1). Die meisten Erzvorkommen sind mineralogisch heterogen, ebenso wie die meisten kommerziellen Formen des Minerals (Skinner, Roos und Frondel 1988). Chrysotil und die verschiedenen Amphibol-Asbestminerale unterscheiden sich in der kristallinen Struktur, in den chemischen und Oberflächeneigenschaften und in den physikalischen Eigenschaften ihrer Fasern, die normalerweise als Verhältnis von Länge zu Durchmesser (oder Aspekt) beschrieben werden. Sie unterscheiden sich auch in Merkmalen, die die kommerzielle Verwendung und Qualität unterscheiden. Relevant für die aktuelle Diskussion ist der Beweis, dass sich die verschiedenen Fasern in ihrer biologischen Potenz unterscheiden (wie unten in den Abschnitten über verschiedene Krankheiten betrachtet).
Abbildung 1. Asbestfasertypen.
Auf Elektronenmikroskopie zusammen mit energiedispersiven Röntgenspektren zu sehen, was die Identifizierung einzelner Fasern ermöglicht. Mit freundlicher Genehmigung von A. Dufresne und M. Harrigan, McGill University.
Kommerzielle Produktion
Das Wachstum der kommerziellen Produktion, dargestellt in Abbildung 2, war in den frühen Jahren dieses Jahrhunderts langsam. Beispielsweise überstieg die kanadische Produktion 100,000 zum ersten Mal 1911 Short Tons pro Jahr und 200,000 1923 Tonnen. Das Wachstum zwischen den beiden Weltkriegen war stetig, nahm erheblich zu, um den Anforderungen des Zweiten Weltkriegs gerecht zu werden, und spektakulär, um den Bedarf in Friedenszeiten zu decken ( einschließlich derjenigen des Kalten Krieges), um 1976 einen Höchststand von 5,708,000 Short Tons zu erreichen (Selikoff und Lee 1978). Danach geriet die Produktion ins Stocken, da die gesundheitsschädlichen Auswirkungen der Exposition in Nordamerika und Europa zu einem zunehmend öffentlichen Problem wurden und bis 4,000,000 bei etwa 1986 Short Tons pro Jahr blieben, in den 1990er Jahren jedoch weiter zurückgingen. In den 1980er Jahren gab es auch eine Verschiebung bei der Verwendung und den Quellen von Fasern; in Europa und Nordamerika ging die Nachfrage zurück, da Ersatzstoffe für viele Anwendungen eingeführt wurden, während auf den afrikanischen, asiatischen und südamerikanischen Kontinenten die Nachfrage nach Asbest stieg, um den Bedarf an einem billigen, langlebigen Material für den Einsatz im Bauwesen und in der Wasserversorgung zu decken. Bis 1981 war Russland mit zunehmender kommerzieller Ausbeutung großer Lagerstätten in China und Brasilien zum größten Produzenten der Welt geworden. Im Jahr 1980 wurde geschätzt, dass weltweit insgesamt über 100 Millionen Tonnen Asbest abgebaut wurden, davon 90 % Chrysotil, davon etwa 75 % aus 4 Chrysotil-Abbaugebieten in Quebec (Kanada), Südafrika und Südafrika das zentrale und südliche Uralgebirge. Zwei bis drei Prozent der weltweiten Gesamtproduktion waren Krokydolith aus dem Nordkap, Südafrika, und aus Westaustralien, und weitere 2 bis 3 % waren Amosit aus dem östlichen Transvaal, Südafrika (Skinner, Ross und Frondel 1988). .
Abbildung 2. Weltproduktion von Asbest in Tausend Tonnen 1900-92
Asbestbedingte Krankheiten und Zustände
Wie Siliziumdioxid hat Asbest die Fähigkeit, Narbenreaktionen in allen biologischen Geweben, Menschen und Tieren, hervorzurufen. Darüber hinaus ruft Asbest bösartige Reaktionen hervor, was der Sorge um die menschliche Gesundheit ein weiteres Element hinzufügt und die Wissenschaft herausfordert, wie Asbest seine negativen Auswirkungen ausübt. Die erste anerkannte asbestbedingte Krankheit, diffuse interstitielle Lungenfibrose oder Vernarbung, später als Asbestose bezeichnet, war Anfang des 1900. Jahrhunderts Gegenstand von Fallberichten im Vereinigten Königreich. Später, in den 1930er Jahren, erschienen Fallberichte über Lungenkrebs in Verbindung mit Asbestose in der medizinischen Literatur, obwohl erst in den nächsten Jahrzehnten wissenschaftliche Beweise dafür gesammelt wurden, dass Asbest der krebserregende Faktor war. Im Jahr 1960 wurde der Zusammenhang zwischen Asbestexposition und einem anderen viel selteneren Krebs, bösartigem Mesotheliom, das die Pleura (eine Membran, die die Lunge bedeckt und die Brustwand auskleidet) betroffen ist, durch den Bericht über eine Anhäufung dieser Tumore in dramatischer Weise auf sich aufmerksam gemacht 33 Personen, die alle im Asbestabbaugebiet des Nordwestkaps arbeiteten oder lebten (Wagner 1996). Asbestose war das Ziel der in den 1960er und 1970er Jahren mit zunehmender Strenge eingeführten und umgesetzten Staubschutzmaßnahmen, und in vielen Industrieländern trat mit abnehmender Häufigkeit dieser Krankheit eine asbestbedingte Pleuraerkrankung als häufigste Manifestation der Exposition auf Zustand, der exponierte Personen am häufigsten zu ärztlicher Behandlung führte. Tabelle 1 listet Krankheiten und Zustände auf, die derzeit als asbestbedingt anerkannt sind. Die fettgedruckten Krankheiten sind diejenigen, die am häufigsten vorkommen und für die ein direkter kausaler Zusammenhang gut belegt ist, während der Vollständigkeit halber auch bestimmte andere Erkrankungen aufgeführt sind, für die der Zusammenhang weniger gut belegt ist (siehe Fußnote zu Tabelle 16 ) und die im Text folgenden Abschnitte, die sich mit den verschiedenen Krankheitsüberschriften befassen).
Tabelle 1. Asbestbedingte Krankheiten und Zustände
| Pathologie | Organ(e) betroffen | Krankheit/Zustand1 |
| Nicht bösartig | Lunge Pleura Haut | Asbestose (diffuse interstitielle Fibrose) Erkrankung der kleinen Atemwege2 (Fibrose beschränkt auf die peribronchioläre Region) Chronische Atemwegserkrankung3 Pleuraplaques Viszeroparietale Reaktionen, einschließlich gutartiger Pleura Erguss, diffuse Pleurafibrose und gerundet Atelektase Asbest Hühneraugen4 |
| Maligne | Lunge Brustfell Andere mit Mesothel ausgekleidete Hohlräume Gastrointestinaltrakt5 Andere5 | Lungenkrebs (alle Zelltypen) Kehlkopfkrebs Mesotheliom der Pleura Mesotheliom des Peritoneums, Herzbeutel und Hodensack (in abnehmender Häufigkeit) Krebs des Magens, der Speiseröhre, des Dickdarms, des Mastdarms, der Eierstöcke, der Gallenblase, der Gallenwege, der Bauchspeicheldrüse, der Niere |
1 Die fett gedruckten Krankheiten oder Zustände sind die am häufigsten auftretenden und diejenigen, für die ein kausaler Zusammenhang gut etabliert und/oder allgemein anerkannt ist.
2 Es wird angenommen, dass Fibrose in den Wänden der kleinen Atemwege der Lunge (einschließlich der membranösen und respiratorischen Bronchiolen) die frühe Reaktion des Lungenparenchyms auf zurückgehaltenes Asbest darstellt (Wright et al. 1992), die sich zu Asbestose entwickelt, wenn die Exposition andauert und/oder besteht schwer, aber wenn die Exposition begrenzt oder leicht ist, kann die Lungenreaktion auf diese Bereiche beschränkt sein (Becklake in Liddell & Miller 1991).
3 Eingeschlossen sind Bronchitis, chronisch obstruktive Lungenerkrankung (COPD) und Emphysem. Es wurde gezeigt, dass alle mit Arbeiten in staubigen Umgebungen in Verbindung gebracht werden. Die Beweise für die Kausalität werden in diesem Abschnitt überprüft Chronische Atemwegserkrankungen und Becklake (1992).
4 Bezieht sich auf den direkten Umgang mit Asbest und ist eher von historischem als aktuellem Interesse.
5 Daten nicht konsistent aus allen Studien (Doll und Peto 1987); Einige der höchsten Risiken wurden in einer Kohorte von über 17,000 amerikanischen und kanadischen Asbestisolierarbeitern (Selikoff 1990) berichtet, die vom 1. Januar 1967 bis zum 31. Dezember 1986 beobachtet wurden und bei denen die Exposition besonders stark war.
Quellen: Becklake 1994; Liddell und Miller 1992; Selikoff 1990; Doll und Peto in Antman und Aisner 1987; Wrightet al. 1992.
Verwendung
Tabelle 2 listet die wichtigsten Quellen, Produkte und Verwendungen der Asbestmineralien auf.
Tabelle 2. Haupthandelsquellen, Produkte und Verwendungen von Asbest
| Fasertyp | Lage der wichtigsten Lagerstätten | Kommerzielle Produkte und/oder Verwendungen |
| Chrysotil (Weiß) |
Russland, Kanada (Québec, auch British Columbia, Neufundland), China (Provinz Sezuan); Mittelmeerländer (Italien, Griechenland, Korsika, Zypern); Südliches Afrika (Südafrika, Simbabwe, Swasiland); Brasilien; kleinere Vorkommen in den Vereinigten Staaten (Vermont, Arizona, Kalifornien) und in Japan | Baumaterialien (Fliesen, Schindeln, Dachrinnen und Zisternen; Dächer, Bleche und Verkleidungen) Druck- und andere Leitungen Brandschutz (Marine und andere) Isolierung und Schallschutz Verstärkte Kunststoffprodukte (Lüfterblätter, Schaltgeräte) Reibmaterialien in der Regel in Kombination mit Harzen in Bremsen, Kupplungen usw Textilien (verwendet in Gürteln, Kleidung, Hüllen, Feuerschutzwänden, Autoklaven, Garnen und Verpackungen) Papierprodukte (verwendet in Vollpappe, Isolatoren, Dichtungen, Dachpappe, Wandverkleidungen usw.) Schwimmt in Farben, Lacken und Schweißstäben |
| Crocidolite (Blau) |
Südafrika (Nordwestkap, Ost-Transvaal), Westaustralien1 | Wird hauptsächlich in Kombination in Zementprodukten (insbesondere Druckrohren), aber auch in vielen anderen oben aufgeführten Produkten verwendet |
| Amosite (braun) |
Südafrika (Nord-Transvaal)1 | Wird hauptsächlich in Zement, Wärmedämmung und Dachprodukten verwendet, insbesondere in den Vereinigten Staaten2 , aber auch in Kombination in vielen der unter Chrysotil aufgeführten Produkte |
| Anthophyllit | Finnland1 | Füllstoff in der Gummi-, Kunststoff- und chemischen Industrie |
| Tremolit | Italien, Korea und einige pazifische Inseln; in kleinem Maßstab in der Türkei, China und anderswo abgebaut; kontaminiert das erzhaltige Gestein in einigen Asbest-, Eisen-, Talk- und Vermiculitminen; auch in landwirtschaftlichen Böden auf der Balkanhalbinsel und in der Türkei gefunden | Wird als Füllstoff in Talk verwendet; kann bei der Verarbeitung des Erzes entfernt werden oder nicht, so dass es in Endprodukten erscheinen kann |
| Actinolite | Kontaminiert Amosit und seltener Chrysotil-, Talk- und Vermiculitablagerungen | Wird normalerweise nicht kommerziell genutzt |
1 Eine solche Liste ist natürlich nicht vollständig, und die Leser sollten die zitierten Quellen und andere Kapitel darin konsultieren Enzyklopädie für ausführlichere Informationen.
2 Nicht mehr in Betrieb.
Quellen: Asbestos Institute (1995); Browne (1994); Liddell und Miller (1991); Selikoff und Lee (1978); Skinneret al. (1988).
Obwohl notwendigerweise unvollständig, betont diese Tabelle Folgendes:
- Lagerstätten befinden sich in vielen Teilen der Welt, von denen die meisten in der Vergangenheit nichtkommerziell oder kommerziell ausgebeutet wurden und von denen einige derzeit kommerziell ausgebeutet werden.
- Es gibt viele hergestellte Produkte, die gegenwärtig oder in der Vergangenheit verwendet werden und Asbest enthalten, insbesondere in der Bau- und Transportindustrie.
- Der Zerfall dieser Produkte oder ihre Entfernung birgt das Risiko der Resuspension von Fasern und einer erneuten Exposition des Menschen.
Eine Zahl von über 3,000 wird allgemein für die Anzahl der Verwendungen von Asbest genannt und führte zweifellos dazu, dass Asbest in den 1960er Jahren als das „magische Mineral“ bezeichnet wurde. Eine Industrieliste von 1953 enthält nicht weniger als 50 Verwendungen für Rohasbest, zusätzlich zu seiner Verwendung bei der Herstellung der in Tabelle 17 aufgeführten Produkte, von denen jede viele andere industrielle Anwendungen hat. 1972 wurde der Asbestverbrauch in einem Industrieland wie den Vereinigten Staaten den folgenden Produktkategorien zugeordnet: Baugewerbe (42 %); Reibungsmaterialien, Filze, Packungen und Dichtungen (20 %); Bodenfliesen (11%); Papier (9%); Isolierung und Textilien (3 %) und andere Verwendungen (15 %) (Selikoff und Lee 1978). Im Gegensatz dazu zeigt eine Industrieliste der Hauptproduktkategorien von 1995 eine große Umverteilung auf weltweiter Basis wie folgt: Asbestzement (84 %); Reibungsmaterialien (10 %); Textilien (3%); Dichtungen und Dichtungen (2%); und andere Verwendungen (1%) (Asbestos Institute 1995).
Berufliche Expositionen, Vergangenheit und Gegenwart
Berufsbedingte Exposition, sicherlich in Industrieländern, war und ist immer noch die wahrscheinlichste Quelle menschlicher Exposition (siehe Tabelle 17 und die in der Fußnote zitierten Referenzen; andere Abschnitte davon Enzyklopädie weitere Informationen enthalten). Es gab jedoch große Veränderungen in industriellen Prozessen und Verfahren, die darauf abzielten, die Freisetzung von Staub in die Arbeitsumgebung zu verringern (Browne 1994; Selikoff und Lee 1978). In Ländern mit Bergbaubetrieben findet das Fräsen normalerweise am Kopf statt. Die meisten Chrysotilminen werden im Tagebau abgebaut, während Amphibolminen normalerweise unterirdische Methoden beinhalten, die mehr Staub erzeugen. Beim Mahlen werden Fasern durch mechanisiertes Brechen und Sieben von Gestein getrennt, was bis zur Einführung von Nassverfahren und / oder Einhausungen in den meisten Mühlen in den 1950er und 1960er Jahren staubige Prozesse waren. Der Umgang mit Abfällen war auch eine Quelle menschlicher Exposition, ebenso wie der Transport von Asbest in Säcken, sei es beim Be- und Entladen von Lastwagen und Eisenbahnwaggons oder bei Arbeiten am Hafen. Diese Belastungen sind seit der Einführung auslaufsicherer Beutel und der Verwendung versiegelter Behälter zurückgegangen.
Arbeiter mussten Rohasbest direkt zum Verpacken und Verkleiden verwenden, insbesondere in Lokomotiven, und zum Spritzen von Wänden, Decken und Luftkanälen und in der Schiffsindustrie, Decksköpfen und Schotten. Einige dieser Verwendungen wurden freiwillig eingestellt oder verboten. Bei der Herstellung von Asbestzementprodukten erfolgt die Exposition beim Empfangen und Öffnen von Säcken mit Rohasbest, beim Vorbereiten der Faser zum Mischen in die Aufschlämmung, bei der Verarbeitung von Endprodukten und beim Umgang mit Abfällen. Bei der Herstellung von Vinylfliesen und -böden wurde Asbest als Verstärkungs- und Füllmittel zum Mischen mit organischen Harzen verwendet, wurde jedoch in Europa und Nordamerika inzwischen weitgehend durch organische Fasern ersetzt. Bei der Herstellung von Garnen und Textilien werden Fasern beim Empfangen, Vorbereiten, Mischen, Kardieren, Spinnen, Weben und Kalandrieren der Fasern ausgesetzt – Prozesse, die bis vor kurzem trocken und potenziell sehr staubig waren. Die Staubexposition wurde in modernen Anlagen durch die Verwendung einer kolloidalen Fasersuspension, die durch ein Koagulans extrudiert wurde, um nasse Stränge für die letztgenannten drei Verfahren zu bilden, beträchtlich verringert. Bei der Herstellung von Asbestpapierprodukten ist es auch am wahrscheinlichsten, dass Menschen Asbeststaub bei der Annahme und Zubereitung der Stoffmischung und beim Schneiden der Endprodukte ausgesetzt werden, die in den 1970er Jahren 30 bis 90 % Asbest enthielten. Bei der Herstellung von Asbest-Reibungsprodukten (trockengemischt, rollgeformt, gewebt oder endlos gewickelt) ist es auch am wahrscheinlichsten, dass Menschen Asbeststaub während der anfänglichen Handhabungs- und Mischprozesse sowie bei der Endbearbeitung des Endprodukts ausgesetzt werden in den 1970er Jahren enthielten 30 bis 80 % Asbest. In der Bauindustrie führte vor der regelmäßigen Verwendung einer geeigneten Absaugung (die in den 1960er Jahren aufkam) das Hochgeschwindigkeitssägen, Bohren und Schleifen von asbesthaltigen Platten oder Fliesen zur Freisetzung von faserhaltigem Staub in der Nähe der Atembereich des Bedieners, insbesondere wenn solche Arbeiten in geschlossenen Räumen durchgeführt wurden (z. B. in im Bau befindlichen Hochhäusern). In der Zeit nach dem Zweiten Weltkrieg war die Verwendung, Entfernung oder der Ersatz asbesthaltiger Materialien beim Abriss oder der Renovierung von Gebäuden oder Schiffen eine Hauptquelle der Exposition des Menschen. Einer der Hauptgründe für diesen Zustand war das mangelnde Bewusstsein sowohl für die Zusammensetzung dieser Materialien (dh dass sie Asbest enthielten) als auch dafür, dass Asbest gesundheitsschädlich sein könnte. Verbesserte Arbeitnehmerausbildung, bessere Arbeitspraktiken und persönlicher Schutz haben das Risiko in den 1990er Jahren in einigen Ländern verringert. In der Transportindustrie waren die Expositionsquellen das Entfernen und Ersetzen von Belägen in Lokomotivmotoren und von Bremsmaterial in Lastkraftwagen und Autos in der Autoreparaturindustrie.
Andere Expositionsquellen
Als Exposition von Personen bezeichnet, die in Gewerben tätig sind, die nicht direkt die Verwendung oder den Umgang mit Asbest beinhalten, aber im selben Bereich wie diejenigen arbeiten, die direkt damit zu tun haben paraberuflich (Zuschauer) Exposition. Dies war nicht nur in der Vergangenheit eine wichtige Expositionsquelle, sondern auch für Fälle, die in den 1990er Jahren zur Diagnose vorstellig wurden. Zu den beteiligten Arbeitern gehören Elektriker, Schweißer und Zimmerleute in der Bau- und Schiffbau- oder Reparaturindustrie; Wartungspersonal in Asbestfabriken; Monteure, Heizer und andere in Kraftwerken und Schiffen und Kesselhäusern, in denen Asbestisolierungen oder andere Isolierungen vorhanden sind, und Wartungspersonal in Hochhäusern der Nachkriegszeit, die verschiedene asbesthaltige Materialien enthalten. In der Vergangenheit, inländische Exposition traten hauptsächlich auf, wenn staubbeladene Arbeitskleidung zu Hause geschüttelt oder gewaschen wurde, wobei der so freigesetzte Staub in Teppichen oder Einrichtungsgegenständen eingeschlossen und bei den Aktivitäten des täglichen Lebens wieder in die Luft geschleudert wurde. Die Faserkonzentrationen in der Luft konnten nicht nur Werte von bis zu 10 Fasern pro Milliliter (f/ml) erreichen, d. h. das Zehnfache des Arbeitsplatzgrenzwerts, der von einer WHO-Konsultation (1989) von 1.0 f/ml vorgeschlagen wurde, sondern die Fasern blieben tendenziell bestehen mehrere Tage in der Luft. Seit den 1970er Jahren ist die Praxis, die gesamte Arbeitskleidung zum Waschen auf der Baustelle aufzubewahren, weit verbreitet, aber nicht überall verbreitet. In der Vergangenheit kam es auch zu Expositionen in Wohngebieten durch Kontamination der Luft aus industriellen Quellen. Beispielsweise wurden in der Umgebung von Bergwerken und Asbestanlagen erhöhte Konzentrationen von Asbest in der Luft dokumentiert, die durch Produktionsmengen, Emissionskontrollen und Wetter bestimmt werden. Angesichts der langen Verzögerungszeit insbesondere bei asbestbedingten Pleuraerkrankungen sind solche Expositionen wahrscheinlich immer noch für einige Fälle verantwortlich, die in den 1990er Jahren zur Diagnose gestellt wurden. In den 1970er und 1980er Jahren, mit dem zunehmenden öffentlichen Bewusstsein sowohl für die gesundheitlichen Folgen der Asbestexposition als auch für die Tatsache, dass asbesthaltige Materialien in großem Umfang im modernen Bauwesen verwendet werden (insbesondere in brüchiger Form, die zum Aufsprühen von Wänden verwendet wird). , Decken und Lüftungskanäle), gab Anlass zu großer Besorgnis darüber, ob Asbestfasern mit zunehmendem Alter und täglicher Abnutzung in der Luft in ausreichender Menge freigesetzt werden, um die Gesundheit der Beschäftigten zu gefährden B. in modernen Hochhäusern (Risikoabschätzungen siehe unten). Andere Quellen der Luftverschmutzung in städtischen Gebieten umfassen die Freisetzung von Fasern aus Bremsen von Fahrzeugen und die erneute Streuung von Fasern, die von vorbeifahrenden Fahrzeugen freigesetzt werden (Bignon, Peto und Saracci 1989).
Zu den nichtindustriellen Quellen der Umweltexposition gehören natürlich vorkommende Fasern in Böden, beispielsweise in Osteuropa, und in Felsvorsprüngen im Mittelmeerraum, einschließlich Korsika, Zypern, Griechenland und der Türkei (Bignon, Peto und Saracci 1989). Eine zusätzliche Expositionsquelle für den Menschen ergibt sich aus der Verwendung von Tremolit für Tünche und Stuckarbeiten in Griechenland und der Türkei und nach neueren Berichten in Neukaledonien im Südpazifik (Luce et al. 1994). Darüber hinaus wurde in mehreren ländlichen Dörfern in der Türkei festgestellt, dass eine Zeolithfaser, Erionit, sowohl im Stuck als auch im Hausbau verwendet wird und mit der Mesotheliomproduktion in Verbindung gebracht wird (Bignon, Peto und Saracci 1991). Schließlich kann eine Exposition des Menschen durch Trinkwasser erfolgen, hauptsächlich durch natürliche Kontamination, und angesichts der weit verbreiteten natürlichen Verteilung der Faser in Aufschlüssen enthalten die meisten Wasserquellen einige Fasern, wobei die Konzentrationen in Bergbaugebieten am höchsten sind (Skinner, Roos und Frondel 1988).
Ätiopathologie von asbestbedingten Erkrankungen
Schicksal eingeatmeter Fasern
Eingeatmete Fasern richten sich mit dem Luftstrom aus und ihre Fähigkeit, in die tieferen Lungenräume einzudringen, hängt von ihrer Abmessung ab, wobei Fasern mit einem aerodynamischen Durchmesser von 5 mm oder weniger eine über 80 %ige Penetration, aber auch eine Retention von weniger als 10 bis 20 % aufweisen. Größere Partikel können in der Nase und in den Hauptluftwegen an Verzweigungen auftreffen, wo sie sich leicht ansammeln. In den Hauptluftwegen abgelagerte Partikel werden durch die Wirkung von Flimmerzellen entfernt und die Schleimrolltreppe nach oben transportiert. Individuelle Unterschiede im Zusammenhang mit scheinbar gleicher Exposition sind zumindest teilweise auf Unterschiede zwischen Individuen in der Penetration und Retention eingeatmeter Fasern zurückzuführen (Bégin, Cantin und Massé 1989). Kleine Partikel, die sich außerhalb der großen Atemwege ablagern, werden von Alveolarmakrophagen, Fresszellen, die Fremdmaterial aufnehmen, phagozytiert. Längere Fasern, d. h. solche über 10 mm, werden oft von mehr als einem Makrophagen angegriffen, werden mit größerer Wahrscheinlichkeit beschichtet und bilden den Kern eines Asbestkörpers, eine charakteristische Struktur, die seit Anfang des 1900. Jahrhunderts als Expositionsmarker anerkannt ist ( siehe Bild 3). Das Beschichten einer Faser wird als Teil der Lungenabwehr betrachtet, um sie inert und nicht-immunogen zu machen. Asbestkörper bilden sich eher auf Amphibol als auf Chrysotilfasern, und ihre Dichte in biologischem Material (Sputum, bronchoalveoläre Lavage, Lungengewebe) ist ein indirekter Marker für die Lungenbelastung. Beschichtete Fasern können lange Zeit in der Lunge verbleiben und bis zu 30 Jahre nach der letzten Exposition aus dem Sputum oder der bronchoalveolären Lavageflüssigkeit gewonnen werden. Die Entfernung von nicht beschichteten Fasern, die im Lungenparenchym abgelagert sind, erfolgt in Richtung der Lungenperipherie und der subpleuralen Regionen und dann zu den Lymphknoten an der Lungenwurzel.
Abbildung 3. Asbestkörper
400-fache Vergrößerung, im mikroskopischen Schnitt der Lunge als leicht gebogenes, längliches Gebilde mit einer feinperligen Eisenproteinhülle zu sehen. Die Asbestfaser selbst kann als dünne Linie nahe einem Ende des Asbestkörpers identifiziert werden (Pfeil). Quelle: Fraser et al. 1990
Theorien zur Erklärung, wie Fasern die verschiedenen Pleurareaktionen hervorrufen, die mit einer Asbestexposition verbunden sind, umfassen:
- direktes Eindringen in den Pleuraraum und Drainage mit der Pleuraflüssigkeit zu Poren in der Pleura, die die Brustwand auskleidet
- Freisetzung von Mediatoren in den Pleuraraum aus subpleuralen Lymphansammlungen
- Rückfluss von Lymphknoten an der Lungenwurzel zur parietalen Pleura (Browne 1994)
Es kann auch einen retrograden Fluss über den Ductus thoracicus zu den abdominalen Lymphknoten geben, um das Auftreten eines Peritonealmesothelioms zu erklären.
Zellwirkungen eingeatmeter Ballaststoffe
Tierversuche weisen darauf hin, dass die ersten Ereignisse, die auf die Asbestretention in der Lunge folgen, Folgendes umfassen:
- eine entzündliche Reaktion mit Anhäufung weißer Blutkörperchen, gefolgt von einer makrophagischen Alveolitis mit Freisetzung von Fibronektin, Wachstumsfaktor und verschiedenen neutrophilen chemotaktischen Faktoren und im Laufe der Zeit der Freisetzung von Superoxidionen und
- Proliferation von Alveolar-, Epithel-, Interstitial- und Endothelzellen (Bignon, Peto und Saracci 1989).
Diese Ereignisse spiegeln sich in dem Material wider, das durch bronchoalveoläre Lavage bei Tieren und Menschen gewonnen wurde (Bégin, Cantin und Massé 1989). Sowohl die Faserabmessungen als auch ihre chemischen Eigenschaften scheinen die biologische Potenz für die Fibrogenese zu bestimmen, und diese Eigenschaften werden zusätzlich zu den Oberflächeneigenschaften auch für wichtig für die Karzinogenese gehalten. Lange, dünne Fasern sind aktiver als kurze, obwohl die Aktivität der letzteren nicht außer Acht gelassen werden kann, und Amphibole sind aktiver als Chrysotil, eine Eigenschaft, die ihrer größeren Biopersistenz zugeschrieben wird (Bégin, Cantin und Massé 1989). Asbestfasern können auch das menschliche Immunsystem beeinträchtigen und die zirkulierende Population von Blutlymphozyten verändern. Beispielsweise kann die durch menschliche Zellen vermittelte Immunität gegen Zellantigene (wie sie in einem Tuberkulin-Hauttest gezeigt wird) beeinträchtigt sein (Browne 1994). Da Asbestfasern außerdem in der Lage zu sein scheinen, Chromosomenanomalien zu induzieren, wurde die Ansicht geäußert, dass sie auch als in der Lage angesehen werden können, Krebs zu induzieren und zu fördern (Jaurand in Bignon, Peto und Saracci 1989).
Beziehung zwischen Dosis und Expositionsreaktion
In biologischen Wissenschaften wie der Pharmakologie oder Toxikologie, in denen Dosis-Wirkungs-Beziehungen verwendet werden, um die Wahrscheinlichkeit erwünschter Wirkungen oder das Risiko unerwünschter Wirkungen abzuschätzen, wird eine Dosis als die Menge eines Wirkstoffs verstanden, die an das Zielorgan abgegeben wird und mit diesem in Kontakt bleibt genügend Zeit, um eine Reaktion hervorzurufen. In der Arbeitsmedizin sind Surrogate für die Dosis, wie verschiedene Expositionsmaße, normalerweise die Grundlage für Risikoabschätzungen. Expositions-Wirkungs-Beziehungen können jedoch in der Regel in arbeitsbezogenen Studien nachgewiesen werden; Die am besten geeignete Expositionsmessung kann jedoch je nach Krankheit unterschiedlich sein. Etwas beunruhigend ist die Tatsache, dass sich die Expositions-Wirkungs-Beziehungen zwar zwischen den Arbeitskräften unterscheiden, diese Unterschiede jedoch nur teilweise durch die Faser, die Partikelgröße und den industriellen Prozess erklärt werden können. Dennoch bildeten solche Expositions-Wirkungs-Beziehungen die wissenschaftliche Grundlage für die Risikobewertung und für die Festlegung zulässiger Expositionshöhen, die ursprünglich auf die Kontrolle der Asbestose ausgerichtet waren (Selikoff und Lee 1978). Da die Prävalenz und/oder Inzidenz dieser Erkrankung zurückgegangen ist, hat sich die Sorge verlagert, den Schutz der menschlichen Gesundheit vor asbestbedingten Krebserkrankungen zu gewährleisten. In den letzten zehn Jahren wurden Techniken zur quantitativen Messung der Lungenstaubbelastung oder der biologischen Dosis direkt in Form von Fasern pro Gramm trockenem Lungengewebe entwickelt. Zusätzlich erlaubt die energiedispensive Röntgenanalyse (EDXA) eine genaue Charakterisierung jeder Faser nach Fasertyp (Churg 1991). Obwohl noch keine Standardisierung der Ergebnisse zwischen Laboratorien erreicht wurde, sind Vergleiche von Ergebnissen, die innerhalb eines bestimmten Labors erzielt wurden, nützlich, und Messungen der Lungenbelastung haben ein neues Werkzeug für die Fallbewertung hinzugefügt. Darüber hinaus hat sich die Anwendung dieser Techniken in epidemiologischen Studien bewährt
- bestätigten die Biopersistenz von Amphibolfasern in der Lunge im Vergleich zu Chrysotilfasern
- identifizierte Faserbelastung in der Lunge einiger Personen, bei denen die Exposition vergessen, weit entfernt oder für unwichtig gehalten wurde
- zeigten einen Gradienten der Lungenbelastung im Zusammenhang mit ländlichem und städtischem Aufenthalt sowie mit beruflicher Exposition und
- bestätigten einen Fasergradienten in der Lungenstaubbelastung im Zusammenhang mit den wichtigsten asbestbedingten Krankheiten (Becklake und Case 1994).
Asbestose
Definition und Geschichte
Asbestose ist die Bezeichnung für die Pneumokoniose infolge einer Exposition gegenüber Asbeststaub. Der Begriff Pneumokoniose wird hier wie im Artikel „Pneumokoniosen: Definitionen“ definiert verwendet Enzyklopädie als ein Zustand, in dem es zu einer „Ansammlung von Staub in der Lunge und Gewebereaktionen auf den Staub“ kommt. Bei Asbestose ist die Gewebereaktion kollagenartig und führt zu einer dauerhaften Veränderung der Alveolararchitektur mit Narbenbildung. Bereits 1898 wurde die Jahresbericht des Chief Inspector of Factories Ihrer Majestät enthielt einen Verweis auf den Bericht einer Fabrikinspektorin über die gesundheitsschädlichen Folgen der Asbestexposition und den Bericht von 1899 Profil melden enthielt Details eines solchen Falls bei einem Mann, der 12 Jahre lang in einer der kürzlich gegründeten Textilfabriken in London, England, gearbeitet hatte. Die Autopsie ergab eine diffuse schwere Fibrose der Lunge, und was später als Asbestkörper bekannt wurde, wurde bei der anschließenden histologischen erneuten Untersuchung der Objektträger gesehen. Da Lungenfibrose ein seltener Zustand ist, wurde angenommen, dass der Zusammenhang kausal ist, und der Fall wurde 1907 einem Komitee zur Entschädigung für Berufskrankheiten vorgelegt (Browne 1994). Trotz des Erscheinens von Berichten ähnlicher Art, die von Inspektoren aus dem Vereinigten Königreich, Europa und Kanada im Laufe des nächsten Jahrzehnts eingereicht wurden, wurde die Rolle der Asbestexposition bei der Entstehung der Erkrankung nicht allgemein anerkannt, bis ein Fallbericht im veröffentlicht wurde British Medical Journal im Jahr 1927. In diesem Bericht wird der Begriff Lungenasbestose wurde zuerst verwendet, um diese spezielle Pneumokoniose zu beschreiben, und es wurde die Bedeutung der damit verbundenen pleuralen Reaktionen kommentiert, im Gegensatz beispielsweise zu Silikose, der damals anerkannten Hauptpneumokoniose (Selikoff und Lee 1978). In den 1930er Jahren lieferten zwei große arbeitsbezogene Studien, die unter Textilarbeitern durchgeführt wurden, eine im Vereinigten Königreich und eine in den Vereinigten Staaten, Beweise für eine Expositions-Wirkungs-Beziehung (und daher wahrscheinlich eine kausale) Beziehung zwischen Höhe und Dauer der Exposition und Röntgenaufnahmen Veränderungen, die auf Asbestose hindeuten. Diese Berichte bildeten die Grundlage der ersten Kontrollvorschriften im Vereinigten Königreich, die 1930 verkündet wurden, und der ersten Grenzwerte für Asbest, die 1938 von der American Conference of Government and Industrial Hygienists veröffentlicht wurden (Selikoff und Lee 1978).
Pathologie
Die fibrotischen Veränderungen, die Asbestose charakterisieren, sind die Folge eines entzündlichen Prozesses, der durch in der Lunge zurückgehaltene Fasern ausgelöst wird. Die Fibrose der Asbestose ist interstitiell, diffus, neigt dazu, bevorzugt die unteren Lappen und die peripheren Zonen zu betreffen, und ist im fortgeschrittenen Fall mit einer Obliteration der normalen Lungenarchitektur verbunden. Eine Fibrose der angrenzenden Pleura ist häufig. Nichts in den histologischen Merkmalen der Asbestose unterscheidet sie von interstitieller Fibrose aufgrund anderer Ursachen, außer dem Vorhandensein von Asbest in der Lunge, entweder in Form von Asbestkörpern, die für das Lichtmikroskop sichtbar sind, oder als unbeschichtete Fasern, von denen die meisten zu fein sind außer mittels Elektronenmikroskopie gesehen werden. Somit schließt das Fehlen von Asbestkörpern in lichtmikroskopischen Bildern weder eine Exposition noch die Diagnose einer Asbestose aus. Am anderen Ende des Spektrums der Schwere der Erkrankung kann die Fibrose auf relativ wenige Zonen begrenzt sein und hauptsächlich die peribronchiolären Regionen betreffen (siehe Abbildung 4), was zu einer sogenannten asbestbedingten Erkrankung der kleinen Atemwege führt. Wiederum, außer vielleicht einer stärkeren Beteiligung der häutigen kleinen Atemwege, unterscheidet nichts in den histologischen Veränderungen dieses Zustands ihn von einer Erkrankung der kleinen Atemwege aufgrund anderer Ursachen (wie Zigarettenrauchen oder Kontakt mit anderen Mineralstäuben) außer dem Vorhandensein von Asbest in die Lunge. Die Erkrankung der kleinen Atemwege kann die einzige Manifestation einer asbestbedingten Lungenfibrose sein oder sie kann mit interstitieller Fibrose unterschiedlichen Grades, d. h. Asbestose, koexistieren (Wright et al. 1992). Zur pathologischen Einstufung der Asbestose wurden sorgfältig erwogene Kriterien veröffentlicht (Craighead et al. 1982). Allgemein hängt das Ausmaß und die Intensität der Lungenfibrose von der gemessenen Lungenstaubbelastung ab (Liddell und Miller 1991).
Abbildung 4. Asbestbedingte Erkrankung der kleinen Atemwege
Peribronchioläre Fibrose und Infiltration durch Entzündungszellen sind auf einem histologischen Schnitt einer respiratorischen Bronchiole (R) und ihrer distalen Abteilungen oder Alveolargänge (A) zu sehen. Die umgebende Lunge ist größtenteils normal, aber mit fokaler Verdickung des interstitiellen Gewebes (Pfeil), was eine frühe Asbestose darstellt. Quelle: Fraser et al. 1990
Klinische Merkmale
Kurzatmigkeit, die früheste, am häufigsten berichtete und quälendste Beschwerde, hat dazu geführt, dass Asbestose als monosymptomatische Krankheit bezeichnet wird (Selikoff und Lee 1978). Kurzatmigkeit geht anderen Symptomen voraus, zu denen ein trockener, oft quälender Husten und ein Engegefühl in der Brust gehören, von denen angenommen wird, dass sie mit pleuralen Reaktionen einhergehen. Späte Atemgeräusche oder Knistergeräusche, die nach dem Husten bestehen bleiben, sind zunächst in der Achselhöhle und über den Lungenbasen zu hören, bevor sie mit fortschreitendem Zustand allgemeiner werden, und es wird angenommen, dass sie auf die explosionsartige Öffnung der Atemwege zurückzuführen sind, die sich beim Ausatmen schließen. Es wird angenommen, dass grobes Rasseln und Rhonchi, falls vorhanden, eine Bronchitis entweder als Reaktion auf die Arbeit in einer staubigen Umgebung oder aufgrund des Rauchens widerspiegeln.
Thorax-Bildgebung
Traditionell war die Röntgenaufnahme des Brustkorbs das wichtigste diagnostische Einzelinstrument zum Nachweis einer Asbestose. Dies wurde durch die Verwendung der radiologischen Klassifikation der ILO (1980) erleichtert, die die kleinen unregelmäßigen Trübungen, die für Asbestose charakteristisch sind, auf einem Kontinuum von keiner Erkrankung bis zur am weitesten fortgeschrittenen Erkrankung einstuft, sowohl nach Schweregrad (beschrieben als Überschuss auf einer 12- bis Punkteskala von –/0 bis 3/+) und Ausdehnung (beschrieben als Anzahl der betroffenen Zonen). Trotz Unterschieden zwischen den Lesern, selbst unter denjenigen, die eine Leseschulung absolviert haben, hat sich diese Einteilung in epidemiologischen Studien als besonders nützlich erwiesen und wurde auch klinisch verwendet. Pathologische Veränderungen der Asbestose können jedoch bei bis zu 20 % der Patienten mit einer normalen Röntgenaufnahme des Brustkorbs bei einer Lungenbiopsie vorhanden sein. Darüber hinaus sind kleine unregelmäßige Trübungen mit geringer Streuung (z. B. 1/0 auf der ILO-Skala) nicht spezifisch für Asbestose, sondern können im Zusammenhang mit anderen Expositionen, z. B. Zigarettenrauchen, gesehen werden (Browne 1994). Die Computertomographie (CT) hat die Bildgebung von interstitiellen Lungenerkrankungen, einschließlich Asbestose, revolutioniert, wobei die hochauflösende Computertomographie (HRCT) eine erhöhte Empfindlichkeit für die Erkennung von interstitiellen und pleuralen Erkrankungen bietet (Fraser et al. 1990). Merkmale von Asbestose, die durch HRCT identifiziert werden können, umfassen verdickte interlobuläre (septale) und intralobuläre Kernlinien, Parenchymbänder, krummlinige subpleurale Linien und subpleurale abhängige Dichten, wobei die ersten beiden die charakteristischsten für Asbestose sind (Fraser et al. 1990). HRCT kann diese Veränderungen auch in Fällen mit Lungenfunktionsstörung identifizieren, bei denen die Röntgenaufnahme des Brustkorbs nicht aussagekräftig ist. Basierend auf postmortem HRCT wurde gezeigt, dass verdickte intralobuläre Linien mit peribronchiolärer Fibrose und verdickte interlobuläre Linien mit interstitieller Fibrose korrelieren (Fraser et al. 1990). Bisher wurde noch keine standardisierte Lesemethode für die Verwendung von HRCT bei asbestbedingten Erkrankungen entwickelt. Zusätzlich zu den Kosten macht die Tatsache, dass ein CT-Gerät eine Krankenhausinstallation ist, es unwahrscheinlich, dass es die Thorax-Röntgenaufnahme für Überwachung und epidemiologische Studien ersetzen wird; seine Rolle wird wahrscheinlich auf die Untersuchung von Einzelfällen oder auf geplante Studien zur Behandlung spezifischer Probleme beschränkt bleiben. Fig. 21 veranschaulicht die Verwendung einer Brustbildgebung bei der Diagnose einer asbestbedingten Lungenerkrankung; der gezeigte Fall weist Asbestose, eine asbestbedingte Pleuraerkrankung und Lungenkrebs auf. Große Trübungen, eine Komplikation anderer Pneumokoniosen, insbesondere Silikose, sind bei Asbestose ungewöhnlich und sind normalerweise auf andere Erkrankungen wie Lungenkrebs (siehe den in Abbildung 5 beschriebenen Fall) oder abgerundete Atelektase zurückzuführen.
Abbildung 5. Brustbildgebung bei asbestbedingter Lungenerkrankung.
Eine posteroanteriore Röntgenaufnahme des Brustkorbs (A) zeigt eine Asbestose, die beide Lungen betrifft und als ILO-Kategorie 1/1 bewertet wurde, verbunden mit einer bilateralen Pleuraverdickung (offene Pfeile) und einer vage definierten Trübung (Pfeilspitzen) im linken Oberlappen. Beim HRCT-Scan (B) zeigte sich, dass dies eine dichte Masse (M) war, die an die Pleura angrenzte, und die transthorakale Nadelbiopsie ergab ein Adenokarzinom der Lunge. Auch auf dem CT-Scan (C) sind bei hoher Schwächung Pleuraplaques (Pfeilspitzen) sowie eine dünne krummlinige Opazität im Parenchym unter den Plaques mit interstitieller Anomalie in der Lunge zwischen der Opazität und der Pleura zu sehen. Quelle: Fraser et al. 1990
Lungenfunktionstests
Eine etablierte interstitielle Lungenfibrose aufgrund einer Asbestexposition ist, ebenso wie eine etablierte Lungenfibrose aufgrund anderer Ursachen, normalerweise, aber nicht immer, mit einem restriktiven Lungenfunktionsprofil verbunden (Becklake 1994). Zu seinen Merkmalen gehören reduzierte Lungenvolumina, insbesondere Vitalkapazität (VC) unter Beibehaltung des Verhältnisses von forciertem Exspirationsvolumen in 1 Sekunde zu forcierter Vitalkapazität (FEV1/FVC%), reduzierte Lungencompliance und gestörter Gasaustausch. Luftstrombegrenzung bei reduziertem FEV1/FVC kann jedoch auch als Reaktion auf eine staubige Arbeitsumgebung oder Zigarettenrauch vorhanden sein. In den frühen Stadien der Asbestose, wenn die pathologischen Veränderungen auf die peribronchioläre Fibrose beschränkt sind und noch bevor kleine unregelmäßige Trübungen auf dem Röntgenbild des Brustkorbs erkennbar sind, kann eine Beeinträchtigung der Tests, die eine Dysfunktion der kleinen Atemwege widerspiegeln, wie z. B. die maximale mittelexspiratorische Flussrate, das einzige Anzeichen sein von respiratorischer Dysfunktion. Auch die Reaktionen auf Belastungsstress können früh im Krankheitsverlauf beeinträchtigt sein, mit erhöhter Ventilation im Verhältnis zum Sauerstoffbedarf der Belastung (aufgrund erhöhter Atemfrequenz und flacher Atmung) und beeinträchtigter O2 Austausch. Mit fortschreitender Krankheit ist immer weniger Bewegung erforderlich, um O zu beeinträchtigen2 Austausch. Angesichts der Tatsache, dass der asbestexponierte Arbeiter Merkmale sowohl eines restriktiven als auch eines obstruktiven Lungenfunktionsprofils aufweisen kann, interpretiert der weise Arzt das Lungenfunktionsprofil des Asbestarbeiters als das, was es ist, als Maß für die Beeinträchtigung und nicht als Hilfsmittel dafür Diagnose. Die Lungenfunktionen, insbesondere die Vitalkapazität, stellen ein nützliches Instrument für die individuelle Nachsorge von Probanden oder in epidemiologischen Studien dar, beispielsweise nach Beendigung der Exposition, um den natürlichen Verlauf von Asbestose oder asbestbedingter Pleuraerkrankung zu überwachen.
Andere Labortests
Bronchoalveoläre Lavage wird zunehmend als klinisches Instrument bei der Untersuchung asbestbedingter Lungenerkrankungen eingesetzt:
- andere Diagnosen auszuschließen
- um die Aktivität der untersuchten Lungenreaktionen wie Fibrose oder zu beurteilen
- den Wirkstoff in Form von Asbestkörpern oder -fasern zu identifizieren.
Es wird auch verwendet, um Krankheitsmechanismen bei Menschen und Tieren zu untersuchen (Bégin, Cantin und Massé 1989). Als Maß für die Aktivität des Lungenfortsatzes wird die Aufnahme von Gallium-67 verwendet, als Faktoren wurden auch antinukleäre Antikörper (ANA) im Serum und Rheumafaktoren (RF) untersucht, die beide den immunologischen Status des Individuums widerspiegeln Beeinflussung des Krankheitsverlaufs und/oder die Berücksichtigung individueller Unterschiede in Reaktion auf scheinbar gleiche Expositionshöhe und -dosis.
Epidemiologie einschließlich Naturgeschichte
Die in arbeitsplatzbezogenen Erhebungen dokumentierte Prävalenz von Radioasbestose variiert erheblich, und wie zu erwarten war, beziehen sich diese Unterschiede eher auf Unterschiede in der Expositionsdauer und -intensität als auf Unterschiede zwischen den Arbeitsplätzen. Aber selbst wenn diese berücksichtigt werden, indem der Vergleich der Expositions-Wirkungs-Beziehungen mit jenen Studien eingeschränkt wird, in denen die Expositionsabschätzungen für jedes Kohortenmitglied individualisiert wurden und auf dem beruflichen Werdegang und industriellen Hygienemessungen basieren, sind deutliche faser- und prozessbezogene Gradienten offensichtlich (Liddell und Müller 1991). Beispielsweise resultierte eine Prävalenz von 5 % kleiner unregelmäßiger Trübungen (1/0 oder mehr nach der ILO-Klassifikation) aus einer kumulativen Exposition gegenüber etwa 1,000 Faserjahren bei Chrysotilbergarbeitern in Quebec, etwa 400 Faserjahren bei korsischen Chrysotilbergarbeitern und darunter 10 Faserjahre bei südafrikanischen und australischen Krokydolith-Bergleuten. Im Gegensatz dazu resultierte bei Textilarbeitern, die Quebec-Chrysotil ausgesetzt waren, eine Prävalenz von 5 % unregelmäßiger kleiner Trübungen aus einer kumulativen Exposition gegenüber weniger als 20 Faserjahren. Lungenstaubbelastungsstudien stimmen auch mit einem Fasergradienten zum Hervorrufen von Asbestose überein: Bei 29 Männern in pazifischen Werften mit Asbestose, die hauptsächlich mit Amosit-Exposition verbunden war, betrug die im Autopsiematerial gefundene durchschnittliche Lungenbelastung 10 Millionen Amosit-Fasern pro Gramm trockenem Lungengewebe im Vergleich zu einer durchschnittlichen Chrysotil-Belastung von 30 Millionen Fasern pro Gramm trockenem Lungengewebe bei 23 Chrysotil-Bergleuten und Müllern in Quebec (Becklake und Case 1994). Die Fasergrößenverteilung trägt zu diesen Unterschieden bei, erklärt sie jedoch nicht vollständig, was darauf hindeutet, dass andere anlagenspezifische Faktoren, einschließlich anderer Schadstoffe am Arbeitsplatz, eine Rolle spielen können.
Asbestose kann stabil bleiben oder fortschreiten, bildet sich aber wahrscheinlich nicht zurück. Die Progressionsraten nehmen mit dem Alter, mit der kumulativen Exposition und mit dem Ausmaß der bestehenden Erkrankung zu und treten mit größerer Wahrscheinlichkeit auf, wenn eine Exposition gegenüber Krokydolith bestand. Radiologische Asbestose kann sowohl fortschreiten als auch lange nach Beendigung der Exposition auftreten. Auch nach Beendigung der Exposition kann es zu einer Verschlechterung der Lungenfunktion kommen (Liddell und Miller 1991). Eine wichtige Frage (und eine, bei der die epidemiologischen Beweise nicht konsistent sind) ist, ob eine fortgesetzte Exposition die Wahrscheinlichkeit einer Progression erhöht, nachdem sich radiologische Veränderungen entwickelt haben (Browne 1994; Liddell und Miller 1991). In einigen Gerichtsbarkeiten, beispielsweise im Vereinigten Königreich, ist die Zahl der Fälle von Asbestose, die für eine Arbeitsunfallversicherung gemeldet werden, in den letzten Jahrzehnten zurückgegangen, was die Arbeitsplatzkontrollen widerspiegelt, die in den 1970er Jahren eingeführt wurden (Meredith und McDonald 1994). In anderen Ländern, zB in Deutschland (Gibbs, Valic und Browne 1994), steigen die Asbestoseraten weiter an. In den Vereinigten Staaten stiegen die altersbereinigten asbestbedingten Sterblichkeitsraten (basierend auf der Angabe von Asbestose in der Sterbeurkunde entweder als Todesursache oder als eine mitwirkende Rolle) für das Alter von 1+ Jahren von unter 1 pro Million im Jahr 1960 auf über 2.5 im Jahr 1986 und auf 3 im Jahr 1990 (US Dept. of Health and Human Services, 1994).
Diagnose und Fallmanagement
Die klinische Diagnose hängt ab von:
- das Vorliegen einer Krankheit festzustellen
- Feststellung, ob eine Exposition stattgefunden hat und
- zu beurteilen, ob die Exposition wahrscheinlich die Krankheit verursacht hat.
Das Thorax-Röntgenbild bleibt das wichtigste Instrument, um das Vorliegen einer Krankheit festzustellen, ergänzt durch HRCT, falls verfügbar, in Fällen, in denen Zweifel bestehen. Andere objektive Merkmale sind das Vorhandensein von basalem Knistern, während das Lungenfunktionsniveau, einschließlich körperlicher Herausforderung, nützlich ist, um eine Beeinträchtigung festzustellen, ein Schritt, der für die Kompensationsbewertung erforderlich ist. Da sich weder die Pathologie, radiologischen Veränderungen noch die Symptome und Lungenfunktionsveränderungen im Zusammenhang mit Asbestose aufgrund anderer Ursachen von denen im Zusammenhang mit interstitieller Lungenfibrose unterscheiden, ist die Feststellung einer Exposition der Schlüssel zur Diagnose. Darüber hinaus machen die vielen Verwendungen von Asbestprodukten, deren Inhalt dem Benutzer oft nicht bekannt ist, eine Expositionsgeschichte zu einer viel entmutigenderen Befragungsübung als bisher angenommen. Wenn die Expositionsanamnese unzureichend erscheint, kann die Identifizierung des Agens in biologischen Proben (Sputum, bronchoalveoläre Lavage und gegebenenfalls Biopsie) die Exposition bestätigen; Dosis in Form der Lungenbelastung kann quantitativ durch Autopsie oder in chirurgisch entfernten Lungen bestimmt werden. Der Nachweis einer Krankheitsaktivität (aus einem Gallium-67-Scan oder einer bronchoalveolären Lavage) kann bei der Einschätzung der Prognose hilfreich sein, einem Schlüsselproblem bei diesem irreversiblen Zustand. Selbst in Ermangelung konsistenter epidemiologischer Beweise dafür, dass die Progression verlangsamt wird, sobald die Exposition aufhört, kann eine solche Vorgehensweise umsichtig und sicherlich wünschenswert sein. Es ist jedoch keine leicht zu treffende oder zu empfehlende Entscheidung, insbesondere für ältere Arbeitnehmer mit geringen Möglichkeiten zur beruflichen Umschulung. Sicherlich sollte die Exposition an keinem Arbeitsplatz fortgesetzt werden, der nicht den derzeit zulässigen Expositionswerten entspricht. Die Kriterien für die Diagnose von Asbestose für epidemiologische Zwecke sind weniger anspruchsvoll, insbesondere für arbeitsplatzbezogene Querschnittsstudien, die diejenigen einschließen, die gesund genug sind, um am Arbeitsplatz zu sein. Diese behandeln normalerweise Fragen der Kausalität und verwenden häufig Marker, die auf eine minimale Erkrankung hinweisen, entweder basierend auf dem Lungenfunktionsniveau oder auf Veränderungen im Röntgenbild des Brustkorbs. Im Gegensatz dazu sind die Diagnosekriterien für medizinrechtliche Zwecke erheblich strenger und variieren je nach den rechtlichen Verwaltungssystemen, unter denen sie arbeiten, und variieren sowohl zwischen den Staaten innerhalb der Länder als auch zwischen den Ländern.
Asbestbedingte Pleuraerkrankung
Historische Perspektive
Frühe Beschreibungen der Asbestose erwähnen Fibrose der viszeralen Pleura als Teil des Krankheitsprozesses (siehe „Pathologie“, Seite 10.55). In den 1930er Jahren gab es auch Berichte über umschriebene Pleuraplaques, oft verkalkt, in der parietalen Pleura (die die Brustwand auskleidet und die Oberfläche des Zwerchfells bedeckt) und die bei Personen auftraten, die nicht beruflich, sondern umweltbedingt exponiert waren. Eine arbeitsplatzbezogene Studie einer deutschen Fabrik aus dem Jahr 1955 berichtete über eine 5%ige Prävalenz von Pleuraveränderungen auf dem Röntgenbild des Brustkorbs, wodurch die Aufmerksamkeit auf die Tatsache gelenkt wurde, dass eine Pleuraerkrankung die primäre, wenn nicht die einzige Manifestation einer Exposition sein könnte. Viszeroparietale Pleurareaktionen, einschließlich diffuser Pleurafibrose, gutartiger Pleuraerguss (erstmals in den 1960er Jahren berichtet) und abgerundete Atelektase (erstmals in den 1980er Jahren berichtet), werden heute alle als zusammenhängende Reaktionen betrachtet, die auf der Grundlage der Pathologie und wahrscheinlich der Pathogenese nützlich von Pleuraplaques unterschieden werden können , sowie klinische Merkmale und Präsentation. In Gerichtsbarkeiten, in denen die Prävalenz- und/oder Inzidenzraten von Asbestose zurückgehen, sind pleurale Manifestationen, die in Umfragen immer häufiger vorkommen, zunehmend die Grundlage für die Erkennung einer früheren Exposition und zunehmend der Grund dafür, dass eine Person einen Arzt aufsucht.
Pleuraplaques
Pleuraplaques sind glatte, erhabene, weiße, unregelmäßige Läsionen, die mit Mesothel bedeckt sind und sich auf der parietalen Pleura oder dem Zwerchfell befinden (Abbildung 6). Sie sind unterschiedlich groß, oft multipel und neigen mit zunehmendem Alter zur Verkalkung (Browne 1994). Nur ein kleiner Teil der bei der Autopsie entdeckten ist auf dem Thorax-Röntgenbild zu sehen, obwohl die meisten durch HRCT entdeckt werden können. In Abwesenheit einer Lungenfibrose können Pleuraplaques keine Symptome verursachen und können nur in Screening-Untersuchungen mit Röntgenaufnahmen des Brustkorbs nachgewiesen werden. Dennoch werden sie in Mitarbeiterbefragungen durchweg mit einer leichten, aber messbaren Beeinträchtigung der Lungenfunktion in Verbindung gebracht, hauptsächlich bei VC und FVC (Ernst und Zejda 1991). In radiologischen Erhebungen in den Vereinigten Staaten werden Raten von 1 % bei Männern ohne bekannte Exposition und 2.3 % bei Männern, einschließlich der städtischen Bevölkerung, mit beruflicher Exposition gemeldet. Die Raten sind auch in Gemeinden mit Asbestindustrien oder hohen Verbrauchsraten höher, während die Raten in einigen Arbeitskräften, wie Blecharbeitern, Isolatoren, Klempnern und Eisenbahnarbeitern, 50 % übersteigen können. In einer finnischen Autopsieuntersuchung von 1994 an 288 plötzlich verstorbenen Männern im Alter von 35 bis 69 Jahren wurden Pleuraplaques bei 58 % entdeckt und zeigten die Tendenz, mit dem Alter zuzunehmen, mit der Wahrscheinlichkeit einer Exposition (basierend auf der Anamnese) mit einer Konzentration von Asbestfasern im Lungengewebe und beim Rauchen (Karjalainen et al. 1994). Der ätiologische Anteil von Plaques, der einer Lungenstaubbelastung von 0.1 Millionen Fasern pro Gramm Lungengewebe zuzuschreiben ist, wurde auf 24 % geschätzt (dieser Wert wird als zu niedrig angesehen). Lungenstaubbelastungsstudien stimmen auch mit Fasergradienten in der Potenz zum Hervorrufen von Pleurareaktionen überein; Bei 103 Männern mit Amosit-Exposition in pazifischen Werften, alle mit Pleuraplaques, betrug die durchschnittliche Lungenlast bei der Autopsie 1.4 Millionen Fasern pro Gramm Lungengewebe, verglichen mit 15.5 und 75 Millionen Fasern pro Gramm Lungengewebe für Chrysotil bzw. Tremolit bei 63 Quebecer Chrysotil-Bergleute und Müller untersuchten auf die gleiche Weise (Becklake und Case 1994).
Abbildung 6. Asbestbedingte Pleuraerkrankung
Eine Zwerchfell-Pleura-Plaque (A) ist in einer Autopsieprobe als glatter, gut definierter Fibroseherd auf dem Zwerchfell eines Bauarbeiters mit zufälliger Exposition gegenüber Asbest und Asbestkörpern in der Lunge zu sehen. Viszerale Pleurafibrose (B) ist auf einem aufgeblasenen Autopsie-Lungenexemplar zu sehen und strahlt von zwei zentralen Herden auf der viszeralen Pleura der Lunge eines Bauarbeiters mit Asbestexposition aus, der auch mehrere parietale Pleuraplaques aufwies. Quelle: Fraser et al. 1990.
Viszeroparietale Pleurareaktionen
Obwohl die Pathologie und Pathogenese der verschiedenen Formen der viszeroparietalen Reaktion auf Asbestexposition mit ziemlicher Sicherheit miteinander zusammenhängen, unterscheiden sich ihre klinischen Manifestationen und wie sie zur Aufmerksamkeit gelangen. Akute exsudative Pleurareaktionen können in Form von Ergüssen bei Patienten auftreten, deren Lungen keine anderen asbestbedingten Erkrankungen aufweisen, oder als Exazerbation der Schwere und des Ausmaßes bestehender Pleurareaktionen. Solche Pleuraergüsse werden als gutartig bezeichnet, um sie von Ergüssen im Zusammenhang mit bösartigem Mesotheliom zu unterscheiden. Gutartige Pleuraergüsse treten typischerweise 10 bis 15 Jahre nach der ersten Exposition (oder nach begrenzter früherer Exposition) bei Personen zwischen 20 und 30 Jahren auf. Sie sind normalerweise vorübergehend, können aber wieder auftreten, können eine oder beide Seiten des Brustkorbs gleichzeitig oder nacheinander betreffen und können entweder still oder mit Symptomen wie Engegefühl in der Brust und/oder Pleuraschmerzen und Dyspnoe verbunden sein. Die Pleuraflüssigkeit enthält Leukozyten, oft Blut, und ist albuminreich; Es enthält nur selten Asbestkörper oder -fasern, die jedoch in Biopsiematerial des Rippenfells oder der darunter liegenden Lunge gefunden werden können. Die meisten gutartigen Pleuraergüsse verschwinden spontan, obwohl sich diese Ergüsse bei einem kleinen Teil der Patienten (in der Größenordnung von 10 % in einer Serie) zu einer diffusen Pleurafibrose entwickeln können (siehe Abbildung 6), mit oder ohne Entwicklung einer Lungenfibrose. Lokale Pleurareaktionen können sich auch in sich selbst zusammenfalten, Lungengewebe einfangen und gut definierte Läsionen verursachen, die als Pleura bezeichnet werden abgerundete Atelektase or Pseudotumor weil sie das radiologische Erscheinungsbild von Lungenkrebs haben können. Im Gegensatz zu pleuralen Plaques, die selten Symptome verursachen, sind viszeroparietale Pleurareaktionen in der Regel mit einer gewissen Atemnot sowie einer Beeinträchtigung der Lungenfunktion verbunden, insbesondere wenn eine Obliteration des costophrenischen Winkels vorliegt. Beispielsweise betrug in einer Studie das durchschnittliche FVC-Defizit 0.07 l bei Beteiligung der Thoraxwand und 0.50 l bei Beteiligung des costophrenischen Winkels (Ernst und Zejda in Liddell und Miller 1991). Wie bereits angedeutet, variieren die Verteilung und Determinanten von Pleurareaktionen erheblich zwischen den Belegschaften, wobei die Prävalenzraten steigen mit:
- geschätzte Verweildauer der Faser in der Lunge (gemessen als Zeit seit der ersten Exposition)
- Expositionen hauptsächlich gegenüber oder einschließlich Amphibol und
- möglicherweise zeitweilige Exposition angesichts der hohen Kontaminationsraten in Berufen, in denen Asbestmaterialien zeitweise verwendet werden, aber die Exposition wahrscheinlich stark ist.
Lungenkrebs
Historische Perspektive
In den 1930er Jahren wurde eine Reihe klinischer Fallberichte aus den Vereinigten Staaten, dem Vereinigten Königreich und Deutschland über Lungenkrebs (eine Krankheit, die damals viel seltener war als heute) bei Asbestarbeitern veröffentlicht, von denen die meisten auch an Asbestose unterschiedlichen Grades litten der Schwere. Weitere Beweise für den Zusammenhang zwischen den beiden Zuständen wurden im Jahresbericht des Chief Inspector of Factories Seiner Majestät von 1947 geliefert, in dem festgestellt wurde, dass Lungenkrebs bei 13.2% der männlichen Todesfälle aufgrund von Asbestose im Zeitraum von 1924 bis 1946 und in nur gemeldet wurde 1.3 % der männlichen Todesfälle werden auf Silikose zurückgeführt. Die erste Studie, die sich mit der Kausalhypothese befasste, war eine Kohortenmortalitätsstudie einer großen Asbest-Textilfabrik im Vereinigten Königreich (Doll 1955), eine der ersten derartigen arbeitsbezogenen Studien, und bis 1980 nach mindestens acht solcher Studien in ebenso vielen Belegschaften eine Expositions-Wirkungs-Beziehung bestätigt hatten, wurde die Assoziation allgemein als kausal akzeptiert (McDonald und McDonald in Antman und Aisner 1987).
Klinische Merkmale und Pathologie
In Ermangelung einer anderen assoziierten Asbesterkrankung unterscheiden sich die klinischen Merkmale und Kriterien für die Diagnose von asbestassoziiertem Lungenkrebs nicht von denen für Lungenkrebs, der nicht mit einer Asbestexposition verbunden ist. Ursprünglich galt asbestassoziierter Lungenkrebs als Narbenkrebs, ähnlich dem Lungenkrebs, der bei anderen Formen diffuser Lungenfibrose wie Sklerodermie auftritt. Merkmale, die diese Ansicht begünstigten, waren ihre Lage in den unteren Lungenlappen (wo die Asbestose normalerweise stärker ausgeprägt ist), ihre manchmal multizentrische Herkunft und ein Übergewicht von Adenokarzinomen in einigen Serien. In den meisten gemeldeten arbeitsplatzbezogenen Studien unterschied sich die Verteilung der Zelltypen jedoch nicht von der in Studien an nicht asbestexponierten Bevölkerungsgruppen, was die Ansicht stützt, dass Asbest selbst ein menschliches Karzinogen sein kann, eine Schlussfolgerung der Internationalen Agentur für Krebsforschung (Weltgesundheitsorganisation: Internationale Agentur für Krebsforschung 1982). Die meisten, aber nicht alle asbestbedingten Lungenkrebsarten treten in Verbindung mit radiologischer Asbestose auf (siehe unten).
Epidemiologie
Kohortenstudien bestätigen, dass das Lungenkrebsrisiko mit der Exposition zunimmt, obwohl die fraktionelle Anstiegsrate für jede Faser pro Milliliter pro Jahr variiert und sowohl mit dem Fasertyp als auch mit dem industriellen Prozess zusammenhängt (Health Effects Institute – Asbestos Research 1991). Beispielsweise lag der Anstieg hauptsächlich bei Chrysotil-Engagements im Bergbau, in der Mühle und bei der Herstellung von Reibungsprodukten zwischen etwa 0.01 und 0.17 % und bei der Textilherstellung zwischen 1.1 und 2.8 %, während es bei Engagements in Amosit-Dämmprodukten und einigen Zementprodukten zu gemischten Engagements kam Faser, wurden sogar Raten von 4.3 und 6.7 % verzeichnet (Nicholson 1991). Kohortenstudien an Asbestarbeitern bestätigen auch, dass das Krebsrisiko für Nichtraucher nachweisbar ist und dass das Risiko durch Zigarettenrauchen erhöht wird (eher multiplikativ als additiv) (McDonald und McDonald in Antman und Aisner 1987). Das relative Risiko für Lungenkrebs sinkt nach Beendigung der Exposition, obwohl der Rückgang langsamer zu sein scheint als nach Beendigung des Rauchens. Studien zur Lungenstaubbelastung stimmen auch mit einem Fasergradienten bei der Entstehung von Lungenkrebs überein; 32 Männer in pazifischen Werften mit hauptsächlich Amosit-Exposition hatten eine Lungenstaubbelastung von 1.1 Millionen Amositfasern pro Gramm trockenem Lungengewebe im Vergleich zu 36 Chrysotil-Bergleuten aus Quebec mit einer durchschnittlichen Lungenstaubbelastung von 13 Millionen Chrysotilfasern pro Gramm Lungengewebe (Becklake und Fall 1994).
Beziehung zur Asbestose
In der Autopsiestudie von 1955 über Todesursachen bei 102 Arbeitern, die in der oben erwähnten Asbest-Textilfabrik im Vereinigten Königreich beschäftigt waren (Doll 1955), wurde bei 18 Personen Lungenkrebs festgestellt, von denen 15 auch Asbestose hatten. Alle Probanden, bei denen beide Zustände festgestellt wurden, hatten vor 9, als nationale Vorschriften zur Asbeststaubbekämpfung eingeführt wurden, mindestens 1931 Jahre gearbeitet. Diese Beobachtungen deuteten darauf hin, dass mit abnehmender Exposition auch das konkurrierende Todesrisiko durch Asbestose abnahm und die Arbeiter lange genug lebten, um die Entwicklung von Krebs zu zeigen. In den meisten auf Arbeitskräften basierenden Studien weisen ältere Arbeitnehmer mit langjähriger Betriebszugehörigkeit einige pathologische Anzeichen von Asbestose (oder asbestbedingter Erkrankung der kleinen Atemwege) bei der Autopsie auf, obwohl dies möglicherweise minimal und auf der Röntgenaufnahme des Brustkorbs im Leben nicht nachweisbar ist (McDonald und McDonald in Antman und Aiser 1987). Mehrere, aber nicht alle Kohortenstudien stimmen mit der Ansicht überein, dass nicht alle exzessiven Lungenkrebsfälle in Bevölkerungsgruppen, die Asbest ausgesetzt sind, mit Asbestose zusammenhängen. Je nach Ort und Ablagerung der Fasern kann tatsächlich mehr als ein pathogenetischer Mechanismus für Lungenkrebs bei Personen verantwortlich sein, die Asbest ausgesetzt sind. Zum Beispiel wird angenommen, dass lange dünne Fasern, die bevorzugt an Atemwegsverzweigungen abgelagert werden, konzentriert werden und als Induktoren des Prozesses der Krebsentstehung durch Chromosomenschädigung wirken. Promotoren dieses Prozesses können eine fortgesetzte Exposition gegenüber Asbestfasern oder Tabakrauch sein (Lippman 1995). Solche Krebsarten sind eher Plattenepithelkarzinome. Im Gegensatz dazu kann in Lungen, die der Ort der Fibrose sind, die Krebsentstehung aus dem fibrotischen Prozess resultieren: solche Krebsarten sind eher Adenokarzinome.
Implikationen und Zurechenbarkeit
Während für exponierte Bevölkerungsgruppen Determinanten für ein erhöhtes Krebsrisiko abgeleitet werden können, ist dies nicht für die Zuordnung im Einzelfall möglich. Offensichtlich ist die Zuordnung zu einer Asbestexposition bei einer exponierten Person mit Asbestose, die nie geraucht hat, wahrscheinlicher und glaubwürdiger als bei einer exponierten Person ohne Asbestose, die raucht. Auch diese Wahrscheinlichkeit lässt sich nicht sinnvoll modellieren. Lungenstaubbelastungsmessungen können eine sorgfältige klinische Bewertung ergänzen, aber jeder Fall muss nach seinen Vorzügen bewertet werden (Becklake 1994).
Bösartiges Mesotheliom
Pathologie, Diagnose, Feststellung und klinische Merkmale
Bösartige Mesotheliome entstehen aus den serösen Körperhöhlen. Etwa zwei Drittel entstehen in der Pleura, etwa ein Fünftel im Peritoneum, während das Perikard und die Tunica vaginalis wesentlich seltener betroffen sind (McDonald und McDonald in Lidell und Miller 1991). Da Mesothelzellen pluripotent sind, können die histologischen Merkmale von Mesotheltumoren variieren; in den meisten Serien machen epitheliale, sarkomatöse und gemischte Formen etwa 50, 30 bzw. 10 % der Fälle aus. Die Diagnose dieses seltenen Tumors ist selbst in den Händen erfahrener Pathologen nicht einfach, und Pathologen des Mesotheliom-Panels bestätigen oft nur einen kleinen Prozentsatz, in einigen Studien weniger als 50 % der zur Überprüfung eingereichten Fälle. Eine Vielzahl von zytologischen und immunhistochemischen Techniken wurde entwickelt, um bei der Differenzierung des malignen Mesothelioms von den wichtigsten alternativen klinischen Diagnosen, nämlich sekundärem Krebs oder reaktiver Mesothelhyperplasie, zu helfen; dies bleibt ein aktives Forschungsfeld, in dem hohe Erwartungen, aber keine schlüssigen Ergebnisse erzielt werden (Jaurand, Bignon und Brochard 1993). Aus all diesen Gründen ist eine Fallerfassung für epidemiologische Erhebungen nicht ohne weiteres möglich und kann selbst auf der Grundlage von Krebsregistern unvollständig sein. Darüber hinaus ist eine Bestätigung durch Expertengremien anhand festgelegter pathologischer Kriterien erforderlich, um die Vergleichbarkeit der Registrierungskriterien zu gewährleisten.
Klinische Merkmale
Schmerz ist normalerweise das charakteristische Merkmal. Bei Pleuratumoren beginnt dies in der Brust und/oder den Schultern und kann schwerwiegend sein. Es folgt Atemnot, verbunden mit einem Pleuraerguss und/oder einer fortschreitenden Einkapselung der Lunge durch einen Tumor und Gewichtsverlust. Bei Peritonealtumoren gehen Bauchschmerzen meist mit Schwellungen einher. Bildgebungsmerkmale sind in Abbildung 7 dargestellt. Der klinische Verlauf ist normalerweise schnell und die mittleren Überlebenszeiten, sechs Monate in einem Bericht von 1973 und acht Monate in einem Bericht von 1993, haben sich in den letzten zwei Jahrzehnten trotz des größeren öffentlichen und medizinischen Bewusstseins kaum verändert führt oft zu einer früheren Diagnose und trotz Fortschritten bei Diagnosetechniken und einer Zunahme der Zahl von Behandlungsoptionen für Krebs.
Abbildung 7. Malignes Mesotheliom
Auf einem überpenetrierten Bruströntgen (A) als große Raumforderung in der Achselregion zu sehen. Beachte die damit einhergehende Volumenreduktion des rechten Hämothorax mit deutlich unregelmäßig knotiger Verdickung der Pleura der gesamten rechten Lunge. Der CT-Scan (B) bestätigt die ausgedehnte Pleuraverdickung, die die parietale und mediastinale Pleura (geschlossene Pfeile) in und um die Rippen umfasst. Quelle: Fraser et al. 1990
Epidemiologie
In den 15 Jahren, die auf den Bericht von 1960 über die Mesotheliom-Fallserie vom Nordwestkap, Südafrika (Wagner 1996) folgten, kam die internationale Bestätigung der Assoziation durch Berichte von anderen Fallserien aus Europa (Vereinigtes Königreich, Frankreich, Deutschland, Holland). , den Vereinigten Staaten (Illinois, Pennsylvania und New Jersey) und Australien sowie Fall-Kontroll-Studien aus dem Vereinigten Königreich (4 Städte), Europa (Italien, Schweden, Holland) und aus den Vereinigten Staaten und Kanada. Odds Ratios in diesen Studien reichten von 2 bis 9. Besonders in Europa war die Assoziation mit Werftberufen stark. Darüber hinaus deuten Studien zur proportionalen Mortalität in Asbest-exponierten Kohorten darauf hin, dass das Risiko sowohl mit dem Fasertyp als auch mit dem industriellen Prozess verbunden ist, wobei die auf Mesotheliom zurückzuführenden Raten von 0.3 % im Chrysotilbergbau bis 1 % in der Chrysotilherstellung reichen, verglichen mit 3.4 % bei Amphibolen Bergbau und Fertigung und bis zu 8.6 % für die Exposition gegenüber gemischten Fasern in der Isolierung (McDonald und McDonald in Liddell und Miller 1991). Ähnliche Fasergradienten zeigen sich in Kohortenmortalitätsstudien, die angesichts der kurzen Überlebenszeiten dieser Tumoren die Inzidenz angemessen widerspiegeln. Diese Studien zeigen auch längere Latenzzeiten, wenn die Exposition gegenüber Chrysotil im Vergleich zu Amphibolen erfolgte. Die geografische Variation der Inzidenz wurde anhand kanadischer alters- und geschlechtsspezifischer Raten für 1966 bis 1972 dokumentiert, um die erwarteten Raten zu berechnen (McDonald und McDonald in Liddell und Miller 1991); Ratenverhältnisse (tatsächlich beobachtete Werte über erwartet) waren 0.8 für die Vereinigten Staaten (1972), 1.1 für Schweden (1958 bis 1967), 1.3 für Finnland (1965 bis 1969), 1.7 für das Vereinigte Königreich (1967 bis 1968) und 2.1 für Niederlande (1969 bis 1971). Während technische Faktoren, einschließlich Ermittlungen, offensichtlich zu den aufgezeichneten Schwankungen beitragen können, deuten die Ergebnisse auf höhere Raten in Europa als in Nordamerika hin.
Zeittrends und geschlechtsspezifische Unterschiede bei der Inzidenz von Mesotheliom wurden als Maß für die gesundheitlichen Auswirkungen der Asbestexposition auf die Bevölkerung verwendet. Die besten Schätzungen für die Gesamtraten in den Industrieländern vor 1950 liegen unter 1.0 pro Million für Männer und Frauen (McDonald und McDonald in Jaurand und Bignon 1993). In der Folge stiegen die Raten bei Männern stetig und bei Frauen entweder gar nicht oder weniger stark an. Zum Beispiel wurden Gesamtquoten bei Männern und Frauen pro Million in den Vereinigten Staaten von 11.0 und unter 2.0 für 1982, 14.7 und 7.0 in Dänemark für 1975-80, 15.3 und 3.2 im Vereinigten Königreich für 1980-83 und 20.9 und 3.6 angegeben 1978 in den Niederlanden für 87-28.9. Höhere Raten bei Männern und Frauen, jedoch ohne jüngere Probanden, wurden für Krokydolithabbauländer gemeldet: 4.7 bzw. 2 in Australien (im Alter von 1986+) für 32.9 und 8.9 bzw. 1 für südafrikanische Weiße (im Alter von 1988+) für 1991 ( Health Effects Institute – Asbestos Research 20). Die steigenden Raten bei Männern spiegeln wahrscheinlich die berufliche Exposition wider, und wenn dies der Fall ist, sollten sie sich innerhalb der 30- bis 1970-jährigen „Inkubationszeit“ nach der Einführung von Arbeitsplatzkontrollen und der Verringerung der Expositionswerte an den meisten Arbeitsplätzen einpendeln oder verringern Industrieländer in den 1985er Jahren. In Ländern, in denen die Raten bei Frauen steigen, kann dieser Anstieg ihre zunehmende Beschäftigung mit Berufen mit Risikoexposition oder die zunehmende Umwelt- oder Innenraumverschmutzung der Stadtluft widerspiegeln (McDonald XNUMX).
Ätiologie
Umweltfaktoren sind eindeutig die Hauptdeterminanten des Mesotheliomrisikos, wobei Asbestexposition am wichtigsten ist, obwohl das Auftreten familiärer Cluster das Interesse an der potenziellen Rolle genetischer Faktoren aufrechterhält. Alle Arten von Asbestfasern wurden mit der Entstehung von Mesotheliom in Verbindung gebracht, einschließlich Anthophyllit zum ersten Mal in einem kürzlich erschienenen Bericht aus Finnland (Meurman, Pukkala und Hakama 1994). Es gibt jedoch zahlreiche Beweise aus Studien zur proportionalen und Kohortenmortalität und Lungenbelastungsstudien, die auf die Rolle eines Fasergradienten bei der Mesotheliomproduktion hindeuten, wobei das Risiko bei Expositionen hauptsächlich gegenüber Amphibolen oder Amphibol-Chrysotil-Mischungen höher ist als bei hauptsächlich Chrysotil Expositionen. Darüber hinaus gibt es Ratenunterschiede zwischen Arbeitskräften für die gleiche Faser bei anscheinend gleicher Expositionshöhe; diese müssen noch erklärt werden, obwohl die Fasergrößenverteilung ein wahrscheinlich beitragender Faktor ist.
Die Rolle von Tremolit wurde weithin diskutiert, eine Debatte, die durch den Nachweis seiner Biopersistenz in tierischem und menschlichem Lungengewebe im Vergleich zu Chrysotil ausgelöst wurde. Eine plausible Hypothese ist, dass die vielen kurzen Fasern, die die Atemwege und Alveolen der peripheren Lunge erreichen und dort abgelagert werden, zu den subpleuralen Lymphgefäßen transportiert werden, wo sie sich ansammeln; ihre Potenz bei der Mesotheliomproduktion hängt von ihrer Biopersistenz in Kontakt mit pleuralen Oberflächen ab (Lippmann 1995). In Studien am Menschen sind die Mesotheliomraten bei Bevölkerungsgruppen niedriger, die bei der Arbeit Chrysotil ausgesetzt waren, das relativ nicht mit Tremolit kontaminiert war (z. B. in simbabwischen Minen), im Vergleich zu denen, die Chrysotil ausgesetzt waren, das so kontaminiert war (z. B. in Minen in Quebec), und diese Ergebnisse haben wurden im Tierversuch repliziert (Lippmann 1995). Auch in einer multivariaten Analyse der Lungenfaserbelastung in Material aus einer kanadaweiten Mesotheliom-Fallkontrollstudie (McDonald et al. 1989) deuteten die Ergebnisse darauf hin, dass die meisten, wenn nicht alle Mesotheliome durch Tremolit-Lungenfaserbelastung erklärt werden könnten. Schließlich unterstützt eine neuere Analyse der Sterblichkeit in der Kohorte von über 10,000 Quebecer Chrysotil-Bergleuten und Müllern, die zwischen 1890 und 1920 geboren wurden und bis 1988 folgten (McDonald und McDonald 1995), diese Ansicht: In fast 7,300 Todesfällen waren die 37 Mesotheliom-Todesfälle in bestimmten Minen aus der Gegend von Thetford konzentriert, jedoch unterschied sich die Lungenbelastung von 88 Kohortenmitgliedern aus den beteiligten Minen nicht von der von Bergleuten aus anderen Minen in Bezug auf die Chrysotilfaserbelastung, sondern nur in Bezug auf die Tremolitbelastung (McDonald et al. 1993 ).
Die sogenannte Tremolit-Frage ist vielleicht die wichtigste der derzeit diskutierten wissenschaftlichen Fragen und hat auch Auswirkungen auf die öffentliche Gesundheit. Es muss auch auf die wichtige Tatsache hingewiesen werden, dass in allen Serien und Gerichtsbarkeiten ein bestimmter Anteil der Fälle ohne gemeldete Asbestexposition auftritt und dass Studien zur Lungenstaubbelastung nur in einigen dieser Fälle auf eine frühere umweltbedingte oder berufliche Exposition hinweisen. Andere berufliche Expositionen wurden mit der Mesotheliomproduktion in Verbindung gebracht, beispielsweise beim Abbau von Talk, Vermiculit und möglicherweise Glimmer, aber bei diesen enthielt das Erz entweder Tremolit oder andere Fasern (Bignon, Peto und Saracci 1989). Eine offene Suche nach anderen Expositionen, beruflich oder nicht beruflich, gegenüber anorganischen und organischen Fasern und anderen Mitteln, die mit der Entstehung von Mesotheliom in Verbindung gebracht werden können, sollte fortgesetzt werden.
Andere asbestbedingte Krankheiten
Chronische Atemwegserkrankung
Üblicherweise gehören zu dieser Rubrik chronische Bronchitis und chronisch obstruktive Lungenerkrankung (COPD), die beide klinisch diagnostiziert werden können, und Emphyseme, die bis vor kurzem nur durch pathologische Untersuchung der bei der Autopsie oder anderweitig entfernten Lungen diagnostiziert wurden (Becklake 1992). Eine Hauptursache ist das Rauchen, und in den letzten Jahrzehnten hat die Mortalität und Morbidität aufgrund chronischer Atemwegserkrankungen in den meisten Industrieländern zugenommen. Mit dem Rückgang der Pneumokoniose in vielen Arbeitnehmern sind jedoch Hinweise aufgetaucht, die eine berufsbedingte Exposition mit der Entstehung chronischer Atemwegserkrankungen in Verbindung bringen, nachdem die dominierende Rolle des Rauchens berücksichtigt wurde. Es wurde gezeigt, dass alle Formen chronischer Atemwegserkrankungen mit der Arbeit in einer Vielzahl von staubigen Berufen verbunden sind, einschließlich jener Berufe, in denen ein wichtiger Bestandteil des Staubs, der den Arbeitsplatz kontaminiert, Asbest war (Ernst und Zejda in Liddell und Miller 1991). Es wird angenommen, dass die Gesamtschadstoffbelastung und nicht die Exposition gegenüber einem seiner besonderen Bestandteile, in diesem Fall Asbeststaub, impliziert ist, ähnlich wie die Wirkung des Rauchens auf chronische Atemwegserkrankungen betrachtet wird, d.h. in Bezug auf Gesamtexpositionsbelastung (z. B. als Packungsjahre), keine Exposition gegenüber einem der über 4,000 Bestandteile des Tabakrauchs. (Siehe an anderer Stelle in diesem Band eine weitere Erörterung der Beziehung zwischen beruflicher Exposition und chronischen Atemwegserkrankungen).
Andere Krebsarten
In mehreren der früheren Kohortenstudien mit Asbest-exponierten Arbeitern lag die auf alle Krebsarten zurückzuführende Sterblichkeit höher als erwartet, basierend auf nationalen oder regionalen Vitalstatistiken. Während Lungenkrebs den größten Teil des Überschusses ausmachte, waren andere beteiligte Krebsarten Magen-Darm-Krebs, Kehlkopfkrebs und Eierstockkrebs, in dieser Reihenfolge der Häufigkeit. Bei Magen-Darm-Krebs (einschließlich solcher, die die Speiseröhre, den Magen, den Dickdarm und das Rektum betreffen) wird angenommen, dass die relevante Exposition in Berufskohorten durch das Verschlucken von asbestbeladenem Sputum erfolgt, das aus den großen Atemwegen in die Lunge und in die Lunge gelangt früher (bevor Schutzmaßnahmen gegen die Exposition an Kantinen getroffen wurden) direkte Kontamination von Lebensmitteln an Arbeitsplätzen, die keine von den Arbeitsbereichen von Werken und Fabriken getrennten Kantinenbereiche hatten. Es kann auch zu einem retrograden Fluss über den Ductus thoracicus aus Lymphknoten kommen, die die Lunge entleeren (siehe „Verbleib inhalierter Fasern“, Seite 10.54). Da der Zusammenhang in den verschiedenen untersuchten Kohorten widersprüchlich war und weil Expositions-Wirkungs-Beziehungen nicht immer gesehen wurden, gab es eine Zurückhaltung, den Beweis für den Zusammenhang zwischen beruflicher Exposition und Asbestexposition als kausal zu akzeptieren (Doll und Peto 1987; Liddell und Miller 1991).
Kehlkopfkrebs ist viel seltener als Magen-Darm- oder Lungenkrebs. Bereits in den 1970er Jahren gab es Berichte über einen Zusammenhang zwischen Kehlkopfkrebs und Asbestexposition. Wie Lungenkrebs ist das Rauchen ein Hauptrisikofaktor und eine Ursache für Kehlkopfkrebs. Kehlkopfkrebs ist auch stark mit Alkoholkonsum verbunden. Angesichts der Lage des Kehlkopfes (ein Organ, das allen eingeatmeten Schadstoffen ausgesetzt ist, denen die Lunge ausgesetzt ist) und der Tatsache, dass er von demselben Epithel ausgekleidet ist, das die großen Bronchien auskleidet, ist es sicherlich biologisch plausibel, dass Kehlkopfkrebs vorliegt tritt als Folge einer Asbestexposition auf. Die bisher verfügbaren Gesamtbeweise sind jedoch widersprüchlich, selbst aus großen Kohortenstudien wie den Chrysotil-Bergleuten in Quebec und Balangero (Italien), möglicherweise weil es sich um einen seltenen Krebs handelt und es immer noch Widerwillen gibt, den Zusammenhang als kausal anzusehen (Liddell und Miller 1991) trotz seiner biologischen Plausibilität. Krebs der Eierstöcke wurde in drei Kohortenstudien überproportional gemeldet (WHO 1989). Fehldiagnosen, insbesondere als Peritonealmesotheliom, können die meisten Fälle erklären (Doll und Peto 1987).
Prävention, Überwachung und Bewertung
Historische und aktuelle Ansätze
Die Prävention von Pneumokoniose, einschließlich Asbestose, erfolgt traditionell durch:
- Technik und Arbeitspraktiken, um die Faserkonzentrationen in der Luft so niedrig wie möglich zu halten oder zumindest den zulässigen Expositionswerten zu entsprechen, die normalerweise durch Gesetze oder Vorschriften festgelegt werden
- Überwachung, die durchgeführt wird, um Trends von Krankheitsmarkern in exponierten Populationen aufzuzeichnen und die Ergebnisse von Kontrollmaßnahmen zu überwachen
- Aufklärung und Produktkennzeichnung mit dem Ziel, Arbeitnehmern und der breiten Öffentlichkeit dabei zu helfen, eine nichtberufliche Exposition zu vermeiden.
Die zulässigen Belastungswerte waren ursprünglich auf die Bekämpfung von Asbestose ausgerichtet und basierten auf industriellen Hygienemessungen in Millionen Partikeln pro Kubikfuß, die mit den gleichen Methoden erhoben wurden, die auch für die Bekämpfung von Silikose verwendet wurden. Mit der Verlagerung des biologischen Fokus auf Fasern, insbesondere lange, dünne, als Ursache der Asbestose, wurden Methoden entwickelt, die für ihre Identifizierung und Messung in Luft besser geeignet sind, und angesichts dieser Methoden der Fokus auf den häufiger vorkommenden kurzen Fasern, die am meisten kontaminieren Arbeitsplätze wurden minimiert. Die Aspektverhältnisse (Länge zu Durchmesser) für die meisten Partikel von gemahlenem Chrysotilasbest fallen in den Bereich von 5:1 bis 20:1 und gehen bis zu 50:1, im Gegensatz zu den meisten Partikeln von gemahlenem Amphibolasbest (einschließlich Spaltfragmenten), deren Werte fallen unter 3:1. Die Einführung des Membranfilters zur Faserzählung von Luftproben führte zu einer willkürlichen arbeitshygienischen und medizinischen Definition einer Faser als Partikel mit einer Länge von mindestens 5 μm, einer Dicke von 3 μm oder weniger und einem Verhältnis von Länge zu Breite von mindestens 3:1 . Diese Definition, die für viele Studien zu Expositions-Wirkungs-Beziehungen verwendet wird, bildet die wissenschaftliche Grundlage für die Festlegung von Umweltnormen.
Beispielsweise wurde es auf einer von der Weltgesundheitsorganisation (1989) gesponserten Tagung verwendet, um Grenzwerte für die Exposition am Arbeitsplatz vorzuschlagen, und wurde von Behörden wie der US-Behörde für Sicherheit und Gesundheit am Arbeitsplatz übernommen; sie wird hauptsächlich aus Gründen der Vergleichbarkeit beibehalten. Das WHO-Treffen unter dem Vorsitz von Sir Richard Doll erkannte zwar an, dass die Grenzwerte für die berufliche Exposition in jedem Land nur von der zuständigen nationalen Stelle festgelegt werden können, empfahl jedoch, dass Länder mit hohen Grenzwerten dringend Maßnahmen ergreifen sollten, um die berufliche Exposition für einen einzelnen Arbeitnehmer zu senken 2 f/ml (achtstündiger zeitgewichteter Durchschnitt) und dass alle Länder so schnell wie möglich auf 1 f/ml (achtstündiger zeitgewichteter Durchschnitt) umsteigen sollten, falls sie dies noch nicht getan haben. Mit dem Rückgang der Asbestoseraten in einigen Industrieländern und der Besorgnis über asbestbedingte Krebserkrankungen in allen hat sich die Aufmerksamkeit nun darauf verlagert, festzustellen, ob die gleichen Faserparameter – d. h. mindestens 5 mm lang, 3 mm oder weniger dick und mit einer Länge – vorhanden sind Breitenverhältnis von mindestens 3:1 – sind ebenfalls zur Kontrolle der Karzinogenese geeignet (Browne 1994). Eine aktuelle Theorie zur Karzinogenese von Asbest geht sowohl von kurzen als auch von langen Fasern aus (Lippmann 1995). Darüber hinaus könnte angesichts der Beweise für einen Fasergradienten bei der Mesotheliom- und Lungenkrebsproduktion und in geringerem Maße für die Asbestoseproduktion ein Argument für zulässige Expositionsniveaus unter Berücksichtigung des Fasertyps vorgebracht werden. Einige Länder haben das Problem angegangen, indem sie die Verwendung (und damit den Import) von Krokydolith verboten und strengere Expositionsgrenzen für Amosit festgelegt haben, nämlich 0.1 f/l (McDonald und McDonald 1987).
Expositionsniveaus am Arbeitsplatz
Zulässige Expositionsniveaus verkörpern die Hypothese, basierend auf allen verfügbaren Beweisen, dass die menschliche Gesundheit erhalten bleibt, wenn die Exposition innerhalb dieser Grenzen gehalten wird. Eine Überarbeitung der zulässigen Expositionsniveaus geht, wenn sie auftritt, ausnahmslos in Richtung einer strengeren Prüfung (wie im vorstehenden Absatz beschrieben). Dennoch kommt es trotz guter Einhaltung von Arbeitsplatzkontrollen immer wieder zu Krankheitsfällen aufgrund persönlicher Anfälligkeit (z. B. überdurchschnittliche Faserrückhalteraten) oder wegen Versagens von Arbeitsplatzkontrollen für bestimmte Tätigkeiten oder Prozesse. Technische Kontrollen, verbesserte Arbeitsplatzpraktiken und die Verwendung von Ersatzstoffen, die an anderer Stelle in diesem Kapitel beschrieben werden, wurden international (Gibbs, Valic und Browne 1994) in größeren Betrieben durch Industrie-, Gewerkschafts- und andere Initiativen eingeführt. Beispielsweise wurde laut einer weltweiten Branchenübersicht von 1986 die Einhaltung des derzeit empfohlenen Standards von 1 f/ml an 83 % der Produktionsstandorte (Minen und Mühlen) mit 13,499 Arbeitern in 6 Ländern erreicht; in 96 % von 167 Zementfabriken, die in 23 Ländern tätig sind; in 71 % von 40 Textilfabriken mit über 2,000 Beschäftigten in 7 Ländern; und in 97 % von 64 Fabriken, die Reibungsmaterialien herstellen, mit 10,190 Arbeitern in 10 Ländern (Bouige 1990). Ein nicht unerheblicher Teil dieser Arbeitsplätze entspricht jedoch noch immer nicht den Vorschriften, nicht alle Herstellerländer haben an dieser Umfrage teilgenommen, und der erwartete gesundheitliche Nutzen ist nur in einigen nationalen Statistiken ersichtlich, in anderen nicht („Diagnose und Fallmanagement“, Seite 10.57). Die Kontrolle von Abbruchprozessen und kleinen Unternehmen, die Asbest verwenden, ist selbst in vielen Industrieländern nach wie vor wenig erfolgreich.
Überwachung
Die Röntgenaufnahme des Brustkorbs ist das wichtigste Instrument für die Asbestoseüberwachung, Krebsregister und nationale Statistiken für asbestbedingte Krebserkrankungen. Eine lobenswerte Initiative zur internationalen Überwachung des Bergbaus, Tunnelbaus und Steinbruchs, die von der ILO durch freiwillige Berichterstattung von Regierungsquellen durchgeführt wird, konzentriert sich auf den Kohle- und Hartgesteinbergbau, könnte aber auch Asbest umfassen. Leider war die Umsetzung dürftig, da der letzte Bericht, der auf Daten für 1973-77 basierte, 1985 veröffentlicht wurde (ILO 1985). Mehrere Länder geben nationale Mortalitäts- und Morbiditätsdaten heraus, ein ausgezeichnetes Beispiel ist der Work-related Lung Disease Surveillance Report für die Vereinigten Staaten, ein Bericht, auf den oben Bezug genommen wurde (USDHSS 1994). Solche Berichte liefern Informationen, um Trends zu interpretieren und die Auswirkungen von Kontrollniveaus auf nationaler Ebene zu bewerten. Größere Branchen sollten (und viele tun dies) ihre eigenen Überwachungsstatistiken führen, ebenso wie einige Gewerkschaften. Die Überwachung kleinerer Industriezweige kann spezifische Studien in angemessenen Abständen erfordern. Andere Informationsquellen umfassen Programme wie das Surveillance of Work-related Respiratory Diseases (SWORD) im Vereinigten Königreich, das regelmäßige Berichte von einer Stichprobe von Brust- und Arbeitsmedizinern des Landes (Meredith und McDonald 1994) und Berichte von Vergütungsgremien sammelt (die jedoch häufig keine Informationen über gefährdete Arbeitnehmer enthalten).
Produktkennzeichnung, Aufklärung und die Datenautobahn
Die obligatorische Produktkennzeichnung zusammen mit der Aufklärung der Arbeitnehmer und der breiten Öffentlichkeit sind wirksame Instrumente der Prävention. Während dies in der Vergangenheit im Rahmen von Arbeitnehmerorganisationen, Betriebsräten und gewerkschaftlichen Bildungsprogrammen geschah, könnten künftige Ansätze elektronische Autobahnen nutzen, um Datenbanken zu Gesundheit und Sicherheit in Toxikologie und Medizin verfügbar zu machen.
Exposition in Gebäuden und aus der Wasserversorgung
1988 wurde vom US-Kongress (Health Effects Institute – Asbestos Research 1991) eine Überprüfung möglicher Gesundheitsrisiken im Zusammenhang mit der Arbeit in Gebäuden angeordnet, die unter Verwendung asbesthaltiger Materialien errichtet wurden. Die Ergebnisse einer großen Anzahl von Studien zur Probenahme in Innenräumen aus Europa, den Vereinigten Staaten und Kanada wurden in Risikoabschätzungen verwendet. Das lebenslange Risiko für einen vorzeitigen Krebstod wurde auf 1 pro Million für diejenigen geschätzt, die 15 Jahre lang in Schulen exponiert waren (für geschätzte Expositionsniveaus im Bereich von 0005 bis 005 f/ml) und 4 pro Million für diejenigen, die 20 Jahre lang in Schulen exponiert waren Bürogebäude (für geschätzte Expositionswerte im Bereich von 0002 bis 002 f/ml). Zum Vergleich: Das Risiko einer berufsbedingten Exposition gegenüber 0.1 f/ml (dh in Übereinstimmung mit dem zulässigen Expositionsgrenzwert, der von der US-amerikanischen Arbeitsschutzbehörde vorgeschlagen wurde) für 20 Jahre wurde auf 2,000 pro Million Exponierter geschätzt. Trinkwassermessungen in städtischen Gemeinden zeigen beträchtliche Schwankungen, von nicht nachweisbaren Werten bis hin zu hohen Werten von 0.7 Millionen f/l in Connecticut, USA, bis zu Werten von 1.1 Millionen bis 1.3 Milliarden f/l in den Bergbaugebieten von Quebec (Bignon, Peto und Saracci 1989). Eine gewisse Verunreinigung kann auch von den Asbestzementrohren ausgehen, die die meisten städtischen Wassernetze der Welt bedienen müssen. Eine Arbeitsgruppe, die die Beweise 1987 überprüfte, schloss jedoch die potenzielle damit verbundene Gefahr nicht aus, betrachtete die mit der Einnahme von Asbest verbundenen Gesundheitsrisiken jedoch nicht als „eine der dringendsten Gefahren für die öffentliche Gesundheit“ (USDHHS 1987), eine Ansicht, die mit übereinstimmt die abschließenden Bemerkungen in einer Monographie der IARC (WHO) über die nichtberufliche Exposition gegenüber Mineralfasern (Bignon, Peto und Saracci 1989).
Asbest und andere Fasern im 21. Jahrhundert
Die erste Hälfte des 1964. Jahrhunderts war gekennzeichnet durch das, was man als grobe Vernachlässigung asbestbedingter Krankheiten bezeichnen könnte. Vor dem Zweiten Weltkrieg sind die Gründe dafür nicht klar; die wissenschaftliche Grundlage für die Kontrolle war da, aber vielleicht nicht der Wille und nicht die Militanz der Arbeiter. Während des Krieges gab es andere nationale und internationale Prioritäten, und nach dem Krieg überwog der Urbanisierungsdruck einer schnell wachsenden Weltbevölkerung, und vielleicht lenkte die Faszination im Industriezeitalter von der Vielseitigkeit des „magischen“ Minerals die Aufmerksamkeit von seinen Gefahren ab . Nach der ersten Internationalen Konferenz über die biologischen Auswirkungen von Asbest im Jahr 1965 (Selikoff und Churg XNUMX) wurden asbestbedingte Krankheiten zu einer Ursache célèbre, nicht nur aus eigenen Gründen, sondern auch, weil es eine Zeit der Auseinandersetzung zwischen Arbeitgebern und Arbeitnehmern um die Rechte der Arbeitnehmer auf Wissen über Gefahren am Arbeitsplatz, Gesundheitsschutz und faire Entschädigung bei Verletzung oder Krankheit markierte. In Ländern mit verschuldensunabhängiger Arbeitsunfallversicherung wurden asbestbedingte Erkrankungen insgesamt fair anerkannt und behandelt. In Ländern, in denen Produkthaftungs- und Sammelklagen üblicher waren, wurden einigen betroffenen Arbeitnehmern (und ihren Anwälten) große Entschädigungen zugesprochen, während andere mittellos und ohne Unterstützung zurückblieben. Während der Bedarf an Fasern in modernen Gesellschaften wahrscheinlich nicht abnehmen wird, kann sich die Rolle der Mineralfasern gegenüber anderen Fasern ändern. Sowohl innerhalb als auch zwischen den Ländern hat es bereits eine Nutzungsverschiebung gegeben (siehe „Andere Expositionsquellen“, Seite 10.53). Obwohl die Technologie vorhanden ist, um die Exposition am Arbeitsplatz zu verringern, gibt es noch Arbeitsplätze, an denen sie nicht angewendet wurde. Angesichts des derzeitigen Wissensstands, der internationalen Kommunikation und Produktkennzeichnung sowie der Arbeitnehmerausbildung und des Engagements der Industrie sollte es möglich sein, dieses Mineral zur Bereitstellung billiger und langlebiger Produkte für den Einsatz im Bauwesen und in der Wasservernetzung auf internationaler Basis ohne Risiko für den Benutzer zu verwenden. Arbeiter, Hersteller oder Bergmann oder für die breite Öffentlichkeit.
HAFTUNGSAUSSCHLUSS: Die ILO übernimmt keine Verantwortung für auf diesem Webportal präsentierte Inhalte, die in einer anderen Sprache als Englisch präsentiert werden, der Sprache, die für die Erstproduktion und Peer-Review von Originalinhalten verwendet wird. Bestimmte Statistiken wurden seitdem nicht aktualisiert die Produktion der 4. Auflage der Encyclopaedia (1998)."