3.2. Potentiometrische Bestimmung von Acetylsalicylsäure
3.2. Potentiometrische Bestimmung von Acetylsalicylsäure
3.2. Potentiometrische Bestimmung von Acetylsalicylsäure
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 1 <strong>von</strong> 41<br />
<strong>Bestimmung</strong> <strong>von</strong><br />
<strong>Acetylsalicylsäure</strong> in<br />
Schmerzmitteln<br />
Gruppe 3: Name entfernt<br />
Name entfernt<br />
Christopher Gallian<br />
Name entfernt
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 2 <strong>von</strong> 41<br />
1. Die <strong>Acetylsalicylsäure</strong><br />
1.1. Physikalische und chemische Daten zur <strong>Acetylsalicylsäure</strong><br />
Synonym:<br />
Srukturformel:<br />
Gefahrensymbol:<br />
Allgemeine Summenformel:<br />
Molare Masse:<br />
Dichte:<br />
pH bei 2,5 g/l<br />
≈ 0,014 mol/l<br />
Schmelzpunkt:<br />
Siedepunkt:<br />
Thermische Zersetzung:<br />
Zündtemperatur:<br />
LD50 oral Ratte:<br />
LD50 dermal Kanninchen:<br />
Preis pro kg:<br />
R-Sätze:<br />
2-Acetoxybenzoesäure<br />
Xn<br />
C9H8O4<br />
180,15 g/mol<br />
1,38 g/cm 3<br />
3,5<br />
136 °C<br />
250 °C<br />
140 °C<br />
500 °C<br />
200 mg/kg<br />
7940 mg/kg<br />
30 Euro (MERK)<br />
R22 - Gesundheitsschädlich beim Verschlucken.<br />
weitere Eigenschafte: fest, farblos, fast geruchslos<br />
physiologische Eigenschaften: schmerzstillend, fiebersenkend, blutverdünnend
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 3 <strong>von</strong> 41<br />
1.2. Geschichte der <strong>Acetylsalicylsäure</strong><br />
Die Synthese <strong>von</strong> <strong>Acetylsalicylsäure</strong> erfolgt durch Acetylierung <strong>von</strong> Salicylsäure mit<br />
Essigsäureanhydrid. Salicylsäure wirkt wie die <strong>Acetylsalicylsäure</strong> auch<br />
Schmerzstillend. Einige Pflanzen wie die Teebeere und die Silberweide enthalten<br />
Salicylsäure. Deren Schmerzstillende Wirkung war schon tausende <strong>von</strong> Jahren bei<br />
Naturvölkern und Hochkulturen bekannt. 1828 ging man dem schmerzstillenden<br />
Wirkstoff der Pflanzen auf den Grund und extrahierte Salicin, welches in<br />
Salicylsäure gespalten werden konnte. 1859 wurde die Struktur und eine Synthese<br />
für die Salicylsäure eingeführt. Nun konnte man sie als Schmerzstillenden Wirkstoff<br />
in größeren Mengen herstellen und Vermarkten. Die Salicylsäure besitzt jedoch<br />
einen widerwärtigen Geschmack und verursacht starke Reizungen des Magens. Sie<br />
war deshalb nicht sehr beliebt und nur bedingt einsetzbar. Von 1896 -1899 wurde bei<br />
der Firma Bayer ein verfahren entwickelt um die die Salicylsäure verträglicher zu<br />
machen deren Wirkung jedoch beizubehalten. Das Resultat war die<br />
<strong>Acetylsalicylsäure</strong>, welche dann um 1899 in Pulver- und später in Tablettenform als<br />
Aspirin <strong>von</strong> Bayer vermarktet wurde.<br />
1.3. Bedeutung der <strong>Acetylsalicylsäure</strong> als Arzneimittel<br />
Es gibt mehrere hundert verschiedene Arzneimittel bei denen <strong>Acetylsalicylsäure</strong> als<br />
Hauptbestandteil enthalten ist. Das <strong>von</strong> Bayer entwickelte klassische Aspirin enthält<br />
ausschließlich <strong>Acetylsalicylsäure</strong> als Wirkstoff. Aspirin wirkt im menschlichen<br />
Organismus schmerzstillend, blutverdünnend und fiebersenkend.<br />
1.4. Zusammensetzung der Proben<br />
Probe: Aspirin<br />
Zusammensetzung: 100 mg / 300 mg <strong>Acetylsalicylsäure</strong><br />
weitere Bestandteile: Cellulosepulver, Maisstärke<br />
Probe: Godamed<br />
Zusammensetzung: 500 mg <strong>Acetylsalicylsäure</strong><br />
250 mg Glycin<br />
weitere Bestandteile: Aromastoffe, Cellulosepulver, Maisstärke,<br />
Saccharin-Natrium<br />
Probe: Melabon<br />
Zusammensetzung: 250 mg <strong>Acetylsalicylsäure</strong><br />
250 mg Paracetamol<br />
50 mg Coffein<br />
weitere Bestandteile: Siliciumdioxid, Maisstärke, Cellulose,<br />
Poly(0-carboxylmethyl)amylopektin-Natriumsalz,<br />
Stearinsäure, Talkum, Povidon
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 4 <strong>von</strong> 41<br />
Probe: Neuralgin<br />
Zusammensetzung: 250 mg <strong>Acetylsalicylsäure</strong><br />
200 mg Paracetamol<br />
50 mg Coffein<br />
weitere Bestandteile: Aluminiumoxid, mikrokristalline Cellulose, Maisstärke,<br />
hydriertes Rizinusöl<br />
2. Photometrische <strong>Bestimmung</strong><br />
2.1. Theoretische Grundlagen der Photometrie:<br />
2.1.1. Photometrie<br />
Als Photometrie bezeichnet man die Konzentrationsbestimmung einer Substanz,<br />
indem gemessen wird, wie sie die Intensität elektromagnetischer Strahlung<br />
schwächt. Der Begriff Photometrie ist auf den UV/VIS-Bereich und geringe<br />
Konzentrationsbereich beschränkt.<br />
2.1.2. Photometer<br />
Einstrahlmessverfahren<br />
Die Lichtquelle sendet einen Lichtstrahl durch das zu messende Medium in der<br />
Messzelle , und die Photozelle misst die Intensität des verbleibenden Lichts. Im<br />
Verstärker wird das elektrische Signal verstärkt und als Messwert ausgegeben.<br />
Das Ziel der Messung ist die Erfassung der Abschwächung der Lichtintensität durch<br />
die in der Messzelle enthaltene Substanz.<br />
2.1.3. Absorption<br />
Abschwächung der Strahlungsleistung beim Durchgang einer optischen Strahlung<br />
durch ein klares Medium. Durchstrahlt man eine Probe mit Licht einer geeigneten<br />
Wellenlänge, so wird ein Teil der Energie an die Moleküle übertragen, so dass der<br />
austretende Strahl eine kleinere Leistung aufweist als der eintretende
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 5 <strong>von</strong> 41<br />
2.1.4. Transmission<br />
Die Transmission bei einer bestimmten Wellenlänge ist das Verhältnis der<br />
Lichtintensitäten am Austritt I und am Eintritt I0 in der Messzelle.<br />
Transmission<br />
I<br />
T =<br />
I<br />
0<br />
Es müssen auch die an den Messzellenfenstern auftretenden Reflexionsverluste<br />
eliminiert werden. Dies geschieht in der Praxis durch Vergleich mit einer Messung<br />
des Trägermediums ohne absorbierendes Produkt (Blindprobe).<br />
2.1.5. Lambert-Beer'sches Gesetz<br />
Nach den beiden Wissenschaftern Johann Heinrich Lambert (1728-1777) und August<br />
Beer (1825-1863) benannter Zusammenhang zwischen der Extinktion E, der<br />
durchquerten Schichtdicke d und der Konzentration c des absorbierenden Stoffes:<br />
E = logT<br />
E = ε ⋅c<br />
⋅ d<br />
E: Extinktion<br />
T: Transmission<br />
ε : molarer Extinktionskoeffizient<br />
d: Schichtdicke<br />
Wobei c in mol/l und d in cm angegeben werden. Der Proportionalitätsfaktor heißt<br />
spektraler molarer Extinktionskoeffizient und ist eine stoffspezifische Funktion der<br />
Wellenlänge.<br />
2.1.6. Konzentrationsmessung<br />
Da die Extinktion E der dekadische Logarithmus der Transmission T ist, lässt sich E<br />
mit Hilfe einer Photozelle messen. Im geeigneten Konzentrationsbereich und bei<br />
Verwendung <strong>von</strong> monochromatischem Licht ist das Lambert-Beer'sche Gesetz mit<br />
hoher Genauigkeit erfüllt. Damit kann durch Messung der Extinktion E die<br />
Konzentration c eines gelösten Stoffes in Flüssigkeiten und Gasen bestimmt werden.<br />
2.1.7. Aufbau eines Photometers<br />
Ein Photometer besteht aus eine Lichtquelle(Lampe), Monochromator,<br />
Probebehälter(Küvette) , Detektor, Verstärker, Schreiber(Drucker, PC)<br />
2.1.8. Monochromatisches Licht<br />
Licht <strong>von</strong> nur einer Wellenlänge (Licht weist nur eine einzige Energie auf)
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 6 <strong>von</strong> 41<br />
Erzeugen <strong>von</strong> monochromatischem Licht:<br />
a. Durch diskontinuierliches Licht und Interferenzfilter<br />
Vorteil: Die Wellenlänge, die man herstellt, ist absolut konstant und reproduzierbar.<br />
Nachteil: Beschränkung auf die Wellenlänge des Elements, das in der Lampe ist.<br />
b. Durch kontinuierliches Licht und Monochromator<br />
Vorteil: Wellenlängenbereich, in dem alle Wellenlängen enthalten sind.<br />
Nachteil: Das monochromatische Licht ist ungenau (λ1 + λ2)<br />
2.1.9. Funktionsprinzip des Photometers<br />
Eine Strahlungsquelle sendet ultraviolettes (UV) und sichtbares Licht (VIS) aus. Die<br />
Strahlung wird <strong>von</strong> einem Monochromator spektral zerlegt. Durch einen Spalt werden<br />
die einzelnen Wellenlängen nacheinander aus gesondert und fallen auf die Probe.<br />
Bestimmte Wellenlängen dieser Strahlung werden <strong>von</strong> der Probe zum Teil<br />
absorbiert, der austretende Lichtstrahl ist entsprechend geschwächt.<br />
Verantwortlich für die Lichtabsorption sind vorwiegend die Elektronen der<br />
absorbierenden Moleküle. Ein Detektor wandelt die optischen Signale in elektrische<br />
Signale um und ein Schreiber zeichnet <strong>von</strong> jeder Wellenlänge das entstandene<br />
elektrische Signal auf. Das Bild, welches der Schreiber aufzeichnet (Extinktion in<br />
Abhängigkeit <strong>von</strong> der Wellenlänge) nennt man das Spektrum der Substanz.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 7 <strong>von</strong> 41<br />
Die Molekülart wird über die absorbierte Wellenlänge ermittelt, und die Stärke der<br />
Lichtschwächung gibt Auskunft über die Probenkonzentration.<br />
Schickt man sichtbares(visuelles) Licht durch eine gefärbte Lösung, so wird durch die<br />
in Lösung befindliche Verbindung, ein Teil des eingestrahlten Lichtes absorbiert. Die<br />
Größe der Absorption wird über die Messgröße Extinktion E ermittelt. Man<br />
bezeichnet die Extinktion auch als spektrales Absorptionsmaß. Sie hängt <strong>von</strong> der<br />
Wellenlänge des Messlichtes und <strong>von</strong> der Verbindung ab.<br />
Mittels eines Photometers, wie einem Spektrallinienphotometer kann die Extinktion<br />
einer Untersuchungslösung gemessen und mit Hilfe der photometrischen<br />
Kalibrierkurve deren Konzentration ermittelt werden.<br />
Dazu ist erforderlich, die Extinktion in Abhängigkeit der Konzentration zu bestimmen.<br />
Stellt man diesen Zusammenhang graphisch dar, so ergibt sich als Kalibrierkurve<br />
eine Gerade, welche zeigt, dass sich Extinktion und Konzentration direkt proportional<br />
zueinander verhalten. (bei verdünnten Lösungen und monochromatischem Licht)<br />
Extinktion<br />
1<br />
0,9<br />
0,8<br />
0,7<br />
0,6<br />
0,5<br />
0,4<br />
0,3<br />
0,2<br />
0,1<br />
0<br />
Kalibrierkurve<br />
0 2 4 6 8 10 12<br />
Konzentration
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 8 <strong>von</strong> 41<br />
Die Kalibriergerade muss für jede <strong>Bestimmung</strong> bei entsprechender Wellenlänge<br />
aufgestellt werden, da nicht jede Wellenlänge gleich stark <strong>von</strong> der Verbindung<br />
absorbiert wird. Ein Absorptionsspektrum zeigt das Absorptionsverhalten eines<br />
Stoffes.<br />
2.1.10. Absorptionsphotometrie und Absorptionsspektrum<br />
In der Absorptionsphotometrie oder Spektroskopie misst man die Lichtschwächung,<br />
die bei Durchstrahlung einer Lösung mit auftritt. Die Absorption ist <strong>von</strong> der in Lösung<br />
befindlichen Verbindung, seiner Konzentration und der Wellenlänge der Strahlung<br />
abhängig. Photometer oder Spektrometer sind die Messgeräte mit denen Absorption<br />
als Extinktions- oder Transmissions-Wert messbar sind. Stellt man den<br />
Zusammenhang der Messgröße Extinktion E oder Transmission T gegenüber der<br />
Wellenlänge graphisch dar, so erhalt man ein sogenanntes Absorptionsspektrum. Da<br />
dieses substanzspezifisch ist, kann dadurch eine Verbindung identifiziert oder deren<br />
Reinheit überprüft werden. Nach Ermittlung des Absorptions-Maximums oder der<br />
Maxima aus dem Absorptionsspektrum der Verbindung weiß man, bei welcher<br />
Wellenlänge eine empfindliche Konzentrationsbestimmung möglich ist. Die<br />
Extinktionswerte sind bei Messung im Absorptionsmaximum am größten.<br />
2.2. Photometrische <strong>Bestimmung</strong> der <strong>Acetylsalicylsäure</strong><br />
2.2.1 Reaktionsprinzip<br />
Zur Photometrischen <strong>Bestimmung</strong> im sichtbaren Bereich wird vorausgesetzt, das die<br />
zu untersuchende Substanz eine Farbe hat, also das sichtbare Licht absorbiert.<br />
<strong>Acetylsalicylsäure</strong> ist jedoch in Lösung farblos. Deshalb muß die Probe für die<br />
<strong>Bestimmung</strong> noch vorbereitet werden. Durch Einwirkung <strong>von</strong> NaOH-Lösung auf die<br />
<strong>Acetylsalicylsäure</strong> wird diese hydrolysiert. Dabei entstehen Salicylsäure und Acetat<br />
(NatriumAcetat). Die Salicylsäure bildet mit dem Fe 3+ -Kation einen violetten<br />
Eisen(III)salicylat-Komplex. Mit diesem Komplex ist die photometrische <strong>Bestimmung</strong><br />
möglich.<br />
2.2.2. Reaktionsgleichungen
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 9 <strong>von</strong> 41<br />
2.2.3. Arbeitsgeräte<br />
- CADAS 50 Photometer<br />
- Küvetten für CADAS 50<br />
- 6x 100 ml Maßkolben<br />
- 250 ml Maßkolben<br />
- 500 ml Maßkolben<br />
- 1 l Maßkolben<br />
- 5 ml Vollpipette<br />
- 10 ml Vollpipette<br />
- 25 ml Vollpilette<br />
2.2.4. Reagenzien<br />
- <strong>Acetylsalicylsäure</strong> (ASS)<br />
- Fe(NO3)3 x 9H20<br />
- 0,25 mol/l NaOH-Lösung<br />
- 0,1 mol/l HCl-Lösung<br />
- Trinder Reagenz<br />
Es werden 4 g Fe(NO3)3 x 9H20 in wenig Wasser im 1 l<br />
Maßkolben gelöst, dann werden 200 ml 0,1 mol/l HCl-Lösung<br />
hinzu gegeben und mit Wasser aufgefüllt.<br />
- <strong>Acetylsalicylsäure</strong> Standardlösung<br />
250 mg <strong>Acetylsalicylsäure</strong> werden in einem 500 ml Maßkolben in<br />
25 ml 0,25 mol/l NaOH-Lösung gelöst. Zur Hydrolyse der<br />
<strong>Acetylsalicylsäure</strong> lässt man die NaOH-Lösung etwa 10 Minuten<br />
lang einwirken. Danach kann mit Wasser aufgefüllt werden.<br />
2.2.5. Aufnahme des Absorptionsspektrums<br />
In einen 100 ml Maßkolben werden 25 ml Trinderreagenz gegeben danach werden<br />
3 ml der <strong>Acetylsalicylsäure</strong> Standardlösung hinzu gegeben und mit Wasser<br />
aufgefüllt. Das Photometer wird eingeschalten und das Programm SCAN aufgerufen.<br />
Es wird der Messbereich λ� <strong>von</strong> 400 nm bis 600 nm wird eingestellt. Eine<br />
Analyseküvette wird mit der Lösung aufgefüllt und im Küvetteschacht des<br />
Photometers eingesetzt. Die Messtaste wird betätigt und das Spektrum wird<br />
aufgezeichnet.<br />
Für den Eisen(III)salicylat-Komplex ergibt sich eine maximale Absorption bei 530 nm.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 10 <strong>von</strong> 41<br />
2.2.6. Erstellen der Kalibrierkurve:<br />
In 6 100 ml Maßkolben werden je 25 ml Trinder Reagenz gegeben. Nun kommen<br />
verschiedene Mengen an <strong>Acetylsalicylsäure</strong> Standardlösung hinzu. Danach werden<br />
die Maßkolben mit Wasser aufgefüllt. Von jedem Maßkolben wird Lösung in eine<br />
Analysenküvette gegeben und mit dem Photometer die Extinktion gemessen. Die<br />
einzelnen Messwerte werden als Punkte in ein Extinktions-Konzentrations<br />
Diagramm eingetragen. Die Ausgleichsgerade der Punkte wird als Kalibrierfunktion<br />
angegeben. Für die Kalibrierkurve ergeben sich folgende Werte:<br />
Zugesetzte Menge an Zugesetzte Menge an<br />
Lösung ASS-Lösung in ml ASS-Lösung in mg Extinktion<br />
1 0 0 0<br />
2 3 1,5 0,139<br />
3 5 2,5 0,229<br />
4 10 5 0,46<br />
5 15 7,5 0,686<br />
6 20 10 0,913<br />
Kalibrierbereich: 0-10 mg/100ml ASS<br />
Extinktion<br />
1<br />
0,9<br />
0,8<br />
0,7<br />
0,6<br />
0,5<br />
0,4<br />
0,3<br />
0,2<br />
0,1<br />
0<br />
Kalibrierfunktion<br />
k = 0,0913c + 0,0014<br />
R 2 = 1<br />
0 2 4 6 8 10 12<br />
Konz. mg/100ml
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 11 <strong>von</strong> 41<br />
2.2.7. Durchführung<br />
Die Probe wird in einem Maßkolben mit 0,25 mol/l NaOH-Lösung gelöst. Zur<br />
Hydrolyse der <strong>Acetylsalicylsäure</strong> lässt man die NaOH-Lösung etwa 10 Minuten<br />
einwirken und füllt dann erst mit Wasser auf. Es werden 6 100 ml Maßkolben mit je<br />
25 ml Trinder Reagenz befüllt. Dann wird in jeden Maßkolben der gleiche Teil an<br />
Probelösung gegeben und mit Wasser aufgefüllt. Von jedem Maßkolben wir <strong>von</strong> der<br />
Lösung in eine Analysenküvette gegeben und mit dem Photometer die Extinktion der<br />
einzelnen Lösungen gemessen. Größen für Messkolben und Zugegeben Mengen<br />
können aus der Tabelle entnommen werden.<br />
Menge an ASS<br />
in der<br />
Menge an<br />
NaOH-Lösung<br />
zur Hydrolyse<br />
Größe des Zugegebene<br />
Probesubstanz Probesubstanz Maßkolbens Probelösung<br />
Aspirin 100 mg 250 ml 10 ml 25 ml<br />
Godamed 500 mg 500 ml 5 ml 50 ml<br />
Melabon 250 mg 500 ml 10 ml 25 ml<br />
Neuralgin 250 mg 500 ml 10 ml 25 ml<br />
Unbekannt - - - 500 ml 10 ml 25 ml<br />
2.2.8. Auswertung<br />
Probe<br />
Aspirin Neuralgin Melabon Goldamed Unbekannte<br />
Probe<br />
E1 0,371 0,456 0,462 0,452 0,453<br />
E2 0,378 0,458 0,461 0,458 0,459<br />
E3 0,375 0,451 0,467 0,446 0,463<br />
E4 0,365 0,458 0,464 0,463 0,460<br />
E5 0,366 0,459 0,469 0,460 0,464<br />
E6<br />
Mittelwert<br />
0,374 0,462 0,469 0,449 0,467<br />
= ∑ i E E 1<br />
6<br />
0,372 0,457 0,465 0,455 0,461<br />
Standardabweichung<br />
σ =<br />
1<br />
2<br />
∑( Ei<br />
− E )<br />
n −1<br />
± 0,005 ± 0,004 ± 0,004 ± 0,007 ± 0,005<br />
Menge an ASS in mg<br />
E<br />
c =<br />
0,<br />
0913<br />
Verdünnungsfaktor<br />
4,1<br />
±0,05<br />
5,0<br />
±0,04<br />
5,1<br />
±0,04<br />
5,0<br />
±0,08<br />
5,1<br />
±0,05<br />
f<br />
Menge pro Tablette in mg<br />
25 50 50 100 50<br />
m = f ⋅ c<br />
Sollwert in mg<br />
101,7 250,5 254,8 498,0 252,5<br />
Abweichung vom Sollwert<br />
100 250 250 500 - - -<br />
+1,7% +0,2% +1,9% -0,4% - - -
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 12 <strong>von</strong> 41<br />
2.2.9. Standardaddition:<br />
In 5 100 ml Maßkolben werden je 25 ml Trinder Reagenz und je 10 ml der<br />
unbekannten Probelösung gegeben. Es kommen dann verschiedene Mengen an<br />
<strong>Acetylsalicylsäure</strong> Standardlösung hinzu. Danach werden die Maßkolben mit Wasser<br />
aufgefüllt. Von jedem Maßkolben wird Lösung in eine Analysenküvette gegeben und<br />
mit dem Photometer die Extinktion gemessen. Die einzelnen Messwerte werden als<br />
Punkte in ein Extinktions-Konzentrations Diagramm eingetragen. Die<br />
Ausgleichsgerade der Punkte wird als Analysenfunktion angegeben. Durch<br />
Extrapolation der Analysenfunktion kann der Schnittpunkt mit der<br />
Konzentrationsachse im negativen Bereich ermittelt werden. Der Betrag des<br />
ermittelten Wertes entspricht dann der Konzentration der Probe.<br />
Lösung Zugesetzte Menge an Zugesetzte Menge an<br />
ASS-Lösung in ml ASS-Lösung in mg Extinktion<br />
1 0 0 0,453<br />
2 3 1,5 0,602<br />
3 6 3 0,736<br />
4 9 4,5 0,873<br />
5 12 6 0,999<br />
1,2<br />
Extinktion<br />
1<br />
0,8<br />
0,6<br />
0,4<br />
0,2<br />
a = 0,0909c + 0,4599<br />
R 2 = 0,9998<br />
0<br />
-6 -5 -4 -3 -2 -1 0 1 2 3 4 5 6 7<br />
Konz. mg /100ml<br />
Die Konzentration der Unbekannten Probe kann im Diagramm abgelesenen wedern<br />
oder durch 0 setzen der Analysenfunktion und auflösen nach c errechnet werden.<br />
Rechnerisch ergeben sich folgende Werte.<br />
0,<br />
4599<br />
c = − =<br />
0,<br />
0909<br />
5,<br />
0594<br />
Menge an ASS in mg 5,1<br />
Verdünnungsfaktor 50<br />
Menge pro Tablette in mg 253,0
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 13 <strong>von</strong> 41<br />
3. <strong>Potentiometrische</strong> <strong>Bestimmung</strong><br />
3.1. Grundlagen der Potentiometrie<br />
3.1.2 Prinzip der Potentiometrie<br />
Die potentiometrische Titration ist eine maßanalytische Methode zur<br />
Konzentrationsbestimmung, bei der die Spannung zwischen den Elektroden<br />
galvanischer Zellen (Indikatorelektrode und einer Bezugselektrode) gemessen wird.<br />
Die Messung muss immer stromlos durchgeführt werden, da sonst das Ergebnis<br />
durch elektrolytische Vorgänge verfälscht werden kann. Um diese stromlose<br />
Messung durchzuführen gibt es 2 Möglichkeiten.<br />
a) Erzeugung einer Gegenspannung mittels eines regelbaren Widerstandes.<br />
(Poggendorff'sche Kompensationsmethode)<br />
b) Hochohmiger Innenwiderstand, so dass der Stromfluss <strong>von</strong> vorneherein<br />
unterbunden wird.<br />
3.1.3.Direkte und Indirekte Titration<br />
Sie wird unterteilt in eine direkte und eine indirekte Methode.<br />
Bei der indirekten Potentiometrie wird die Probe gelöst, danach eine definierte<br />
Menge NaOH zugegeben und anschließend die überschüssige NaOH mit HCl titriert.<br />
Der Gehalt der Probe wird über die fehlende NaOH bestimmt.<br />
Bei der direkten Potentiometrie wird der Gehalt der Probe direkt über eine Titration<br />
mit NaOH bestimmt.<br />
3.1.4. Glasektrode<br />
Als Bezugselektrode können Ag/AgCl-,<br />
Kalomel- und Normalwasserstoffelektroden<br />
verwendet werden.<br />
Wobei die ersten beiden zur Gruppe der<br />
Elektroden 2. Art (das Elektrodenmetall ist<br />
<strong>von</strong> einer Schicht eines seiner<br />
schwerlöslichen Salze umgeben) und die<br />
Normalwasserstoffelektrode zur Gruppe der<br />
Elektroden 1. Art (Metallelektrode steht im<br />
Gleichgewicht mit ihren Ionen) gehören.<br />
Meistens wird jedoch die Ag/AgCl-Elektrode<br />
verwendet, da sie im Gegensatz zur<br />
Kalomelelektrode (Hg/HgCl) auch bei<br />
Temperaturen über 80°C nicht zerstört wird.<br />
Die Normalwasserstoffelektrode wird<br />
heutzutage kaum noch verwendet, da sie<br />
einige Nachteile gegenüber den anderen 2<br />
Arten hat. Sie hat kein konstantes Potential<br />
und es besteht die Gefahr einer<br />
Knallgasreaktion
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 14 <strong>von</strong> 41<br />
In unserem Fall benutzen wir eine Ag/AgCl-Elektrode, deren Einzelpotential nach<br />
den Regeln der Elektroden 2. Art durch die Chlorid-Konzentration bestimmt wird.<br />
Aufgrund des potentialbildenden Vorgangs<br />
AgCl + e - → Ag + + Cl -<br />
Und unter Einbeziehung des Löslichkeitsproduktes <strong>von</strong> AgCl<br />
K L<br />
+ − [ Ag ] ⋅[<br />
]<br />
= Cl<br />
Ergibt sich das Potential der Elektrode zu :<br />
E = E<br />
E = E<br />
0<br />
0<br />
RT<br />
+ lg<br />
zF<br />
RT<br />
+ lg K<br />
zF<br />
E = konst.<br />
− = E<br />
+ [ Ag ]<br />
0<br />
L<br />
+<br />
− = E<br />
RT<br />
zF<br />
0<br />
lg<br />
+<br />
RT<br />
zF<br />
− [ Cl ]<br />
lg<br />
+ [ Cl ]<br />
Da die Bezugselektrode ein geschlossenes System bildet, bleibt die Konzentration<br />
der Cl- -Ionen konstant und somit auch das Einzelpotential der Elektrode.<br />
Als Indikatorelektrode wird meist eine Glaselektrode verwendet. Ihr Prinzip beruht auf<br />
Austauschgleichgewichten zwischen Alkaliionen der Glasmembran und den<br />
Protonen der Messlösung. Es kommt zu messbaren Potentialdifferenzen an den<br />
Glasmembrangrenzflächen.<br />
Zur einfacheren Handhabung sind Bezugs- und Glaselektrode meist in einer<br />
Einstabmesskette (Anhang1) zusammengefasst.<br />
Die Glaselektrode muss stets in einer KCl-Lösung aufbewahrt werden, da es sonst<br />
zu einer Austrocknung der Glasmembran kommen kann und ihre Struktur verändert<br />
wird. Dadurch ist die äussere und innere Schicht nicht mehr gleich, was zu einem<br />
Asymmetriepotential führt.<br />
Ihre Vorteile gegenüber den anderen Indikatorelektroden sind ihre einfach<br />
Handhabung (Einstabmesskette), ihr schnelles Ansprechen, hohe Genauigkeit und<br />
ihre geringe Beeinflussung durch Fremdionen.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 15 <strong>von</strong> 41<br />
3.1.5. Anwendung der Nernst'schen Gleichung<br />
E = E<br />
0<br />
+<br />
RT<br />
zF<br />
⎡ Edukt ⎤<br />
log<br />
⎢<br />
⎣Pr<br />
odukt ⎥<br />
⎦<br />
E=Potentialdifferenz<br />
E0 : Normalpotential<br />
R: Gaskonstante (8,314 J/molK)<br />
T: Temperatur<br />
Z: Anzahl der bei dem potentialbestimmenden Redoxvorgang ausgetauschten<br />
Elektronen<br />
F: Faradaysche Konstante (96,486 C/mol)<br />
Anhand der Nernstschen Gleichung sieht man, dass die Potentialdifferenz eine<br />
Funktion der Konzentration ist, und kann somit einen Funktionsgraphen aus dem<br />
gemessenen Potential E[mV] und dem verbrauchten Volumen V[ml] der Masslösung<br />
erstellen, da die Konzentration c in direktem Zusammenhang mit dem Volumen V<br />
und der Stoffmenge n steht:<br />
c =<br />
3.1.6. Ermittlung des Äquivalentpunktes<br />
Die Auswertung der so entstandenen Titrationskurve erfolgt durch einbringen 2<br />
paralleler Tangenten an den Kurvenbiegungen. Danach wird eine zu den Tangenten<br />
parallele Strecke auf die Hälfte des Abstandes der Tangenten gezeichnet. Der<br />
Schnittpunkt der Strecke mit der Kurve ist der Äquivalenzpunkt. Durch Konstruieren<br />
des Lots durch den Äquivalenzpunkt kann man das verbrauchte Volumen <strong>von</strong> NaOH<br />
ablesen.<br />
n<br />
V
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 16 <strong>von</strong> 41<br />
Da wir allerdings über einen PC auswerten, kann man auch einfach die 1. oder 2.<br />
Ableitung zeichnen lassen und den Verbrauch am Hochpunkt (1. Ableitung),bzw<br />
Nulldurchgang (2. Ableitung) ablesen.<br />
16<br />
14<br />
12<br />
10<br />
8<br />
6<br />
4<br />
2<br />
0<br />
0<br />
0,6<br />
1,2<br />
1,8<br />
2,4<br />
Reihe1 entspricht einer pH-Wert Messung<br />
Reihe2 entspricht der 1. Ableitung<br />
3<br />
3,6<br />
4,2<br />
4,8<br />
5,4<br />
6<br />
6,6<br />
7,2<br />
7,8<br />
Reihe1<br />
Reihe2<br />
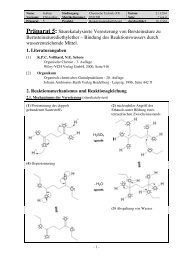
<strong>3.2.</strong> <strong>Potentiometrische</strong> <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong><br />
<strong>3.2.</strong>1. Reaktionsprinzip<br />
Als Grundprinzip der Potentiometrie liegt eine Säure-Base-Titration vor, bei der die<br />
Potentialdifferenz einer Mess- und einer Bezugselektrode gemessen werden. Diese<br />
Differenz ändert sich mit der Konzentration der H3O + bzw OH - -Ionen.<br />
<strong>3.2.</strong>2. Reaktionsgleichung
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 17 <strong>von</strong> 41<br />
<strong>3.2.</strong>3. Arbeitsgeräte: <strong>3.2.</strong>4. Reagenzien:<br />
-Metrohm Dosimat 655 E549<br />
-WTW Inolab Ph/Cond Level3<br />
-100/250ml Erlenmeyerkolben<br />
-10/20/25ml Vollpipetten<br />
-0,1mol/l HCl<br />
-0,1mol/l NaOH<br />
-Ethanol<br />
<strong>3.2.</strong>5. Titerbestimmung<br />
Um den Titer der NaOH zu bestimmen, wurde eine genau bestimmte Masse<br />
<strong>Acetylsalicylsäure</strong> (ASS) in einem Ethanol-Wasser-Gemisch gelöst und mit der<br />
NaOH titriert. Der Titer berechnet sich wie folgt:<br />
<strong>3.2.</strong>6. Durchführung<br />
Die zu überprüfenden Proben mit bekanntem Gehalt ASS wurden in einem Ethanol-<br />
Wasser-Gemisch gelöst und in einen Erlenmeyerkolben überführt. Aus diesem<br />
wurden dann Aliquote für die Titration entnommen. Es wurde in 0,2ml-Schritten<br />
titriert, die in der Nähe des Äquivalenzpunktes teilweise auf 0,1ml-Schritte reduziert<br />
wurden. Von jeder Probe wurden mindestens 3 Titrationen durchgeführt um den<br />
Fehler in der Durchführung möglichst gering zu halten.<br />
Die <strong>Bestimmung</strong> der Probe unbekannten Gehaltes wurde zunächst wie die anderen<br />
Proben durchgeführt, wobei wir allerdings kein brauchbares Ergebnis<br />
herausbekamen, da die Probe neben der ASS auch CaCO3 enthielt, das mit der ASS<br />
in gelöstem Zustand reagiert. Somit musste eine starke Säure (HCl) zugegeben<br />
werden, um das CaCO3 zu eliminieren.<br />
CaCO3 + 2HCl � CaCl2 + H2O + CO2<br />
Da ASS eine schwache Säure ist, kann man in der Auswertung die verschiedenen<br />
Äquivalenzpunkte <strong>von</strong> HCl und ASS deutlich unterscheiden.<br />
3.3.7. Auswertung<br />
Probe<br />
Aspirin Neuralgin Melabon Goldamed<br />
V1 1,3 1,6 1,9 2,4<br />
V2 1,2 2,1 1,8 2,4<br />
V3 1,4 2,1 1,4 2,5<br />
Menge pro Tablette in mg<br />
Sollwert in mg<br />
V NaOHtheor<br />
Titer t= V NaOHprakt<br />
96,5<br />
±7,4<br />
194,9 171,7<br />
±6,6<br />
451,5<br />
±10,7<br />
100 250 250 500<br />
Die Unbekannte Substanz wurde durch Rücktitration mit NaOH bestimmt. Dabei gab<br />
es nur einen Umschlagpunkt bei 5 ml. Die Auswertung ist nicht möglich.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 18 <strong>von</strong> 41<br />
4. Konduktometrische <strong>Bestimmung</strong><br />
4.1. Grundlagen der Konduktometrie<br />
Elektrolytlösungen, also Lösungen, die frei bewegliche Ionen enthalten, leiten<br />
den elektrischen Strom. Die Ionen wandern dabei zu den jeweils<br />
entgegengesetzt geladenen Elektroden. Hierbei setzten verschiedene<br />
Elektrolyte dem Stromfluss verschieden große Widerstände entgegen, es gilt<br />
das gleiche Gesetz wie bei metallischen Leitern<br />
Der Kehrwert des elektrischen Widerstandes heißt elektrische Leitfähigkeit κ.<br />
„Bei konduktometrischen <strong>Bestimmung</strong> wird der elektrische Leitwert G (bzw. der<br />
Widerstand R) <strong>von</strong> Elektrolytlösungen gemessen. Die Messung erfolgt mit<br />
Wechselspannung.“ 1 Gleichspannung könnte zur Zersetzung der Lösung durch<br />
Abscheidungen auf den Elektroden und damit zur Polarisation der Elektroden<br />
führen. Bei Wechselspannung findet jedoch Ionentransport ohne Entladung<br />
statt. Die Messung selbst erfolgt stromlos. „Das Produkt aus Leitwert G und<br />
Zellkonstante ergibt die Leitfähigkeit des Elektrolyten (Gleichung 1)<br />
• κ = Leitfähigkeit<br />
• G = Leitwert = 1/R<br />
• R = elektrischer Widerstand [ Ω ]<br />
• k = Zellkonstante der verwendeten Messelektrode“ 1<br />
Die Zellkonstante k ist der Quotient aus Elektrodenabstand l und Elektrodenfläche<br />
A. In der Praxis ist der Widerstand relativ leicht bestimmbar, der<br />
Elektrodenabstand und die Elektrodenfläche jedoch nicht. Deshalb werden sie<br />
zu einem für die jeweilige Leitfähigkeitsmesszelle konstanten Faktor k<br />
zusammengefasst, dieser Wert wird vom Hersteller angegeben. „Die<br />
Leitfähigkeitsmessung ist nicht stoffspezifisch, da alle in einer Lösung<br />
vorliegenden Ladungsträger (Ionen) ihren Beitrag zur Leitfähigkeit leisten.<br />
Deren Beitrag zur Leitfähigkeit ist abhängig <strong>von</strong> Art (Ionenbeweglichkeit) und<br />
Konzentration der vorhandenen Ionen. Über weite Konzentrationsbereiche<br />
herrscht eine lineare Abhängigkeit zwischen Ionenkonzentration und<br />
Leitfähigkeit der Lösung. Da die Ionenbeweglichkeit sehr stark<br />
temperaturabhängig ist, ist auch die Leitfähigkeit eine stark temperaturabhängige<br />
Größe.<br />
Einige typische Anwendungsbereiche konduktometrischer Messungen sind:<br />
• Reinheitskontrolle <strong>von</strong> Lösungen, z.B. Wasser aus Ionenaustauschern<br />
(ention. Wasser)<br />
• Konzentrationsbestimmung <strong>von</strong> einzelnen, dissoziierenden Substanz,<br />
z.B. Säuren, Laugen, Salze<br />
• <strong>Bestimmung</strong> charakteristischer Stoffgrößen, z.B. Löslichkeitskonstante,<br />
Dissoziationsgrad<br />
1 http://www.lrz-muenchen.de/~aae/aaeframe.html<br />
(1)
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 19 <strong>von</strong> 41<br />
• <strong>Bestimmung</strong> der Gesamtelektrolytkonzentration, z.B. Wässer aller Art,<br />
Blutserum<br />
• Strukturuntersuchungen, Wechselwirkung zwischen Ionen wie<br />
Solvatation, Assoziation<br />
• Indikation, z.B. Endpunktbestimmung <strong>von</strong> Titrationen verschiedenster Art<br />
Beim vorliegenden Praktikumsversuch wird die Leitfähigkeitsänderung eines<br />
Elektrolyten im Verlauf einer Titration verfolgt. Durch Zugabe <strong>von</strong><br />
Titrationsmittel ändert sich die Zusammensetzung des Elektrolyten und die<br />
Konzentration der verschiedenen Ionen [...]<br />
Da die Leitfähigkeit proportional zur Elektrolytkonzentration ist, spielt in der<br />
Konduktometrie die Verdünnung durch Reagenzzugabe [...] eine große Rolle.<br />
Um den Verdünnungseffekt klein zu halten, muss mit relativ großem<br />
Elektrolytvolumen und möglichst geringem Reagensvolumen (d.h. hohe<br />
Reagenskonzentration) gearbeitet werden. Die Temperatur muss im Verlauf der<br />
Titration konstant gehalten werden.“ 1<br />
Wider Erwarten steigt die Leitfähigkeit nicht unbegrenzt mit steigender<br />
Ionenkonzentration, sondern nimmt ab einer bestimmten Konzentration wieder ab.<br />
Das hat verschiedene Ursachen. Zum ersten die Bildung <strong>von</strong> „Ionenwolken“ und<br />
somit verminderter „effektiver“ Konzentration. Zum zweiten die verringerte<br />
Beweglichkeit dieser Ionenwolken; und zum dritten nimmt bei schwachen<br />
Elektrolyten die Dissoziation mit steigender Konzentration ab.<br />
Leitfähigkeitswerte lassen sich besser vergleichen, wenn sie unabhängig <strong>von</strong> der<br />
Stoffmengenkonzentration sind. Um das zu erreichen, teilt man die Leitfähigkeit κ<br />
durch die Stoffmengenkonzentration c und erhält die molare Leitfähigkeit, die sich auf<br />
ein Mol Elektrolyt in Lösung bezieht.<br />
Jedoch transportiert nicht jedes Mol Ionen dieselbe Ladungsmenge. Deshalb ist es<br />
sinnvoll, die Leitfähigkeit auf dieselbe Ionenladungsmenge in Lösung zu beziehen.<br />
Um das zu erreichen muss man die molare Leitfähigkeit durch die Wertigkeit des<br />
Elektrolyten dividieren, so erhält man die Äquivalentleitfähigkeit.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 20 <strong>von</strong> 41<br />
4.2. Die Elektrode<br />
Die Leitfähigkeit wird mit einer Leitfähigkeitselektrode gemessen.<br />
Der prinzipielle Aufbau einer Leitfähigkeitselektrode sieht so aus<br />
Ableitung<br />
Auf die Platinelektroden ist zusätzlich Platinschwamm aufgetragen, man sagt die<br />
Oberfläche ist „bemohrt“ (Elektrolytische Abscheidung <strong>von</strong> Platin auf Platin)<br />
um die Oberfläche möglichst groß zu machen. Da die Polarisierbarkeit eine Funktion<br />
der Oberfläche ist, wird durch eine möglichst große Oberfläche, die Polarisierung<br />
möglichst unterdrückt, um eine Zersetzung der Probelösung zu verhindern. (vergl. 2 )<br />
Eine Leitfähigkeitselektrode der Firma Schott sieht beispielsweise so aus<br />
Von Metrohm dagegen sehen sie so aus:<br />
Elektroden (Größe ca. 1 – 2 cm 2 )<br />
2 „Chemie für Laboranten und Techniker“; Latscha, Klein, Gulbins; Springer-Verlag; S.286<br />
3 www.schott/schweiz/german/download/laborelektroden_de.pdf<br />
4 http://www.metrohm.de/shop/detail_big.php?ArticleID=44276&UKAT_ID=76<br />
2<br />
4<br />
3
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 21 <strong>von</strong> 41<br />
4.3. Die Titrationskurve<br />
Typische Titrationskurven <strong>von</strong> Leitfähigkeitstitrationen sehen so aus:<br />
Wobei der Endpunkt der gedachte Schnittpunkt der beiden verlängerten Geraden ist.<br />
Man muss bei einer Leitfähigkeitstitration immer bedenken, dass man einen<br />
Summenparameter bestimmt, dass also jeweils alle in der Lösung vorhandenen<br />
Ionen zur Leitfähigkeit beitragen.<br />
Die typische Form der Titrationskurve bei der Alkalimetrie und Acidimetrie ergibt sich<br />
durch die Abnahme der Ionen mit hoher Aktivität (OH - , H3O + ) zum Äquivalenzpunkt<br />
hin. Am Anfang der Titration ist der Gehalt dieser Ionen hoch – in unserem Versuch<br />
verursacht durch die ASS, die ein Proton abgeben kann und H3O + bildet. Da die ASS<br />
aber eine schwache Säure ist, ist die Gesamtleitfähigkeit nicht so hoch. Bei Zugabe<br />
<strong>von</strong> Natronlauge nimmt dann die Leitfähigkeit ab, da die ASS jedoch auch abpuffert<br />
(weil sie eine schwache Säure ist, die im Verlauf der Titration sowohl als Säure als<br />
auch als Anion vorliegt) sieht die Kurve am ehesten aus, wie im Bsp. c).<br />
Am Äquivalenzpunkt liegt dann ein Minimum dieser Ionen vor und die Leitfähigkeit<br />
hat ihr Minimum erreicht. Wird weiterhin Maßlösung zugegeben, steigt die<br />
Leitfähigkeit im Zuge der Erhöhung der aktiven Ionen durch die Maßlösung wieder an<br />
[wie in Bsp. a)].<br />
Wird mit schwachen Elektrolyten titriert (NH3-Lösung [Bsp. b)], H3C-COOH), ist der<br />
Kurvenast dieses Elektrolyten flacher, weil er weniger stark dissoziiert ist und somit<br />
weniger Hydroxid- bzw. Hydroniumionen bildet. Die Leitfähigkeit bleibt also<br />
insgesamt auch geringer.<br />
Bsp. c) zeigt die <strong>Bestimmung</strong> einer staken und schwachen Säure nebeneinander,<br />
ähnlich sähe die <strong>Bestimmung</strong> einer zweiprotonigen Säure aus.<br />
5 „Chemie für Laboranten und Techniker“; Latscha, Klein, Gulbins; Springer-Verlag; S.289<br />
5
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 22 <strong>von</strong> 41<br />
4.4. <strong>Bestimmung</strong> des Äquivalenzpunkt<br />
Um den Äquivalenzpunkt grafisch zu bestimmen, muss man zunächst die<br />
Kurvendaten aufnehmen, in dem man nach einer definierten Zugabe <strong>von</strong> Maßlösung<br />
den jeweiligen Wert der Leitfähigkeit notiert. Die so erhaltenen Wertepaare kann man<br />
zeichnen.<br />
Leitfähigkeit<br />
Verlängert man nun die linearen Kurvenäste, gibt der Schnittpunkt den Verbrauch am<br />
Äquivalenzpunkt an<br />
Leitfähigkeit<br />
Volumen Maßlösung<br />
Volumen Maßlösung<br />
Das Bild zeigt den prinzipiellen Aufbau einer „Dosimat“ Wechseleinheit.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 23 <strong>von</strong> 41<br />
6<br />
konduktometrischen Titration<br />
Thermometer<br />
Oft ist das Thermometer in der Elektrode integriert.<br />
4.6. Die Durchführung<br />
6 http://www.lrz-muenchen.de/~aae/dosi.htm<br />
Zusammen mit einem Computer ist es so<br />
möglich voreingestellte Volumina zuzugeben.<br />
Während des Versuchs wird mit der<br />
Titrierspritze die Maßlösung zur Probe<br />
gegeben.<br />
Elektrode<br />
4.5. Prinzipieller Aufbau einer<br />
Konduktometer<br />
Dosimat mit Maßlösung<br />
Becherglas mit Probe<br />
Magnetrührer
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 24 <strong>von</strong> 41<br />
Bei der Durchführung der Titration gibt es zwei Möglichkeiten:<br />
1) Man verseift zunächst die ganze vorliegende <strong>Acetylsalicylsäure</strong> (ASS) mit<br />
Natronlauge und titriert die Überschüssige Natronlauge mit Salzsäure zurück.<br />
2) Man titriert die schwache ASS direkt mit Natronlauge.<br />
Wir haben uns aus folgenden Gründen für die zweite Methode entschieden:<br />
Bei der Verseifung der ASS entsteht Essigsäure, die den Gesamtelektrolytgehalt<br />
erhöht und damit eventuell die Linearität der Kurve beeinflussen könnte.<br />
Außerdem ist das Verseifen und wieder Abkühlen der Proben zeit- und<br />
arbeitsintensiv. Um effizient zu arbeiten ist die zweite Methode also besser geeignet.<br />
Als Reagenzien brauchen wir Natronlauge, eine Urtitersubstanz für die Natronlauge<br />
(z.B. Oxalsäure oder KHP), Ethanol da die Löslichkeit <strong>von</strong> ASS in einem Ethanol-<br />
Wasser-Gemisch besser ist, als in reinem Wasser, ggf. ein „Leitfähigkeitswasser“ um<br />
die Funktionalität der Messzelle zu überprüfen (z.B. gesättigte NaCl-Lösung)<br />
4.7. Der Titer der Natronlauge<br />
Um den Titer der Natronlauge zu bestimmen wiegt man ungefähr so viel<br />
Urtitersubstanz genau ein, um die gleiche Konzentration der Urtiterlösung zu<br />
bekommen, wie die Maßlösung hat. (Berechnung: m = M * c * V)<br />
Ein Aliquot dieser Lösung wird in ein Becherglas gegeben, mit etwas VE-Wasser<br />
verdünnt und auf einem Magnetrührer gerührt. Nun werden nach und nach definierte<br />
Volumina an Maßlösung zugegeben. Um eine „gute“ Kurve zu bekommen, sollte man<br />
ungefähr so viel Maßlösung zugeben, bis die Leitfähigkeit wieder den Wert wie zu<br />
Beginn der Titration hat. Die Kurve wird nun am Computer gezeichnet und der<br />
Äquivalenzpunkt ermittelt.<br />
Weiß man den Verbrauch am Äquivalenzpunkt, kann man den Titer berechnen:<br />
V ( KHP)<br />
⋅ c<br />
wobei<br />
t<br />
( KHP)<br />
hier<br />
=<br />
mol<br />
25mL<br />
⋅ 0,<br />
012 ⋅t<br />
L<br />
2,<br />
45076g<br />
c(<br />
KHP)<br />
=<br />
1000mL<br />
( KHP)<br />
⋅ t(<br />
KHP)<br />
⋅ z(<br />
KHP)<br />
= V ( NaOH ) ⋅ c(<br />
NaOH )<br />
Einwaage<br />
Einwaage<br />
praktisch<br />
theoretisch<br />
( KHP)<br />
⋅1<br />
= V ( NaOH )<br />
=<br />
0,<br />
012<br />
tatsächlich<br />
250mg<br />
⎯⎯⎯<br />
⎯ →<br />
= 1,<br />
030<br />
245,<br />
076mg<br />
mol<br />
L<br />
mol<br />
⋅ 0,<br />
1 ⋅ t(<br />
NaOH )<br />
L<br />
damit<br />
⎯ ⎯⎯ →V<br />
( NaOH ) = 3mL<br />
⋅t<br />
( NaOH ) ⋅ z(<br />
NaOH )<br />
Durch Einsetzen der Einwaage, und des Verbrauchs am Äquivalenzpunkt kann man<br />
also den Titer der Natronlauge berechen.<br />
4.8. Gehaltbestimmung der Probe
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 25 <strong>von</strong> 41<br />
Für die Probe löst man nun eine Tablette in wenig einer Gemisch aus Ethanol und<br />
VE-Wasser auf und überführt sie quantitativ in einen Messkolben (voraussichtlich<br />
250 mL um 6 Titrationen pro Tablette durchführen zu können), dieser wird nun mit<br />
der Lösung aufgefüllt. Man entnimmt nun ein Aliquot und titriert es auf die oben<br />
angegebene Weise mit der Natronlauge.<br />
der Äquivalenzpunkt wird wie beim Titer bestimmt, der Gehalt wird wie folgt<br />
berechnet:<br />
m(<br />
ASS)<br />
⋅ z(<br />
ASS)<br />
= V<br />
M ( ASS)<br />
hier<br />
( NaOH ) ⋅ c(<br />
NaOH )<br />
⋅t<br />
( NaOH ) ⋅ z(<br />
NaOH )<br />
mol<br />
g<br />
( ASS)<br />
⋅1<br />
= V ( NaOH ) ⋅ 0,<br />
1 ⋅ t(<br />
NaOH ) ⋅1⋅180,<br />
17<br />
L<br />
mol<br />
die so errechnete Masse an ASS bezieht sich auf das Aliquot in der ganzen Tablette<br />
war dann entsprechend das x fache. 7<br />
4.9. Ergebnisse:<br />
n<br />
∑<br />
i=<br />
1<br />
( x − x)<br />
i<br />
2<br />
Standartabweichung s =<br />
n −1<br />
; n ≥ 2<br />
Vertrauensgrenzen γ = 90%<br />
x ± t ⋅<br />
s<br />
; t = ( 3Messungen)<br />
2,<br />
92;<br />
t(<br />
2Messungen)<br />
= 6,<br />
31<br />
n<br />
V(Titer)=2,97 mL<br />
m<br />
⋅ z = V ⋅t<br />
⋅ c ⋅ z<br />
M<br />
hier :<br />
z(<br />
KHP)<br />
= z(<br />
NaOH ) = 1<br />
=> Einwaage = 250mg<br />
/ 100mL<br />
→ 0,<br />
0625g<br />
/ 25mL<br />
0,<br />
0625g<br />
=<br />
g<br />
204,<br />
23<br />
mol<br />
t = 1,<br />
030<br />
0,<br />
00297<br />
mol<br />
L ⋅ t ⋅ 0,<br />
1<br />
L<br />
Aspirin: 25 aus 100 Soll: 100 mg<br />
V(Kond) = 1,32 mL ; 1,3 mL ; 1,43 mL<br />
7 vergl. www.usi.edu/science/chemistry/mkrahlin/courses/chem_321/volumetric%20Aspirin.pdf
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 26 <strong>von</strong> 41<br />
m<br />
⋅ z = V ⋅t<br />
⋅ c ⋅ z<br />
M<br />
m = V ⋅ t ⋅ c ⋅ M<br />
m<br />
m<br />
m<br />
1<br />
2<br />
3<br />
g<br />
* 4<br />
= 0,<br />
00132L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0244959g<br />
/ 25mL<br />
⎯⎯→<br />
97,<br />
98mg<br />
/ Tablette<br />
mol<br />
g<br />
* 4<br />
= 0,<br />
0013L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0241248g<br />
/ 25mL<br />
⎯⎯→<br />
96,<br />
50mg<br />
/ Tablette<br />
mol<br />
g<br />
* 4<br />
= 0,<br />
00143L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0265372g<br />
/ 25mL<br />
⎯⎯→<br />
106,<br />
15mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 100,21 mg<br />
( 4,<br />
9729 + 13,<br />
7641+<br />
35,<br />
2836)<br />
s =<br />
= 5,<br />
20mg<br />
2<br />
γ ( 90%)<br />
= 100,<br />
21mg<br />
± 8,<br />
77<br />
V(pH) = 1,3 mL ; 1,2 mL ; 1,4 mL<br />
g<br />
* 4<br />
m1<br />
= 0,<br />
0012L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
022269g<br />
/ 25mL<br />
⎯⎯→<br />
89,<br />
08mg<br />
/ Tablette<br />
mol<br />
g<br />
* 4<br />
m2<br />
= 0,<br />
0013L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0241248g<br />
/ 25mL<br />
⎯⎯→<br />
96,<br />
50mg<br />
/ Tablette<br />
mol<br />
g<br />
* 4<br />
m3<br />
= 0,<br />
0014L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0259805g<br />
/ 25mL<br />
⎯⎯→<br />
103,<br />
92mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 96,50 mg<br />
( 55,<br />
0564 + 0 + 55,<br />
0564)<br />
s =<br />
2<br />
= 7,<br />
42mg<br />
γ ( 90%)<br />
= 96,<br />
50mg<br />
± 12,<br />
51<br />
Godamed: 20 aus 250 Soll: 500 mg<br />
enthält 250 mg Glycin<br />
V(Kond) = 2,42 mL ; 2,4 mL ; 2,49 mL<br />
g<br />
* 10<br />
m1<br />
= 0,<br />
00242L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0449092g<br />
/ 25mL<br />
⎯⎯→<br />
449,<br />
09mg<br />
/ Tablette<br />
mol<br />
g<br />
* 10<br />
m2<br />
= 0,<br />
0024L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
044538g<br />
/ 25mL<br />
⎯⎯→<br />
445,<br />
38mg<br />
/ Tablette<br />
mol<br />
g<br />
* 10<br />
m3<br />
= 0,<br />
00249L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0462082g<br />
/ 25mL<br />
⎯⎯→<br />
462,<br />
08mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 452,18 mg<br />
( 9,<br />
5481+<br />
46,<br />
24 + 98,<br />
01)<br />
s =<br />
= 8,<br />
77mg<br />
2
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 27 <strong>von</strong> 41<br />
γ ( 90%)<br />
= 452,<br />
18mg<br />
± 14,<br />
79<br />
V(pH): 2,4 mL ; 2,4 mL ; 2,5 mL<br />
g<br />
* 10<br />
m1<br />
= 0,<br />
0024L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
044538g<br />
/ 25mL<br />
⎯⎯→<br />
445,<br />
38mg<br />
/ Tablette<br />
mol<br />
g<br />
* 10<br />
m2<br />
= 0,<br />
0025L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0463938g<br />
/ 25mL<br />
⎯⎯→<br />
463,<br />
94mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 451,57 mg<br />
( 38,<br />
3161+<br />
38,<br />
3161+<br />
153,<br />
0169)<br />
s =<br />
= 10,<br />
72mg<br />
2<br />
γ ( 90%)<br />
= 451,<br />
57mg<br />
± 18,<br />
07<br />
Melabon: 20 aus 100 Soll: 250 mg<br />
enthält Talkum -> Salz der Kieselsäure (MgO, SiO2 [Mg3Si4O10(OH)2])<br />
enthält 250 mg PCM & 50 mg Coffein<br />
V(Kond) = 1,74 mL ; 1,72 mL (; 1,42 mL)<br />
g<br />
* 5<br />
m1<br />
= 0,<br />
00174L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0322901g<br />
/ 25mL<br />
⎯⎯→<br />
161,<br />
45mg<br />
/ Tablette<br />
mol<br />
g<br />
* 5<br />
m2<br />
= 0,<br />
00172L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0319189g<br />
/ 25mL<br />
⎯⎯→<br />
159,<br />
49mg<br />
/ Tablette<br />
mol<br />
g<br />
* 5<br />
( m3<br />
= 0,<br />
00142L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0263517g<br />
/ 25mL<br />
⎯⎯→<br />
131,<br />
76mg<br />
/ Tablette)<br />
mol<br />
Mittelwert x : 160,52 mg<br />
( 0,<br />
8649 + 1,<br />
0609)<br />
s =<br />
1<br />
= 1,<br />
39mg<br />
γ ( 90%)<br />
= 160,<br />
52mg<br />
± 6,<br />
20<br />
V(pH) = 1,9 mL ; 1,8 mL (; 1,4 mL)<br />
g<br />
* 5<br />
m1<br />
= 0,<br />
0019L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0352593g<br />
/ 25mL<br />
⎯⎯→<br />
176,<br />
30mg<br />
/ Tablette<br />
mol<br />
g<br />
* 5<br />
m2<br />
= 0,<br />
0018L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0334035g<br />
/ 25mL<br />
⎯⎯→<br />
167,<br />
02mg<br />
/ Tablette<br />
mol<br />
g<br />
* 5<br />
( m3<br />
= 0,<br />
0014L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0259805g<br />
/ 25mL<br />
⎯⎯→<br />
129,<br />
90mg<br />
/ Tablette)<br />
mol<br />
Mittelwert x : 171,66 mg<br />
( 21,<br />
5296 + 21,<br />
5296)<br />
s =<br />
= 6,<br />
56mg<br />
1<br />
γ<br />
( 90%)<br />
= 171,<br />
66mg<br />
± 29,<br />
27
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 28 <strong>von</strong> 41<br />
Neuralgin 20 aus 100 Soll 250 mg<br />
enthält 250 mg PCM & 50 mg Coffein<br />
V(Kond) = 1,81 mL ; 1,97 mL ; 2,0 mL<br />
g<br />
•5<br />
m1<br />
= 0,<br />
00197L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0365583g<br />
/ 25mL<br />
⎯⎯→<br />
182,<br />
79mg<br />
/ Tablette<br />
mol<br />
g<br />
•5<br />
m2<br />
= 0,<br />
00181L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0335891g<br />
/ 25mL<br />
⎯⎯→<br />
167,<br />
95mg<br />
/ Tablette<br />
mol<br />
g<br />
* 5<br />
m3<br />
= 0,<br />
002L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
037115g<br />
/ 25mL<br />
⎯⎯→<br />
185,<br />
58mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 178,77 mg<br />
( 16,<br />
1604 + 117,<br />
0724 + 46,<br />
3761)<br />
s =<br />
= 9,<br />
48mg<br />
2<br />
γ ( 90%)<br />
= 178,<br />
77mg<br />
± 15,<br />
98<br />
V(pH) = 1,6 mL ; 2,1 mL ; 2,1 mL<br />
g<br />
* 5<br />
( m1<br />
= 0,<br />
0016L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
029692g<br />
/ 25mL<br />
⎯⎯→<br />
148,<br />
46mg<br />
/ Tablette)<br />
mol<br />
g<br />
* 5<br />
m2<br />
= 0,<br />
0021L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0389708g<br />
/ 25mL<br />
⎯⎯→<br />
194,<br />
85mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 194,85 mg<br />
( 0 )<br />
s = = 0mg<br />
1<br />
γ<br />
( 90%)<br />
= 194,<br />
85mg<br />
± 0
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 29 <strong>von</strong> 41<br />
Unbekannte Probe: 25 aus 100<br />
enthält CaCO3<br />
Vorgehen:<br />
Tablette mit 10 mL Ethanol versetzen und lösen, quantitativ überführen. mit 20 mL<br />
HCl versetzen und 5 min im Ultraschallbad lösen. Dann auffüllen und 25 mL titrieren.<br />
Die starke Abnahme der Leitfähigkeit entspricht der Neutralisation der stark dissoz.<br />
HCl. Der langsame Anstieg zeigt die Umsetzung der schwach dissoz. ASS. Der<br />
starke Anstieg am Schluss resultiert aus dem Überschuss der zugegebenen<br />
Maßlösung.<br />
Der erste Äquivalenzpunk zeigt also der Verbrauch für die HCl an, der zweite den für<br />
das Säuregemisch (Äp(ASS) = Äp2 – Äp1)<br />
V(Kond) = 3,22 mL ; 3,22 mL ; 3,15 mL<br />
g<br />
* 4<br />
m1<br />
= 0,<br />
00322L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0597552g<br />
/ 25mL<br />
⎯⎯→<br />
239,<br />
02mg<br />
/ Tablette<br />
mol<br />
g<br />
* 4<br />
m2<br />
= 0,<br />
00315L<br />
⋅1,<br />
030 ⋅ 0,<br />
1M<br />
⋅180,<br />
17 = 0,<br />
0584562g<br />
/ 25mL<br />
⎯⎯→<br />
233,<br />
82mg<br />
/ Tablette<br />
mol<br />
Mittelwert x : 237,29<br />
( 2,<br />
9929 + 2,<br />
9929 + 12,<br />
0409)<br />
s =<br />
2<br />
= 3,<br />
00mg<br />
γ ( 90%)<br />
= 237,<br />
29mg<br />
± 5,<br />
06<br />
Potentiometrisch lässt sich diese Probe nicht auswerten, weil man nur einen<br />
Äquivalenzpunkt erkennt, dessen Verbrauch immer bei genau 5 mL liegt.<br />
Man kann jedoch den Verbrauch für die Salzsäure nicht erkennen.<br />
Zusammenfassend die konduktometrischen Ergebnisse:<br />
Einzelwerte in mg Mittelwert in mg<br />
Aspirin 97,98 96,50 106,15 100,21<br />
Godamed 449,09 445,38 462,08 452,18<br />
Melabon 161,79 159,49 (131,76) 160,52<br />
Neuralgin 182,79 167,95 185,58 178,77<br />
Probe 239,02 239,02 233,82 237,29<br />
5. Fehlerbetrachtung<br />
5.1. Grundlagen der Fehlerrechnung
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 30 <strong>von</strong> 41<br />
5.1.1. Fehler und Unsicherheiten<br />
Bei der analytischen <strong>Bestimmung</strong> <strong>von</strong> Substanzen können viele Faktoren auftreten,<br />
die zu falschen Ergebnissen führen. So kann es zu systematischen und zu zufälligen<br />
Fehlern kommen. Systematische Fehler treten immer gleich auf. Sie werden<br />
hervorgerufen durch<br />
- Unvollkommenheit der Sensoren<br />
- Unvollkommenheit der Meßaufbereitung<br />
- Unvollkommenheit der Meßverfahren<br />
- Unvollkommenheit des Meßgegenstandes<br />
- nicht erfaßte Einflüsse der Umwelt<br />
Systematische Fehler haben eine bestimmte Größe und ein bestimmtes Vorzeichen<br />
und lassen sich grundsätzlich korrigieren.<br />
Wird der Meßwert nicht korrigiert, so ist das Meßergebnis falsch. Es hat einen<br />
systematischen Fehler.<br />
Würde z.B. eine Skala immer am falschen Punkt abgelesen werden oder ein<br />
Messgerät immer den falschen Wert anzeigen so wäre dies ein systematischer<br />
Fehler weil er immer die gleiche Abweichung hat.<br />
Zufällige Fehler nennt man Unsicherheiten.<br />
Sie werden hervorgerufen Durch:<br />
Beobachtungsfehler<br />
- Ablesegenauigkeit<br />
- Schätzen<br />
- Ungeschicklichkeit<br />
Zufällige Einflüsse<br />
- Störungen<br />
Unkontrollierbare Einflüsse<br />
- Mechanische Erschütterung<br />
- Elektrische oder magnetische Felder<br />
- Rauschen<br />
- Rückkopplungen<br />
- Spannungsschwankungen<br />
Zufällige Fehler lassen sich in der Regel nicht korrigieren. Die Möglichkeit einer<br />
Lösung dieser Probleme beruht auf der Tatsache, daß die Beobachtungsfehler,<br />
obwohl sie im Einzelfall größer oder kleiner, positiv oder negativ sein können, im<br />
Ganzen gesehen einer Gesetzmäßigkeit unterliegen und mit Methoden der<br />
Wahrscheinlichkeitslehre und der Statistik zum Teil gelöst werden können.<br />
Es gibt absolute Unsicherheiten und relative Unsicherheiten.<br />
Die absoluten Unsicherheiten geben einen konkreten Zahlenwert an um den das<br />
Ergebnis wohl vom tatsächlichen Wert abweichen wird. Die absolute Unsicherheit<br />
kann entweder durch den Vergleich mehrerer Messwerte Errechnet werden oder sie<br />
wird wenn mehrere Messungen nicht durchführbar sind einfach abgeschätzt indem
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 31 <strong>von</strong> 41<br />
man sich überlegt wie genau man wohl mit dem Messgerät den Messwert ablesen<br />
oder bestimmen kann.<br />
Die relativen Unsicherheiten geben eine prozentuale Abweichung vom Messwert an,<br />
welche auch als Güte für die Messung angesehen werden kann.<br />
10% Abweichung sind eine sehr grobe Messung.<br />
1% Abweichung hingegen wäre eine relative genaue Messung.<br />
5.1.2. Normalverteilung<br />
Die Zufälligen Fehler folgen in der Regel der Gaußschen Normalverteilung. Es wird<br />
da<strong>von</strong> ausgegangen das ein Wert niemals genau ermittelt werden kann. Der<br />
gemessene Wert ist jedoch je nach Genauigkeit der Messung in einem größeren<br />
oder kleineren Unsicherheitsintervall ± s zu finden.<br />
Im Diagramm ist die Funktion der Gaußschen Normalverteilung zu sehn.<br />
Hier sieht man dass x Best der Wahrscheinlichste Wert der Messergebnisse sein wird.<br />
Während sich die tatsächlich gemessenen Werte wohl um den Punkt x Best Bilden<br />
werden. Ermittelt man nun die Gesamtfläche unter der Kurve so und vergleicht sie<br />
mit den Flächen im Intervall <strong>von</strong> 2s und 4s so wird man sehn das 64% der Fläche im<br />
Intervall <strong>von</strong> 2s sind und 95% der Fläche im Intervall <strong>von</strong> 4 s sind. Für das Intervall<br />
6s kann da<strong>von</strong> ausgegangen werden, dass es 100% der Fläche beinhaltet.<br />
Die Fläche gibt jeweils an wie wahrscheinlich ein Wert in dem Intervall auftritt.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 32 <strong>von</strong> 41<br />
s kann also als absolute Unsicherheit des Wertes xBest betrachtet werden. Das heißt<br />
der tatsächliche messwert Weicht liegt immer im Intervall zwischen xBest - s und xBest<br />
+ s. Oder wenn man noch sicherer sein will zwischen xBest - 2s und xBest + 2s.<br />
5.1.3. Mittelwert, Standardabweichung und Fehlerfortpflanzung<br />
Bei mehren Messwerten kann xBest leicht ermittelt werden. xBest entspricht ganz<br />
einfach dem Mittelwert der Messungen.<br />
1<br />
n<br />
x = Best ∑ i= 1x<br />
i n<br />
s kann entweder durch vergleich der Messwerte abgeschätzt werden oder über die<br />
Formel für die Standardabweichung ermittelt werden. Die Standardabweichung ist<br />
ein Maß für die Streuung der Messwerte. Darüber kann auf die Güte der Messungen<br />
geschlossen werden.<br />
s =<br />
1<br />
n −1<br />
n<br />
∑ ( x −<br />
i= i x<br />
1<br />
)<br />
2<br />
Es kann auch einfach ein Intervall gewählt werden in dem alle Messwerte<br />
vorkommen sofern sie nicht zu sehr abweichen. z.B. s = ± (größte Abweichung).<br />
Wenn ein Messwert zu sehr abweicht sollte er in der Regel für die Rechnung nicht<br />
berücksichtigt werden.<br />
Für die relative Unsicherheit gilt:<br />
s<br />
r<br />
=<br />
x<br />
s<br />
Best<br />
Hat man eine Funktion <strong>von</strong> mehreren Variablen die jeweils mit einer Unsicherheit<br />
behaftet ist, so gilt für den Gesamtfehler das Gesetz der Fehlerfortpflanzung.<br />
Für die Fehlerfortpflanzung <strong>von</strong> absoluten Unsicherheiten mit mehren Faktoren gilt:<br />
Dabei gilt für zufällige Fehler, die sich gegenseitige kompensieren folgende Regel:<br />
s<br />
⎛ ∂<br />
⎜<br />
⎝ ∂x<br />
2<br />
2<br />
⎞ ⎛ ∂<br />
⎞ ⎛ ∂<br />
f • ⎟ + ⎜<br />
⎟ + ⎜ •<br />
( , , ) f •<br />
∂ ( , , ) f<br />
x y z s x<br />
x y z s y<br />
( x,<br />
y,<br />
z ) z<br />
y<br />
z<br />
= s<br />
⎠<br />
⎝<br />
⎠<br />
⎝ ∂<br />
⎞<br />
⎟<br />
⎠<br />
2
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 33 <strong>von</strong> 41<br />
Wirken jedoch alle Fehler in eine Richtung so gilt folgende Regel:<br />
s<br />
⎡ ∂<br />
⎢<br />
⎣∂x<br />
⎤ ⎡ ∂<br />
⎤ ⎡ ∂ ⎤<br />
•<br />
( ) ⎥ + ⎢ f • +<br />
( ) ⎥ ⎢ f •<br />
x, y,<br />
z sx<br />
( ) ⎥<br />
⎦ ⎣∂<br />
s y<br />
y x,<br />
y,<br />
z<br />
⎦ ⎣∂z<br />
x,<br />
y,<br />
z ⎦<br />
f z<br />
= s<br />
Wobei die Funktionen in den oberen Gleichungen nur <strong>von</strong> 3 Variablen abhängen. Die<br />
Funktion kann beliebig viele Variablen beinhalten <strong>von</strong> jeder Variablen muß beim<br />
berechnen der absoluten Unsicherheit die partielle Ableitung gebildet werden. Die<br />
Ableitung wird dann mit der absoluten Unsicherheit der Variablen multipliziert. Je<br />
nach Art der Messungen muß entschieden werden ob sich Fehler aufheben oder alle<br />
in eine Richtung wirken. Wirken alle Fehler in eine Richtung so arbeitet man nur mit<br />
den Beträgen. Heben sich jedoch Fehler auf so werden die Beträge quadriert, addiert<br />
und dann <strong>von</strong> der Summe die Wurzel gezogen.<br />
Bevor man mit dem Versuch beginnt sollte man sich überlegen welche Fehler<br />
auftreten könnten und wie genau man mit den vorhandenen Geräten die Werte<br />
bestimmen kann. Es gibt auch Methoden die einem helfen Fehler klein zu halten. Es<br />
bietet sich bezogen auf das bestimmen der <strong>Acetylsalicylsäure</strong> z.B. an den Versuch<br />
zuerst mit einer Probe bekannten Gehaltes durchzuführen. Weitere Hilfen bieten<br />
Kalibrierkurven und auch das mehrmalige durchführen <strong>von</strong> Messungen und des<br />
Versuches.<br />
5.1.4. Kalibrierung eines Verfahrens<br />
Bei der Kalibrierung eines Verfahrens wir ermittelt wie sich Proben unterschiedlicher<br />
Konzentration auf das Messverfahren hin verhalten. Zu jedem Messwert x wird das<br />
Signal y ermittelt. Die Punkte werden dann in ein Signal – Konzentrations Diagramm<br />
eingezeichnet. Da die Punkte wohl nicht ideal auf einer Linie liegen sonder ebenfalls<br />
eine gewisse Abweichung s sowohl in x als auch in y Richtung haben werden kann<br />
eine Mittelgrade gezogen werden die in der Summe <strong>von</strong> allen Punkten etwa die<br />
Gleiche Abweichung hat bzw. das Unsicherheitsintervall des Punktes berührt.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 34 <strong>von</strong> 41<br />
Die gezogene Gerade ist eine Funktion der Konzentration x. Sie wird auch<br />
Kalibrierfunktion k(x) genannt. Und folgt der Gleichung.<br />
∆y<br />
k = mx + b m =<br />
( x )<br />
wobei ∆x<br />
Steigung der Geraden und b der Blindwert ist<br />
des Messgeräts ist. Der blindwert muss in der Regel mit in die Rechnung einbezogen<br />
werden.<br />
Um die Unsicherheit der Kurve zu beschreiben kann eine Kurve durch den Blindwert<br />
und den Punkt der größten Abweichung gezogen werden. Diese kurve besitz eine<br />
größere Steigung und gibt den Fehler nach oben hin an. So kann auch die kleinste<br />
Steigung ermittelt werden und durch Kenntnis dieser auf die richtigkeit der<br />
Mittelgeraden geschlossen werden.<br />
Die Kalibrierfunktion kann später dann mit den Messergebnissen verglichen werden<br />
und auf deren Richtigkeit geschlossen werden.<br />
5.1.4. Standardadditionsverfahren<br />
Das Standardadditionsverfahren wird in etwa wie das Kalibrierverfahren<br />
durchgeführt. Es wird jedoch wird hier mit der Probe gearbeitet. Von der Probe<br />
werden etwa 5 gleiche Anteile genommen. Jedem der Anteile wird eine<br />
unterschiedliche Stoffmenge der zu untersuchenden Substanz zu gegeben. Danach<br />
werden aus den Proben die Signalwerte ermittelt und in ein Diagramm<br />
eingezeichnet. Es kann wieder die mittelgerade gebildet werden.<br />
Signal<br />
0,81 1,2<br />
0,2 0,4 0,6<br />
-6 -5 -4 -3 -2 -1 0 1 2 3 4 5 6 7 0<br />
Konz. mg /100ml
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 35 <strong>von</strong> 41<br />
Wenn man die Mittelgerade auf die x-Achse extrapoliert so erhält man einen<br />
negativen Wert, dessen Betrag der Konzentration der Probelösung entspricht. Dieses<br />
Verfahren eignet sich zum Bestimmen <strong>von</strong> kleinen Stoffmengen. Der Blindwert des<br />
Lösungsmittels muss jedoch vorher bekannt sein. Bei dieser Methode fließen<br />
sämtliche <strong>von</strong> der Probe verursachten Fehlerquellen mit in die Funktion ein. Mit<br />
Steigender ASS-Konzentration fällt die Reaktion der ASS immer merh ins Gewicht.<br />
Die fallen dadurch weniger auf.<br />
5.1.5. Richtigkeit, Genauigkeit und Präzision<br />
Präzision:<br />
„Die Präzision ist ein Maß für die Übereinstimmung zwischen unabhängigen<br />
Messergebnissen unter festen Bedingungen. Liegen also mehrere Messwerte dicht<br />
beieinander, so hat die Messmethode eine hohe Präzision. Das bedeutet aber noch<br />
nicht, dass die gemessenen Werte auch richtig sind. Sie könnten präzise falsch sein.<br />
[...] Hier könnten durch einen systematischen Fehler [...] die Wert zwar sehr präzise<br />
bestimmt worden sein, aber eben verschoben sein.“ 9<br />
Richtigkeit:<br />
„Die Richtigkeit ist ein Maß für die Übereinstimmung zwischen dem aus einem<br />
großen Datensatz erhaltenen Mittelwert und dem anerkannten Referenzwert. Wenn<br />
also der Mittelwert aus vielen Messungen gut [...] dem wahren Wert<br />
übereinstimmt, so ist die Richtigkeit hoch. Dies sagt nichts darüber aus, wie stark die<br />
einzelnen Werte streuen.“ 9<br />
Genauigkeit:<br />
„Der Begriff Genauigkeit wird (fälschlicherweise) häufig mit Präzision gleichgesetzt.<br />
Die Genauigkeit ist ein Maß für die Übereinstimmung zwischen dem (einzelnen)<br />
Messergebnis und dem wahren Wert der Messgröße. Eine hoher Genauigkeit kann<br />
man also nur erreichen, wenn sowohl die Präzision als auch die Richtigkeit gut<br />
sind.“ 8<br />
8 http://www.kowoma.de/gps/zusatzerklaerungen/Praezision.htm
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 36 <strong>von</strong> 41<br />
5.2.1. Allgemeine Fehler<br />
Bei jedem Versuch treten Fehler auf, die mehr oder weniger ins Gewicht fallen. Diese<br />
Fehler können <strong>von</strong> den Arbeitsgeräten abhängig sein. Je nach dem wie genau sie<br />
geeicht oder abgelesen werden könne. In der Tabelle sind einige Tolleranzen<br />
geeichter Maßkolben und Vollpipetten aufgeführt. Diese Fehler fallen in der Regel<br />
nicht sehr ins Gewicht. Sie sollten jedoch nicht ganz außer acht gelassen werden.<br />
Maßkolben Volumen<br />
100 ml<br />
250 ml<br />
500 ml<br />
Toleranz einer Waage<br />
Toleranz Vollpipetten<br />
± 0,1 ml<br />
± 0,15 ml<br />
± 0,25 ml<br />
± 0,1 mg<br />
± 0,5 mg<br />
3 ml<br />
5 ml<br />
15 ml<br />
20 ml<br />
25 ml<br />
50 ml<br />
Toleranz<br />
± 0,01 ml<br />
± 0,015 ml<br />
± 0,03 ml<br />
± 0,03 ml<br />
± 0,03 ml<br />
± 0,075 ml<br />
Es können aber auch Einflüsse wie Temperatur, Druck und Zeit zu Fehlern führen.<br />
Temperaturänderungen führen z.B. zu Volumenänderungen <strong>von</strong> Flüssigkeiten.<br />
Maßkolben und Vollpipetten sind ebenfalls auf eine gewisse Temperatur geeicht.<br />
Eine Temperaturänderung führt auch zu veränderten Reaktionsgeschwindigkeiten<br />
und Ionenaktivitäten.<br />
Die Zeit spielt auch oft eine rolle so kann z.B. eine Maßlösung ihre Konzentration<br />
ändern oder deine Substanz zerfallen und nicht mehr richtig nachgewiesen werden.<br />
5.2.2. Spezifische Fehler<br />
5.2.2.1 Fehler bei der Konduktometrie und der Potentiometrie<br />
Betrachtet man sich die Sollwerte und die gefundenen Istwerte<br />
Sollwert in mg/Tablette Istwert (kond) s Istwert (pH) s<br />
Aspirin 100 100,21 5,20 96,50 7,42<br />
Godamed 500 452,18 8,77 451,57 10,72<br />
Melabon 250 160,52 1,39 171,66 6,56<br />
Neuralgin 250 178,77 9,48 194,85 0<br />
Probe ? 237,29 3,00 nicht mögl. -<br />
So stellt man fest, dass bei Aspirin die Werte am nahsten beim Sollwert liegen. Das<br />
liegt vermutlich daran, dass Aspirin die einzige Tablette ist, die keine weiteren<br />
wirksamen Bestandteile enthält.<br />
Godamed enthält 250 mg Glycin pro Tablette. Glycin ist die einfachste Aminosäure<br />
mit einem isoelektischen Punkt (IEP) <strong>von</strong> 6,06. Am IEP hat Glycin folgende Struktur:
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 37 <strong>von</strong> 41<br />
H<br />
O<br />
+<br />
NH3 O<br />
pH = 6,06<br />
Während der Tirtration haben wir einen pH-Bereich <strong>von</strong> 3 bis ca. 11 durchlaufen<br />
Das bedeutet, das das Gycin, welches in Ethanol schlecht löslich in Wasser jedoch<br />
gut löslich ist, folgende Protolysestufen durchlaufen hat:<br />
pH < 6,06: pH 6,06 pH > 6,06:<br />
O<br />
O<br />
O<br />
H<br />
+<br />
NH3 OH<br />
H<br />
+<br />
NH3 Währenddessen wurden zwei Protonen abgegeben, die natürlich auch Natronlauge<br />
verbrauchen. Dadurch wird der pH-Wert niedriger gemessen, als er eigentlich ist und<br />
dadurch später ein zu geringer Verbrauch am Äquivalenzpunkt abgelesen.<br />
Das sieht man auch im Ergebnis, die werte liegen unterhalb <strong>von</strong> 500 mg<br />
Melabon und Neuralgin enthalten je 250 mg Paracetamol und 50 mg Koffein je<br />
Tablette. Melabon enthält außerdem noch Talkum. Auch hier wurden die Werte zu<br />
tief gefunden<br />
Koffein Paracetamol (PCM):<br />
C<br />
H 3<br />
N<br />
N<br />
CH 3<br />
N<br />
O<br />
N<br />
O<br />
CH 3<br />
C<br />
H 3<br />
O<br />
N<br />
H<br />
Die Struktur des Koffeins lässt nicht auf eine saure oder alkalische Reaktion<br />
schließen<br />
Laut www.http://de.wikipedia.org ist jedoch Paracetamol ein Phenol und hat damit<br />
auch saure Eigenschaften, es kann also im Verlauf der Titration ein Proton abgeben:<br />
C<br />
H 3<br />
O<br />
N<br />
H<br />
OH<br />
O<br />
C<br />
H 3<br />
OH<br />
H<br />
NH 2<br />
Auch hier wird dadurch der tatsächliche Äquivalenzpunkt zu tief gefunden.<br />
Vergleicht man die Prozentualen Abweichungen der Soll- und der Istwerte<br />
miteinander:<br />
O<br />
N<br />
H<br />
O<br />
O
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 38 <strong>von</strong> 41<br />
Sollwert Istwert (kond) Absoluter Fehler Relativer Fehler in %<br />
Godamed 500 452,18 -47,82 mg -9,56<br />
Melabon 250 160,52 -89,48 mg -35,79<br />
Neuralgin 250 178,77 -71,23 mg -28,49<br />
Sollwert Istwert (pH) Absoluter Fehler Relativer Fehler in %<br />
Godamed 500 451,57 -48,43 mg -9,69<br />
Melabon 250 171,66 -78,34 mg -31,34<br />
Neuralgin 250 194,85 -55,15 mg -22,06<br />
erkennt man, dass sich Glycin nicht so stark auf das Messergebnis auswirkt, wie<br />
PCM, obwohl Glycin während der Titration formal zwei Protonen abgeben kann und<br />
PCM. Ich kann mir das nur so erklären, dass PCM eine stärkere Säure ist, als Glycin,<br />
leider habe ich keine pKs-Werte gefunden um diese Behauptung unterstützen zu<br />
können.<br />
Melabon hat im Vergleich zu Neuralgin sogar noch eine größere Messabweichung,<br />
was vermutlich mit dem darin enthaltenen Talkum zusammenhängt<br />
Um diese Fehler bei einer erneuten Messung zu umgehen, wäre eine Kalibrierkurve<br />
angebracht.<br />
Die Verfälschung des Ergebnisses durch PCM und Glycin ist ein systematischer<br />
Fehler.<br />
Bewertung der Messergebnisse nach Genauigkeit und Präzision<br />
Da die Richtigkeit der Ergebnisse bei Godamed, Melabon und Neuralgin aufgrund<br />
des großen systematischen Fehlers schlecht ist, kann auch die Genauigkeit nicht gut<br />
sein.<br />
Einzelwerte in mg Mittelwert in mg<br />
Aspirin 97,98 96,5 106,15 100,21<br />
Abweichung <strong>von</strong> 100 mg -2,02 -3,5 6,15 0,21<br />
Godamed 449,09 445,38 462,08 452,18<br />
Abweichung <strong>von</strong> 500 mg -50,91 -54,62 -37,92 -47,82<br />
Melabon 161,79 159,49 (131,76) 160,52<br />
Abweichung <strong>von</strong> 250 mg -88,21 -90,51 - -89,48<br />
Neuralgin 182,79 167,95 185,58 178,77<br />
Abweichung <strong>von</strong> 250 mg -67,21 -82,05 -64,42 -71,23<br />
Probe 239,02 239,02 233,82 237,29<br />
Was die Präzision betrifft, wird aus der Tabelle ersichtlich, dass nur bei Neuralgin,<br />
der unbekannten Probe und Godamed die Messwerte einigermaßen dicht beieinander<br />
liegen. Bei Melabon gab es sogar einen Ausreißer bei drei Messungen. Ich<br />
würde deshalb die potentiometrische <strong>Bestimmung</strong> <strong>von</strong> ASS nicht als Methode der<br />
Wahl empfehlen.<br />
Aufgrund der nicht akzeptablen Präzisionen ist auch die Genauigkeit der Werte nicht<br />
gegeben.<br />
Wobei der Mittelwert der Aspirinprobe trotz schlechter Präzision eine gute Richtigkeit<br />
aufweist.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 39 <strong>von</strong> 41<br />
Abschließend würde ich diese Messmethode allenfalls für Aspirin oder andere<br />
Tabletten ohne zusätzliche Wirkstoffe empfehlen, und auch da eher auf die<br />
Konduktometrie vertrauen, als auf die Potentiometrie. Die Konduktometrie ist zwar<br />
schwieriger auszuwerten (hohe Unsicherheit beim festlegen der linearen Bereiche<br />
der Kurve), doch liefert sie insgesamt gesehen die besseren Ergebnisse.<br />
Bei allen anderen Proben, lagen die Konduktometriewerte noch tiefer, als die der<br />
Potentiometrie und waren damit noch weiter vom Sollwert entfernt.<br />
5.2.2.1 Fehler bei der Photometrie<br />
Es war überraschend das alle Werte der Photometrie nicht viel mehr als 1% vom<br />
erwarteten Wert abwichen (siehe Auswertung der Photometrie).<br />
Es wurde erwartet das vorhandenes Paracetamol, welches auch einen Farbigen<br />
komplex mit Fe 3+ Ionen Bildet den Analysenvorgang stört. Dies war jedoch nicht der<br />
fall. Es ist anzunehmen dass der Paracetamolkomplex seine maximale Absorbtion<br />
bei einer komplett anderen Wellenlänge und das Licht bei 520 nm kaum abschwächt.<br />
6. Vergleich der Verfahren<br />
6.1 Zeit und Aufwand<br />
Bei der Photometrie muß die Probe bevor sie analysiert werden kann erst vorbereitet<br />
werden. Dies nimmt die meiste Zeit in Anspruch. Die eigentlichen Messungen sind<br />
schnell durchgeführt. Es können in kurzer Zeit viel Messungen durchgeführt werden.<br />
Bei der Potentiometrie und Konduktometrie ist es lediglich erforderlich die Probe zu<br />
lösen. Dann kann schon los titriert werden. Die Titrationen nehmen jedoch viel Zeit<br />
in Anspruch. In besonderen fällen ist es erforderlich eine Rücktitration durchzuführen.<br />
Dies nimmt noch mehr Zeit in Anspruch. Vorteil bei den Verfahren ist es, dass beide<br />
Parallel durchgeführt werden können.<br />
Aspirin<br />
100 mg ASS<br />
Neuralgin<br />
250 mg ASS<br />
Melabon<br />
250 mg ASS<br />
Godamed<br />
500 mg ASS<br />
Unbekannte<br />
Substanz<br />
Photometrie Konduktometrie Potentiometrie<br />
Wert<br />
101,7<br />
250,5<br />
254,8<br />
498,0<br />
252,5<br />
Abweichung<br />
1,7%<br />
0,2%<br />
1,9%<br />
0,4%<br />
- - -<br />
Wert<br />
100,2<br />
178,8<br />
160,5<br />
452,2<br />
237,3<br />
Abweichung<br />
0,2%<br />
28,5%<br />
35,8%<br />
9,56%<br />
- - -<br />
Wert<br />
96,5<br />
194,9<br />
171,7<br />
451,6<br />
- - -<br />
Abweichung<br />
3,5%<br />
22%<br />
31,3%<br />
9,7%<br />
- - -
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 40 <strong>von</strong> 41<br />
550<br />
500<br />
450<br />
400<br />
350<br />
300<br />
250<br />
200<br />
150<br />
100<br />
50<br />
0<br />
Asprin Melabon Goldamed Neuralgin Probe<br />
Sollwert<br />
Photometrie<br />
PH<br />
Kondu.<br />
Standardadd.<br />
Die Werte sprechen für sich Die Photometrie liefert für jede Probe annähernd das<br />
erwartetet Ergebnis. Die Potentio- und Konduktometrie liefern lediglich bei der<br />
<strong>Bestimmung</strong> <strong>von</strong> ASS in Aspirin gute Ergebnisse.<br />
Es bleibt zu schreiben, dass Die Photometrie für die <strong>Bestimmung</strong> <strong>von</strong> ASS die<br />
vorzuziehende Analysenmethode ist. Sie liefert gute Ergebnisse bei kleinem<br />
Aufwand.
Gruppe3: Name entfernt, Name entfernt, Christopher Gallian, Name entfernt Versuch T3<br />
Studiengang: Chemische Technik Datum: 07.04.09<br />
Thema: <strong>Bestimmung</strong> <strong>von</strong> <strong>Acetylsalicylsäure</strong> in Schmerzmitteln Seite: 41 <strong>von</strong> 41<br />
Literaturangaben:<br />
Potentiometrie:<br />
http://www.alexanderretzlaff.de/docs/instru_analytik/Versuch%2014%20-<br />
%20direkte%20potentiometrische%20Titration.pdf<br />
http://www.alexanderretzlaff.de/docs/instru_analytik/Versuch%2013%20-<br />
%20indirekte%20potentiometrische%20Titration.pdf<br />
Römpp Chemie Lexikon auf CD-ROM,9.Auflage 1<br />
<strong>Acetylsalicylsäure</strong>:<br />
ChemDAT ® Die Merk Chemie Datenbank CD-Rom, Version 2.2.5<br />
Zusammensetzung der Proben:<br />
www.rote-liste.de<br />
Fehlerrechnung:<br />
Analytische Chemie<br />
Matthias Otto<br />
VHC-Verlagsgesellschaft mbH 1995, Seiten 21-29<br />
Fehleranalyse<br />
John R. Taylor<br />
VHC-Verlagsgesellschaft mbH 1988