Das Gehirn ist reparaturfähig - Forschung Frankfurt - Goethe ...
Das Gehirn ist reparaturfähig - Forschung Frankfurt - Goethe ...
Das Gehirn ist reparaturfähig - Forschung Frankfurt - Goethe ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Das</strong> <strong>Gehirn</strong> <strong>ist</strong> <strong>reparaturfähig</strong><br />
Stammzellen in der Neurologie<br />
Als die 1990er Jahre zur »Dekade<br />
des <strong>Gehirn</strong>s« ausgerufen<br />
wurden, war noch nicht abzusehen,<br />
dass in diesem Zeitraum eines der<br />
wichtigsten Dogmen der Neurobiologie<br />
aus den Angeln gehoben werden<br />
würde. Noch vor zehn Jahren<br />
galt es als undenkbar, dass das ausgewachsene<br />
(adulte) Nervensystem<br />
neue Nervenzellen (Neurone) produzieren<br />
kann. Als Grund wurde<br />
die geringe Reparaturfähigkeit des<br />
zentralen Nervensystems nach traumatischen<br />
Verletzungen, wie Verkehrsunfällen,<br />
aber auch bei neurodegenerativen<br />
Erkrankungen, die<br />
mit einem Verlust von Nervenzellen<br />
einhergehen, angeführt.<br />
Umso überraschender war die<br />
Feststellung, dass im adulten <strong>Gehirn</strong><br />
Regionen ex<strong>ist</strong>ieren, in denen täglich<br />
große Mengen Nervenzellen<br />
neu hergestellt werden. Diese Untersuchungen,<br />
ursprünglich an Nagern<br />
und Singvögeln durchgeführt,<br />
sind inzwischen auf Primaten und<br />
auf den Menschen ausgedehnt worden.<br />
Quintessenz <strong>ist</strong>, dass im adulten<br />
<strong>Gehirn</strong> in vielen unterschiedlichen<br />
Regionen undifferenzierte<br />
Stammzellen residieren, die das Potenzial<br />
besitzen, neue Nervenzellen<br />
zu generieren. Diese neugebildeten<br />
Nervenzellen können sich in vorhandene<br />
neuronale Netzwerke integrieren<br />
und funktionelle Kontakte<br />
mit ihren Nachbarzellen aufnehmen.<br />
Wandlungsfähige<br />
Stammzellen<br />
Während der Embryonalentwicklung<br />
wird das »Schicksal« von Zellen<br />
weitgehend festgelegt. Ein<br />
körpereigenes Programm entscheidet<br />
darüber, ob eine Zelle beispielsweise<br />
zu einer Leberzelle oder einer<br />
Nervenzelle heranreift. Ist diese<br />
Entscheidung gefallen, <strong>ist</strong> eine Umkehr<br />
normalerweise nicht mehr<br />
möglich. Ein einmal eingeschlagener<br />
Differenzierungsweg galt als<br />
irreversibel. Umso erstaunlicher<br />
sind Befunde verschiedener Arbeitsgruppen,<br />
die nahelegen, dass aus<br />
Knochenmark- und Muskelzellen<br />
<strong>Gehirn</strong>zellen heranreifen können.<br />
Auch der umgekehrte Weg scheint<br />
möglich zu sein. Dieses Phänomen<br />
wird als »Transdifferenzierung« be-<br />
Stammzellforschung<br />
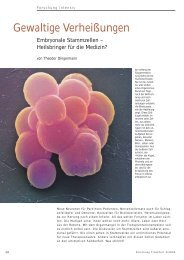
Oben links: Neurale Stammzellen formen in der Gewebekultur kugelförmige Gebilde, so genannte Neurospheres.<br />
Hier sind drei Neurospheres zu erkennen. Oben rechts: Ein einzelnes Neurospere in stärkerer Vergrößerung.<br />
Unten links: Bestimmte Botenstoffe, so genannte Wachstumsfaktoren, führen zu Differenzierungsvorgängen<br />
in Neurospheres. In der Abbildung <strong>ist</strong> das Sprossen von Nervenzellen deutlich zu erkennen.<br />
Unten rechts: Innerhalb der Neurospheres entstehen aus den Stammzellen differenzierte Hirnzellen,<br />
wie Nervenzellen und Gliazellen, die durch unterschiedliche Farben dargestellt sind (grün = Nervenzellen,<br />
rot = Astrozyten, blau = Oligodendrozyten).<br />
zeichnet und deutet auf eine unerwartete<br />
Plastizität verschiedener<br />
Stammzellpopulationen hin (siehe<br />
»Stammzellen bilden Nervenzellen«,<br />
Seite 56).<br />
Dies könnte beispielsweise bedeuten,<br />
dass zugrunde gegangene<br />
Nervenzellen im adulten <strong>Gehirn</strong><br />
durch im Knochenmark residierende<br />
Vorläuferzellen, die in das <strong>Gehirn</strong><br />
wandern und dort ausdifferenzieren,<br />
ersetzt werden. Damit schien<br />
zunächst ein weiteres Dogma der<br />
Zellbiologie erschüttert worden zu<br />
sein. Jüngste Befunde ziehen diese<br />
Beobachtungen allerdings wieder in<br />
Zweifel. Zukünftige Experimente<br />
werden klären müssen, inwieweit<br />
bereits ausgereifte Zellen tatsächlich<br />
auf verschiedene Differenzierungswege<br />
zurückgreifen können.<br />
Die Ex<strong>ist</strong>enz von Stammzellen<br />
im <strong>Gehirn</strong> und anderen Organen<br />
sowie das Phänomen der Transdifferenzierung<br />
führt naturgemäß zur<br />
Frage der therapeutischen Anwendbarkeit,<br />
oder anders formuliert:<br />
»Können <strong>Gehirn</strong>erkrankungen<br />
durch eine Stammzelltherapie geheilt<br />
werden?« In diesem Zusammenhang<br />
wird oft die Kritik geäußert,<br />
dass der körpereigene (endogene)<br />
Reparaturmechanismus im<br />
Nervensystem offenbar wenig effizient<br />
sei, sonst müssten neurodegenerative<br />
Erkrankungen wie die Alz-<br />
<strong>Forschung</strong> <strong>Frankfurt</strong> 3/2002 55
56<br />
Stammzellen bilden Nervenzellen<br />
Eine sternförmige<br />
Gliazelle (Astrozyt)<br />
aus dem menschlichen<br />
<strong>Gehirn</strong>.<br />
Man nimmt an,<br />
das Astrozyten<br />
maßgeblich an der<br />
Bildung neuer<br />
Nervenzellen beteiligt<br />
sind.<br />
<strong>Forschung</strong> aktuell<br />
heimer’sche Erkrankung oder die<br />
Parkinson’sche Erkrankung (siehe<br />
»Können Stammzellen Parkinson-<br />
Kranke heilen«, Seite 57) wesentlich<br />
seltener vorkommen. Auf diesen<br />
Einwand gibt es keine schlüssige<br />
Antwort, allerdings <strong>ist</strong> auch nicht<br />
bekannt, ob die Alzheimer’sche Erkrankung<br />
nicht wesentlich häufiger<br />
wäre oder die Patienten in jüngerem<br />
Alter erkranken würden, wenn<br />
keine endogenen Reparaturmechanismen<br />
durch Stammzellen vorhanden<br />
wären. Einige Wissenschaftler<br />
Große sternförmige Hirnzellen<br />
(Astrozyten) können Stammzellen<br />
des <strong>Gehirn</strong>s dazu bringen, neue<br />
Nervenzellen zu bilden. Dies zeigten<br />
Fred Gage und seine Mitarbeiter<br />
vom amerikanischen Salk-Institut<br />
in La Jolla in Kalifornien. Sie<br />
ließen adulte Stammzellen gemeinsam<br />
mit anderen <strong>Gehirn</strong>zellen<br />
in Zellkulturen wachsen und<br />
stellten dabei fest, dass nur Astrozyten<br />
die Stammzellen zur Neubildung<br />
von Neuronen anregen<br />
konnten. Diese Fähigkeit war auf<br />
Astrozyten aus dem Hippocampus<br />
beschränkt, einer Hirnregion, die<br />
eng mit der Gedächtnisle<strong>ist</strong>ung<br />
und Emotionen verknüpft <strong>ist</strong>.<br />
Astrozyten aus dem Rückenmark<br />
stimulierten die Neubildung dagegen<br />
nicht. Darüber hinaus war<br />
zweifeln die endogene Reparaturfähigkeit<br />
des <strong>Gehirn</strong>s an. Deshalb<br />
transplantieren sie Zellen in das <strong>Gehirn</strong>,<br />
um <strong>Gehirn</strong>erkrankungen zu<br />
heilen. Wegen ihrer hohen Teilungsfähigkeit<br />
außerhalb des Organismus<br />
(in vitro) und ihrer Fähigkeit,<br />
viele unterschiedliche Zelltypen<br />
bilden zu können (Pluripotenz),<br />
favorisieren diese Wissenschaftler<br />
hierfür den Gebrauch von menschlichen<br />
embryonalen Stammzellen.<br />
In den zum Teil hitzig geführten<br />
Diskussionen über den Import<br />
diese so genannte Neurogenese<br />
besonders stark ausgeprägt bei<br />
Astrozyten aus dem <strong>Gehirn</strong> neugeborener<br />
Ratten und ließ mit zunehmenden<br />
Alter – wie beim<br />
Menschen – nach. Diese Ergebnisse<br />
nähren die Hoffnung, dass<br />
»neurogene« Astrozyten in der<br />
Nähe von Stammzellen Schäden<br />
nach einem Schlaganfall oder neurogenerativen<br />
Erkrankungen wie<br />
Alzheimer oder Parkinson mildern<br />
könnten.<br />
Astrozyten sind Bestandteil des<br />
Hüll- und Stützgewebes des <strong>Gehirn</strong>s<br />
und waren bisher als reines<br />
»Füllmaterial« angesehen worden.<br />
Inzwischen mehren sich die<br />
Hinweise, dass sie umfangreiche<br />
regulatorische Aufgaben wahrnehmen.<br />
menschlicher embryonaler Stammzellen<br />
wurde aber oft unterschlagen,<br />
dass auch diese Zellen – ganz<br />
abgesehen von den ethischen Bedenken,<br />
die mit ihrer Nutzung verbunden<br />
sind – erhebliche Nachteile<br />
aufweisen: Der Vorteil ihrer hohen<br />
Teilungsfähigkeit und Pluripotenz<br />
muss mit dem Nachteil »erkauft«<br />
werden, dass aus den transplantierten<br />
Zellen bösartige Tumoren heranreifen<br />
können. Undifferenzierte<br />
Zellen können auf eine Vielzahl von<br />
genetischen Programmen zugreifen;<br />
unter anderem auf solche, die die<br />
Tumorbildung fördern. Erst die genaue<br />
Kenntnis dieser Programme<br />
wird es ermöglichen, die Tumorbildung<br />
bei Stammzellen mehr oder<br />
weniger sicher zu verhindern.<br />
Unsere eigene Arbeitsgruppe am<br />
Neurologischen Institut in <strong>Frankfurt</strong><br />
am Main beschäftigt sich mit den<br />
Mechanismen, die die Aktivität von<br />
Stammzellen im adulten <strong>Gehirn</strong> regulieren.<br />
An Nagern konnte von<br />
anderen Arbeitsgruppen gezeigt<br />
werden, dass beispielsweise physische<br />
Aktivität, eine abwechslungsreiche<br />
Umgebung, aber auch ein<br />
Sauerstoffmangel im <strong>Gehirn</strong> die<br />
dort vorhandenen Stammzellen dazu<br />
anregen können, neue Nervenzellen<br />
zu bilden. Wir untersuchen<br />
derzeit, ob ein Protein, dessen Produktion<br />
sauerstoffabhängig <strong>ist</strong>, für<br />
diesen Prozess verantwortlich <strong>ist</strong>.<br />
Weiterhin gehen wir der Frage<br />
nach, ob nach einer erfolgten Läsion<br />
im <strong>Gehirn</strong> tatsächlich Zellen, die aus<br />
dem Knochenmark stammen, Reparaturaufgaben<br />
wahrnehmen.<br />
Diese <strong>Forschung</strong>sprojekte werden<br />
durch die Deutsche <strong>Forschung</strong>sgemeinschaft<br />
innerhalb des nationalen<br />
Schwerpunktprogramms 1109<br />
»Embryonale und gewebespezifische<br />
Stammzellen« gefördert. Zusammen<br />
mit Mitteln der Ludwig-<br />
Edinger-Stiftung stehen dafür in<br />
den nächsten fünf Jahren 1,5 Millionen<br />
Euro bereit.<br />
Keine leeren<br />
Heilsversprechungen<br />
Die Erforschung der körpereigenen<br />
Reparaturfähigkeit des <strong>Gehirn</strong>s<br />
durch endogene adulte Stammzellen<br />
– unabhängig davon, ob sie aus<br />
dem <strong>Gehirn</strong> selbst oder dem Knochenmark<br />
stammen – wird eine der<br />
wichtigsten Zukunftsaufgaben der<br />
modernen Neurowissenschaften<br />
darstellen. Allerdings sind noch viele<br />
Arbeiten in der Grundlagenfor-<br />
<strong>Forschung</strong> <strong>Frankfurt</strong> 3/2002
schung zu le<strong>ist</strong>en, bevor an eine<br />
Anwendung in der Therapie von<br />
Patienten mit Erkrankungen des<br />
Nervensystems gedacht werden<br />
sollte. <strong>Das</strong> mögliche Spektrum einer<br />
therapeutischen Anwendbarkeit <strong>ist</strong><br />
groß: Neben neurodegenerativen<br />
Bei kaum einer anderen Krankheit<br />
setzen Forscher und Patienten<br />
so viel Hoffnung in eine Therapie<br />
mit Stammzellen wie bei der Parkinson’schen<br />
Krankheit. An dieser<br />
auch als Schüttellähmung bekannten<br />
Erkrankung des zentralen<br />
Nervensystems leiden in Deutschland<br />
rund 250 000 Menschen. Sie<br />
<strong>ist</strong> bis heute unheilbar, aber nicht<br />
akut lebensbedrohlich. Die Symptome,<br />
darunter Muskelstarre, eine<br />
gebeugte Haltung und unkontrolliertes<br />
Zittern, können medikamentös<br />
behandelt werden. Die<br />
biochemische Ursache der Schüttellähmung<br />
<strong>ist</strong> bekannt: Nach dem<br />
Tod einer bestimmten Gruppe von<br />
Zellen im Mittelhirn fehlt der Nervenbotenstoff<br />
Dopamin. Dadurch<br />
wird die Signalübertragung zwischen<br />
den Nervenzellen gestört.<br />
Die Folge sind unkontrolliert zitternde<br />
und verkrampfte Muskeln.<br />
Mit Hilfe der Stammzelltherapie<br />
könnten neue Zellen in das abgestorbene<br />
Hirnareal gebracht werden,<br />
so der therapeutische Ansatz,<br />
und dort die Aufgabe der zerstörten<br />
Zellen übernehmen, die Dopaminsynthese.<br />
Ob dies funktioniert,<br />
<strong>ist</strong> jedoch noch völlig ungewiss.<br />
Entsprechende Versuche an<br />
Ratten, die Parkinson-Symptome<br />
zeigen, waren vielversprechend:<br />
Den Tieren wurden embryonale<br />
Stammzellen aus Mäusen ins <strong>Gehirn</strong><br />
gespritzt. Die Zellen siedelten<br />
Erkrankungen, die mit einem Verlust<br />
von Nervenzellen einhergehen,<br />
<strong>ist</strong> die Behandlung von Schlaganfall-Patienten,Schädel-Hirn-Verletzten<br />
und Patienten mit Hirntumoren<br />
denkbar. Umso wichtiger <strong>ist</strong><br />
es, keine leeren Heilsversprechun-<br />
Können Stammzellen Parkinson-Kranke heilen?<br />
An der Parkinson’schen Krankheit leiden auch zahlreiche Prominente: Zu ihnen<br />
gehören der frühere Boxweltme<strong>ist</strong>er Muhammed Ali und Papst Johannes Paul II.<br />
sich an, teilten sich und produzierten<br />
Dopamin, wodurch sich die<br />
Hirnfunktion und das Verhalten<br />
der Ratten messbar verbesserte.<br />
Diese Ergebnisse zeigen aber nur,<br />
dass das Verfahren prinzipiell<br />
funktioniert, denn bei rund einem<br />
Viertel der Ratten wuchsen die<br />
Zellen nicht an, bei weiteren 20<br />
Prozent bildeten sich tödliche<br />
krebsähnliche Zellklumpen. Auf<br />
die Schlüsselfrage: »Wie können<br />
embryonale Stammzellen so gelenkt<br />
werden, dass sie nützliches<br />
Gewebe schaffen, ohne unkontrolliert<br />
zu wuchern?« gibt es bisher<br />
keine Antwort.<br />
Eine andere Möglichkeit wäre<br />
es, Dopamin bildende Zellen aus<br />
abgetriebenen menschlichen Feten<br />
zur Therapie zu verwenden.<br />
Dies <strong>ist</strong> in Ländern wie Mexiko<br />
und den USA seit Ende der 1980er<br />
Jahre bereits klinische Praxis, birgt<br />
aber verschiedene Probleme: Zum<br />
einen <strong>ist</strong> es schwierig, die Zellen<br />
zu isolieren – der Embryo <strong>ist</strong> acht<br />
Wochen nach der Befruchtung<br />
nur wenige Zentimeter groß –,<br />
zum anderen sterben 90 bis 95<br />
Prozent der Zellen nach der Transplantation<br />
ab. Hier könnten embryonale<br />
Stammzellen des Menschen<br />
Abhilfe le<strong>ist</strong>en, vorausgesetzt,<br />
diese Zellen lassen sich in<br />
Dopamin bildende Zellen umwandeln<br />
und in der Zellkultur vermehren.<br />
Stammzellforschung<br />
gen zu wecken. Bei neu angedachten<br />
Therapiekonzepten wie der<br />
Stammzelltherapie vergehen bis zu<br />
einer erfolgreichen Therapie von<br />
Patienten häufig Jahre oder Jahrzehnte.<br />
In vielen Fällen erfüllen die<br />
Therapieergebnisse die hochgesteckten<br />
Erwartungen nicht. Die<br />
Geschichte sowohl der Krebstherapie<br />
als auch der Gentherapie sind<br />
hier sehr lehrreich. Die Zukunft wird<br />
zeigen, inwieweit Stammzellen zur<br />
Behandlung menschlicher Erkrankungen<br />
tatsächlich geeignet sind. ◆<br />
Der Autor<br />
Prof. Dr. Karlheinz Plate, 43, <strong>ist</strong> seit September<br />
2001 Direktor des Neurologischen<br />
Instituts (Edinger-Institut)<br />
am Universitätsklinikum<br />
der Johann<br />
Wolfgang <strong>Goethe</strong>-Universität<br />
sowie Geschäftsführer<br />
der Ludwig-Edinger-Stiftung.<br />
Plate, der von 1999<br />
bis 2001 als Leiter<br />
der Neuropathologie<br />
an der Erlanger Universität tätig war, <strong>ist</strong><br />
ein erfahrener Spezial<strong>ist</strong> in der Hirntumordiagnostik<br />
und auf dem Gebiet der<br />
stereotaktischen Hirnbiopsie. Der gebürtige<br />
Hesse, geboren in Ostheim bei Hanau,<br />
studierte von 1978 bis 1986 Medizin<br />
in Bochum, Marburg und Glasgow. Danach<br />
bildete er sich weiter zum Facharzt<br />
für Neuropathologie an den Universitätskliniken<br />
in Marburg und Zürich sowie am<br />
Max-Planck-Institut für Neurobiologie in<br />
Martinsried. Nach Auslandsaufenthalten<br />
in London, Southampton und San Francisco<br />
war er von 1995 bis 1999 leitender<br />
Oberarzt am Neurozentrum der Universitätsklinik<br />
Freiburg im Breisgau. Plate <strong>ist</strong><br />
Mitglied verschiedener Fachgesellschaften,<br />
Mitglied und Autor der Weltgesundheitsorganisation<br />
WHO zur Klassifizierung<br />
von Tumoren des zentralen und peripheren<br />
Nervensystems, Verbundskoordinator<br />
des Projektes »Angiogene Therapie« des<br />
Bundesmin<strong>ist</strong>eriums für Bildung und <strong>Forschung</strong><br />
sowie Projektleiter der Deutschen<br />
Krebshilfe. 1994 wurde er mit dem <strong>Forschung</strong>spreis<br />
der Hessischen Krebsgesellschaft<br />
und dem Adam-Preis der <strong>Goethe</strong>-<br />
Universität ausgezeichnet. Die wissenschaftlichen<br />
Arbeiten des Autors werden<br />
unterstützt durch die Schwerpunktprogramme<br />
1069 »Angiogenese: Molekulare<br />
Mechanismen und funktionelle Interaktionen«<br />
und 1109 »Embryonale und gewebespezifische<br />
Stammzellen: Regenerative<br />
Zellsysteme für einen Zell- und Gewebeersatz«<br />
der Deutschen <strong>Forschung</strong>sgemeinschaft,<br />
den Förderschwerpunkt<br />
»Therapie mit molekulargenetischen Methoden«<br />
des Bundesmin<strong>ist</strong>eriums für Bildung<br />
und <strong>Forschung</strong> sowie die Ludwig-<br />
Edinger-Stiftung, die Sturge-Weber-Foundation<br />
und die Deutsche Krebshilfe.<br />
<strong>Forschung</strong> <strong>Frankfurt</strong> 3/2002 57









![Unterwegs in physischen und virtuellen Welten [Barbara Lenz]](https://img.yumpu.com/22035353/1/184x260/unterwegs-in-physischen-und-virtuellen-welten-barbara-lenz.jpg?quality=85)