Haut- und Weichteilinfektionen: Zellulitis, Erysipel und ...
Haut- und Weichteilinfektionen: Zellulitis, Erysipel und ...
Haut- und Weichteilinfektionen: Zellulitis, Erysipel und ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
curriculum<br />
<strong>Haut</strong>- <strong>und</strong> <strong>Weichteilinfektionen</strong>:<br />
<strong>Zellulitis</strong>, <strong>Erysipel</strong> <strong>und</strong> nekrotisierende Fasziitis<br />
Stefano Bassetti a , Rein Jan Piso a , Peter Itin b<br />
a<br />
Medizinische Klinik, Kantonsspital Olten<br />
b<br />
Dermatologie, Universitätsspital Basel<br />
Quintessenz<br />
Die häufigsten Erreger der <strong>Zellulitis</strong> sind S. aureus <strong>und</strong> β-hämolysierende<br />
Streptokokken. Die häufigsten Erreger des <strong>Erysipel</strong>s sind β-hämolysierende<br />
Streptokokken.<br />
Bei einer eitrigen <strong>Zellulitis</strong> bei Patienten, die sich in einem Endemiegebiet<br />
aufgehalten haben (z.B. USA), müssen CA-MRSA als Erreger in Erwägung<br />
gezogen werden.<br />
Die initiale Markierung der Grenzen der <strong>Haut</strong>rötung bei <strong>Erysipel</strong> oder<br />
<strong>Zellulitis</strong> ist sehr wichtig für die Beurteilung des Verlaufs.<br />
Alarmzeichen, die auf eine nekrotisierende Fasziitis hinweisen können,<br />
sind: Diskrepanz zwischen starken Schmerzen <strong>und</strong> nur geringer <strong>Haut</strong>veränderung<br />
(im Initialstadium), ausgeprägtes Ödem, schwere systemische<br />
Infektzeichen, rasche Progredienz der <strong>Haut</strong>veränderungen, Blasenbildung,<br />
Anästhesie der <strong>Haut</strong>.<br />
Bei hohem Verdacht auf eine nekrotisierende Fasziitis muss sofort<br />
eine chirurgische Exploration erfolgen. Weil ein rasches Débridement für<br />
die Prognose entscheidend ist, muss auf präoperative bildgebende Untersuchungen<br />
aus Zeitgründen verzichtet werden.<br />
Stefano Bassetti<br />
Die Autoren haben<br />
keine finanzielle<br />
Unterstützung <strong>und</strong><br />
keine Interessenkonflikte<br />
im<br />
Zusammenhang<br />
mit diesem Beitrag<br />
deklariert.<br />
Eine <strong>Haut</strong>- oder Weichteilinfektion ist einer der häufigsten<br />
Gründe für Konsultationen in der Hausarztpraxis<br />
oder in Notfallstationen <strong>und</strong> für eine Hospitalisation.<br />
Zudem nimmt die Häufigkeit der ambulanten <strong>und</strong><br />
station ären Behandlungen von Patienten mit <strong>Haut</strong>- <strong>und</strong><br />
<strong>Weichteilinfektionen</strong> in einigen Regionen der Welt zu,<br />
wahrscheinlich wegen der Ausbreitung von ambulant<br />
erworbenen Methicillin-resistenten Staphylococcus aureus<br />
(«community-associated MRSA», CA-MRSA). In den<br />
USA werden mehr als 14 Millionen ambulante Konsultationen<br />
pro Jahr wegen <strong>Haut</strong>- <strong>und</strong> <strong>Weichteilinfektionen</strong><br />
registriert, mit mehr als 600 000 Hospitalisationen (3,7%<br />
aller Notfallhospitalisationen) [1]. Die Anzahl Hospitalisationen<br />
wegen dieser Infektionen nahm von 2000 bis<br />
2004 um 29% zu [2].<br />
Eine der ersten kontrollierten Studien zur Wirksamkeit<br />
einer antibakteriellen Substanz (Prontosil) wurde bei<br />
Patienten mit <strong>Erysipel</strong> durchgeführt [3]. Umso erstaunlicher<br />
ist es, dass heute die Empfehlungen zur Behandlung<br />
von <strong>Zellulitis</strong> <strong>und</strong> <strong>Erysipel</strong> immer noch auf wenig<br />
Evidenz basieren, wie auch eine neuere Cochrane-Review<br />
feststellen musste [4]. Bereits die Begriffe zur Beschreibung<br />
der <strong>Haut</strong>- <strong>und</strong> <strong>Weichteilinfektionen</strong> werden<br />
nicht einheitlich verwendet <strong>und</strong> führen oft zu Verwirrung.<br />
So werden zum Beispiel <strong>Erysipel</strong> <strong>und</strong> <strong>Zellulitis</strong> oft synonym<br />
gebraucht.<br />
Definitionen<br />
<strong>Zellulitis</strong>: Akute <strong>Haut</strong>infektion, die Epidermis, Dermis<br />
<strong>und</strong> subkutanes Gewebe betrifft. Als purulente <strong>Zellulitis</strong><br />
wird eine <strong>Zellulitis</strong> mit purulenter Sekretion definiert,<br />
ohne dass ein drainierbarer Abszess vorliegt. Der häufigste<br />
Erreger einer <strong>Zellulitis</strong> ist Staphylococcus aureus<br />
[5].<br />
<strong>Erysipel</strong>: Akute, oberflächliche <strong>Haut</strong>infektion, die auf<br />
Epidermis <strong>und</strong> Dermis beschränkt ist. Typisch ist die<br />
Mitbeteiligung der Lymphgefässe. Die grosse Mehrheit<br />
der <strong>Erysipel</strong>-Fälle wird durch β-hämolysierende Streptokokken<br />
verursacht.<br />
Nekrotisierende Fasziitis: Schwere, tiefe Infektion des<br />
subkutanen Gewebes mit rasch fortschreitender Nekrose<br />
des Fettgewebes <strong>und</strong> der Faszie. Auch die Muskeln können<br />
betroffen sein. Die darüberliegende <strong>Haut</strong> kann ausgespart<br />
bleiben [6–8].<br />
<strong>Zellulitis</strong><br />
Ätiologie der <strong>Zellulitis</strong><br />
Die häufigsten Erreger der <strong>Zellulitis</strong> sind S. aureus <strong>und</strong><br />
β-hämolysierende Streptokokken (meistens der Gruppe<br />
A [Streptococcus pyogenes], aber auch der Gruppe B, C<br />
<strong>und</strong> G). Eine neulich publizierte Arbeit analysierte die<br />
Daten von Studien, in denen der Erreger einer <strong>Zellulitis</strong><br />
mittels Nadelaspiration oder Stanzbiopsie gesucht wurde.<br />
In 51% der positiven Kulturen wurden S. aureus <strong>und</strong> nur<br />
in 27% β-hämolysierende Streptokokken der Gruppe A<br />
nachgewiesen [5]. Wenn Furunkel, Abszesse oder eine<br />
purulente Sekretion vorliegen, dann ist S. aureus noch<br />
häufiger.<br />
Inzwischen werden die meisten purulenten Zellulitiden<br />
in den USA durch CA-MRSA verursacht (59% der Fälle),<br />
während der Methicillin-empfindliche S. aureus in 17%<br />
<strong>und</strong> β-hämolysierende Streptokokken nur in 2,6% der<br />
Fälle nachgewiesen werden [6]. Auch in Europa wird<br />
eine zunehmende Inzidenz von Infektionen durch CA-<br />
MRSA registriert, allerdings mit grossen regionalen Unterschieden.<br />
Aus gewissen Zentren in Griechenland werden<br />
ähnliche Inzidenzraten wie in den USA berichtet,<br />
während in den nordeuropäischen Ländern CA-MRSA<br />
noch selten sind [9]. Im Gegensatz zu den USA, wo ein<br />
CA-MRSA-Klon überwiegt (USA 300), treten in Europa<br />
verschiedene CA-MRSA-Klone auf. Einige dieser Klone<br />
sind mit Tieren assoziiert, zum Beispiel Schweinen [9].<br />
In der Schweiz zeigte eine Studie, dass sich die Prävalenz<br />
von MRSA bei Schlachtschweinen von 2009 auf<br />
2010 fast verdreifacht hat (von 2% auf 5,9%) [10].<br />
Schweiz Med Forum 2013;13(35):672–677<br />
672
curriculum<br />
Die Prävalenz von CA-MRSA bei Patienten bleibt noch<br />
tief (in einer neueren Studie aus Luzern z.B. ≤5%), muss<br />
aber beobachtet werden [9, 11]. Bei Patienten mit engem<br />
Tierkontakt (z.B. Landwirte, Schlachthofmitarbeiter, Tierärzte)<br />
muss zudem die Möglichkeit einer MRSA-Infektion<br />
in Betracht gezogen werden.<br />
Oft entsteht eine <strong>Zellulitis</strong> oder ein <strong>Erysipel</strong> in der Umgebung<br />
einer <strong>Haut</strong>verletzung (Ulkus, Mykose, chirurgische<br />
oder traumatische W<strong>und</strong>e), die als Eintrittspforte<br />
für die Bakterien dient. Bei gewissen Expositionen kommen<br />
seltene Erreger als Ursache einer <strong>Zellulitis</strong> in<br />
Frage (Tab. 1 ).<br />
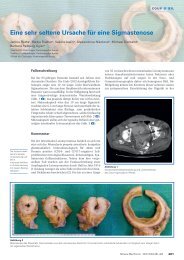
Abbildung 1<br />
<strong>Erysipel</strong> am Unterschenkel.<br />
Tabelle 1<br />
Erreger von <strong>Zellulitis</strong> oder von nodulären <strong>Haut</strong>infektionen bei besonderen Expositionen<br />
(adaptiert nach [7, 11]).<br />
Exposition oder Anamnese<br />
<strong>Zellulitis</strong> mit purulenter Sekretion,<br />
aus Endemiegebiet (z.B. USA)<br />
Traumatische Inokulation von Erde,<br />
penetrierende Verletzung mit Dornen<br />
Aufenthalt in den Tropen<br />
Trauma mit Wasserkontamination:<br />
Süsswasser<br />
Salzwasser<br />
Aquarium<br />
Bäder in Thermalbädern / Badewanne<br />
Kontakt mit Schweinen, Salzwasserfischen,<br />
Krabben <strong>und</strong> anderen Schalentieren,<br />
Geflügel (Metzger, Fischer, Hausfrauen)<br />
Bisse durch:<br />
Menschen<br />
Katzen<br />
H<strong>und</strong>e<br />
Ratten<br />
Kontakt mit Katzen<br />
Prädisponierende Erkrankungen:<br />
Immunosuppression<br />
(z.B. HIV, Transplantation)<br />
Leberzirrhose<br />
IV-Drogenkonsum<br />
Mögliche Erreger<br />
CA-MRSA<br />
Nicht-tuberkulöse Mykobakterien<br />
(z.B. Mycobacterium fortuitum, M. chelonae,<br />
M. ulcerans), Nocardia spp., Pilze<br />
Burkholderia pseudomallei (Melioidose),<br />
Chromoblastomycosis*, Chromobacterium<br />
violaceum<br />
Aeromonas hydrophila<br />
Vibrio vulnificus<br />
Mycobacterium marinum*<br />
(Aquarium-Granulom)<br />
Pseudomonas aeruginosa<br />
<strong>Erysipel</strong>othrix rhusiopathiae (<strong>Erysipel</strong>oid)<br />
Eikenella corrodens<br />
Pasteurella multocida<br />
P. multocida, Capnocytophaga canimorsus<br />
Streptobacillus moniliformis<br />
Bartonella henselae* (Katzenkratzkrankheit)<br />
Gramneg. Erreger (Enterobacteriaceae, P.<br />
aeruginosa), Nocardia spp., Cryptococcus<br />
neoformans<br />
Gramneg. Erreger, Campylobacter fetus,<br />
Vibrio vulnificus,<br />
Capnocytophaga canimorsus<br />
S. aureus, P. aeruginosa<br />
*verursachen in der Regel eher noduläre oder verruköse Läsionen.<br />
Klinik der <strong>Zellulitis</strong><br />
Typisch für eine <strong>Zellulitis</strong> ist eine schmerzhafte, sich<br />
rasch ausbreitende überwärmte Rötung mit Ödem. Im<br />
Gegensatz zum <strong>Erysipel</strong> sind die Ränder einer <strong>Zellulitis</strong><br />
nicht scharf demarkiert. Bei schwereren Verläufen können<br />
Blasen (gefüllt mit klarer Flüssigkeit) <strong>und</strong> kutane<br />
Hämorrhagien (Petechien, Ekchymosen) vorliegen.<br />
Falls eine eitrige Sekretion besteht, ist S. aureus der<br />
wahrscheinlichste Erreger [6–7]. Eine Krepitation bei<br />
der Palpation der Rötung weist auf eine Infektion durch<br />
gasbildende Bakterien hin (wie Anaerobier oder gramnegative<br />
Stäbchen), ein fauliger Geruch auf eine Infektion<br />
durch Anaerobier, ein süsslicher Geruch hingegen<br />
auf Pseudomonas oder Clostridien [13].<br />
Die <strong>Zellulitis</strong> durch Streptokokken der Gruppe A als Folge<br />
einer postoperativen W<strong>und</strong>infektion manifestiert sich<br />
sehr rasch innerhalb von 6 bis 48 St<strong>und</strong>en nach der<br />
Operation (ähnlich dem Gasbrand), während eine postoperative<br />
S. aureus-Infektion erst einige Tage nach der<br />
Operation auftritt. Systemische Zeichen der Infektion mit<br />
Fieber, Malaise <strong>und</strong> erhöhten Entzündungszeichen (Leukozytose,<br />
erhöhtes C-reaktives Protein) sind häufig <strong>und</strong><br />
bestehen teilweise bereits vor dem Auftreten der <strong>Haut</strong>veränderungen<br />
[6] (in unserer Erfahrung gilt das vor<br />
a llem beim <strong>Erysipel</strong>). Bei der unkomplizierten <strong>Zellulitis</strong><br />
können systemische Infektzeichen aber auch oft fehlen:<br />
Gemäss publizierten Fallserien wird Fieber nur in 26–<br />
67% der Fälle <strong>und</strong> eine Leukozytose mit erhöhter Blutsenkungsreaktion<br />
in ca. der Hälfte der Fälle berichtet [7].<br />
Wichtig für die klinische Beurteilung ist auch die Suche<br />
nach prädisponierenden Faktoren wie chronische venöse<br />
Insuffizienz (wahrscheinlich der häufigste Faktor),<br />
Lymphödem, periphere arterielle Verschlusskrankheit,<br />
Adipositas, Diabetes mellitus, Status nach Entfernung<br />
einer Vena saphena oder Status nach lokaler Bestrahlung.<br />
Zusätzlich sollen lokale Faktoren (Eintrittspforten)<br />
berücksichtigt werden: Ulcera, W<strong>und</strong>en, trockene <strong>Haut</strong><br />
mit Fissuren, chronische <strong>Haut</strong>erkrankungen (z.B. Ekzeme),<br />
Tinea pedis oder Unguis incarnatus [1, 7]. Die<br />
Differentialdiagnose der <strong>Zellulitis</strong> beinhaltet mehrere<br />
Erkrankungen (Tab. 2 ). Da <strong>Zellulitis</strong> <strong>und</strong> <strong>Erysipel</strong> am<br />
häufigsten die unteren Extremitäten betreffen, wird eine<br />
Stauungsdermatitis bei chronischer venöser Insuffizienz<br />
häufig fälschlicherweise als <strong>Zellulitis</strong> oder <strong>Erysipel</strong> diagnostiziert<br />
[1].<br />
Diagnostik<br />
In schwereren Fällen sollte neben den üblichen Laboruntersuchungen<br />
(Blutbild, CRP, Elektrolyte, Kreatinin)<br />
Schweiz Med Forum 2013;13(35):672–677 673
curriculum<br />
Tabelle 2<br />
Differentialdiagnose von <strong>Zellulitis</strong> <strong>und</strong> <strong>Erysipel</strong> (adaptiert nach [1, 6, 7, 13]).<br />
Krankheit<br />
Stauungsdermatitis<br />
Allergische Reaktion<br />
Kontaktdermatitis<br />
Toxische epidermale Nekrolyse<br />
Tiefe Venenthrombose<br />
Septische Arthritis oder Gicht<br />
Akute Bursitis<br />
Erythema migrans (Lyme disease)<br />
Nekrotisierende Fasziitis<br />
Herpes Zoster im Frühstadium (vor Auftreten der Bläschen)<br />
Herpes-simplex-Paronychie («herpetic whitlow»)<br />
Pyoderma gangraenosum<br />
Sweet-Syndrom (akute febrile neutrophile Dermatose)<br />
Eigenschaften<br />
Kein Fieber, keine Schmerzen; Rötung betrifft den ganzen Umfang<br />
des Unterschenkels <strong>und</strong> ist häufig bilateral. Juckreiz. Papulo-Vesikel<br />
Juckend, nicht schmerzhaft. Kein Fieber. Evtl. Insektenstich vorhanden<br />
Juckend, kein Fieber. Exposition mit Allergen / Irritans. Papulo-Vesikel<br />
Befall der Schleimhäute, Blasen, grossflächige Ablösung der <strong>Haut</strong>,<br />
Exposition mit Medikamenten<br />
In der Regel kein Fieber <strong>und</strong> keine Rötung der <strong>Haut</strong>. Schmerz in der Tiefe<br />
(meistens in der Wade). Schwellung der betroffenen Extremität, vermehrte<br />
Venenzeichnung im Stehen<br />
Gelenk betroffen. Schmerzen insbesondere bei Bewegung des Gelenks<br />
Typische Lokalisation über Patella oder Olecranon, oft mit palpabler Flüssigkeitskollektion.<br />
Bewegung im Gelenk nicht schmerzhaft<br />
Nicht schmerzhaft, breitet sich langsamer aus (weniger Fieber)<br />
Starke Schmerzen, ausgeprägtes Ödem <strong>und</strong> Fieber. Rasche Progression<br />
mit schweren systemischen Infektzeichen. Typisch ist die initiale Diskrepanz<br />
zwischen starken Schmerzen <strong>und</strong> nur geringen <strong>Haut</strong>veränderungen.<br />
Im weiteren Verlauf: <strong>Haut</strong>nekrosen, Blasenbildung (mit hämorrhagischem/<br />
violettem Inhalt)<br />
Schmerzen <strong>und</strong> Rötung treten vor den Bläschen auf. Hyperästhesie im<br />
betroffenen Areal<br />
Typische Lokalisation am Finger. Bläschen<br />
Zerfallende, schmierig belegte Ulzera, oft mit bläulich/schwarzer Verfärbung.<br />
Kultur für Bakterien typischerweise negativ. Oft bei Patienten mit entzündlicher<br />
Darmerkrankung. Sehr schmerzhaft<br />
Scharf demarkierte, erhabene Papeln, welche zu Plaques konfluieren.<br />
Oft bei Patienten mit hämatologischen Neoplasien<br />
auch die CK bestimmt werden. Ein erhöhter CK-Wert<br />
kann auf eine Muskelbeteiligung hinweisen (wie z.B. bei<br />
der nekrotisierenden Fasziitis oder einer bakteriellen<br />
Myositis). Der eindeutige Nachweis des Erregers einer<br />
<strong>Zellulitis</strong> oder eines <strong>Erysipel</strong>s ist schwierig. Blutkulturen<br />
sind in ≤5% der Fälle positiv [1, 6] <strong>und</strong> sollten deshalb<br />
nur in schweren Fällen <strong>und</strong> bei Patienten mit Fieber<br />
oder Immunsuppression durchgeführt werden [1]. Die<br />
Aspiration von Flüssigkeit für die bakteriologische Kultur<br />
aus dem fortschreitendem Rand der <strong>Haut</strong>läsion (mit einer<br />
dünnen Nadel, z.B. 22 G, gegebenfalls nach Injektion<br />
e iner geringen Menge steriler NaCl-Lösung 0,9%, die<br />
wieder aspiriert wird) ergibt ein positives Resultat je<br />
nach Studie in ≤5 bis ca. 40% der Fälle [6]. Die Kultur<br />
einer Stanzbiopsie ist in 20−30% der Fälle positiv [6].<br />
Die Kulturen des Abstrichs einer W<strong>und</strong>e oder eines Ulcus,<br />
welche mit einer <strong>Zellulitis</strong> oder einem <strong>Erysipel</strong> assoziiert<br />
sind, sind häufig positiv [1]. Allerdings ist es bei diesen<br />
Resultaten schwierig zu unterscheiden, ob es sich bei<br />
den nachgewiesenen Keimen um die ursächlichen Erreger<br />
oder nur um irrelevante, kolonisierende Bakterien<br />
handelt. Deswegen sollten mikrobiologische Proben nur<br />
nach Débridement der W<strong>und</strong>e entnommen werden <strong>und</strong><br />
wenn möglich mittels Biopsie oder Curetage [7].<br />
Eine mikrobiologische Diagnostik ist in den meisten,<br />
gewöhnlichen Fällen von <strong>Zellulitis</strong> <strong>und</strong> <strong>Erysipel</strong> nicht nötig.<br />
Sie sollte aber in ausgewählten Fällen durchgeführt<br />
werden, wie bei Patienten mit Immunsuppression, bei<br />
besonderer Exposition (z.B. Bissw<strong>und</strong>e, Wasserexposition,<br />
Tropenaufenthalt) oder bei fehlendem Ansprechen<br />
auf die empirische Antibiotikatherapie [7]. Die einfachste<br />
<strong>und</strong> von uns bevorzugte Untersuchung in einem ersten<br />
Schritt ist die oben beschriebene Aspiration aus dem<br />
Rand der <strong>Haut</strong>läsion. Eine Aspiration mit Kultur sollte<br />
auch durchgeführt werden aus Blasenflüssigkeit oder<br />
wenn im Bereich der <strong>Haut</strong>läsion eine Fluktuation palpabel<br />
ist. Die Sonographie der Weichteile ist eine sehr<br />
hilfreiche Methode, um rasch klinisch nicht manifeste<br />
Abszesse im Bereich der <strong>Haut</strong>veränderung zu identifizieren,<br />
die drainiert werden müssen [14].<br />
Therapie<br />
Die Ausdehnung der <strong>Haut</strong>rötung muss initial klar markiert<br />
werden, um Verlauf <strong>und</strong> Ansprechen auf die<br />
T herapie beurteilen zu können. Entsprechend dem Erregerspektrum<br />
muss die Antibiotikatherapie gegen Staphylococcus<br />
aureus <strong>und</strong> Streptokokken gut wirksam<br />
sein. In bestimmten Situationen (z.B. diabetischer Fuss<br />
mit <strong>Zellulitis</strong>, die auf die Behandlung mit Amoxicillin/<br />
Clavulansäure nicht anspricht, oder Neutropenie) muss<br />
die Therapie auch gegen gramnegative Bakterien gerichtet<br />
sein. Mögliche empirische Antibiotikatherapien<br />
für eine unkomplizierte <strong>Zellulitis</strong> sind in Tabelle 3<br />
angegeben. In den komplizierten <strong>Zellulitis</strong>-Fällen, bei<br />
denen mit gramnegative Erregern <strong>und</strong> allenfalls auch<br />
Pseudomonas aeruginosa zu rechnen ist (z.B. schwere<br />
<strong>Zellulitis</strong> bei diabetischem Fuss, Neutropenie), werden<br />
Breitspektrumantibiotika eingesetzt, wie z.B. Piperacillin/<br />
Schweiz Med Forum 2013;13(35):672–677 674
curriculum<br />
Tabelle 3<br />
Auswahl von möglichen empirischen Antibiotikatherapien für die unkomplizierte<br />
<strong>Zellulitis</strong>; zusätzlich muss immer die lokale Resistenzlage berücksichtigt werden<br />
(adaptiert nach [1, 6, 7, 13, 15]).<br />
<strong>Zellulitis</strong> ohne besondere Risikofaktoren<br />
oder Exposition<br />
Bei Penicillin-Allergie (nur Exanthem)<br />
Bei Penicillin-Allergie mit Anaphylaxie<br />
<strong>Zellulitis</strong> mit Verdacht auf CA-MRSA<br />
(z.B. eitrige <strong>Zellulitis</strong> aus Endemiegebiet<br />
wie USA)<br />
Amoxicillin/Clavulansäure<br />
3 × 625 mg/Tag p.o.<br />
Amoxicillin/Clavulansäure<br />
3 × 1,2–2,2 g/Tag i.v.<br />
Cefuroximaxetil 2 × 500 mg/Tag p.o.<br />
Cefazolin 3 × 1 g/Tag i.v.<br />
Clindamycin 3 × 300 (–600) mg/Tag p.o.<br />
Clindamycin 3 × 600 mg/Tag i.v.<br />
Clarithromycin 2 × 500 mg/Tag p.o.<br />
Clindamycin 3 × 300 (–600) mg/Tag p.o.<br />
Trimethoprim/Sulfamethoxazol 160/800 mg<br />
1 bis 2 Tbl. 2×/Tag p.o.<br />
Doxycyclin 2 × 100 mg/Tag p.o.<br />
(kontraindiziert bei Schwangeren<br />
<strong>und</strong> Kindern ≤8 Jahre)<br />
Vancomycin 15 mg/kg i.v. 12-stündlich<br />
Tazobactam, Imipenem oder Meropenem. Falls im Verlauf<br />
ein Erreger identifiziert wird, muss die Antibiotika-<br />
Therapie entsprechend angepasst werden.<br />
Bei einer Infektion durch Streptokokken (sowie beim<br />
t ypischen <strong>Erysipel</strong>) ist Penicillin G die parenterale Therapie<br />
der Wahl (z.B. 4 × 2,5 Mio. E/Tag i.v.). Für die orale<br />
Therapie bevorzugen wir Amoxicillin (z.B. 3 × 500 mg/<br />
Tag p.o.), weil es im Gegensatz zum Penicillin V eine<br />
bessere Bioverfügbarkeit hat <strong>und</strong> mit den Mahlzeiten<br />
eingenommen werden kann, was die Compliance verbessert.<br />
Für den Entscheid, ob ein Patient oral oder parenteral<br />
behandelt werden muss, <strong>und</strong> ob eine Hospitalisation<br />
notwendig ist, werden in der Literatur Klassifikationssysteme<br />
diskutiert [1]. Gr<strong>und</strong>sätzlich hängt dieser Entscheid<br />
ab vom Schweregrad der systemischen Infektion<br />
(Zeichen einer Sepsis, Hypotension, Verwirrung), vom<br />
Lokalbef<strong>und</strong> (Ausdehnung, rasche Progredienz, Blasen<br />
<strong>und</strong>/oder Nekrosen, eitrige W<strong>und</strong>e, die chirurgisch saniert<br />
werden muss), von der Topographie <strong>und</strong> von den<br />
Komorbiditäten (Niereninsuffizienz, Diabetes mellitus,<br />
periphere arterielle Verschlusskrankheit, chronische<br />
venöse Insuffizienz, Immunsuppression).<br />
In den ersten 24 St<strong>und</strong>en nach Beginn der Antibiotikatherapie<br />
kommt es bei einigen Patienten zu einer Verschlechterung<br />
des lokalen Bef<strong>und</strong>s mit Zunahme der<br />
lokalen <strong>Haut</strong>entzündung [6, 13]. Das weist nicht unbedingt<br />
auf eine unwirksame Antibiotikatherapie hin, sondern<br />
kann lediglich Ausdruck sein einer entzündlichen<br />
Reaktion auf die Freisetzung von bakteriellen Antigenen,<br />
die durch die Zerstörung der Bakterien entstehen.<br />
Die Dauer der Antibiotikatherapie ist nicht klar definiert<br />
<strong>und</strong> hängt vom klinischen Ansprechen ab. Bei gutem<br />
Verlauf wird meistens eine Therapiedauer zwischen 5<br />
<strong>und</strong> 10 Tagen empfohlen oder es wird vorgeschlagen,<br />
die Antibiotika für drei Tage nach Abklingen der akuten<br />
Entzündungszeichen weiter zu verabreichen [7]. Eine<br />
randomisierte, plazebokontrollierte Studie (allerdings<br />
mit Levofloxacin) hat gezeigt, dass bei unkomplizierter<br />
<strong>Zellulitis</strong> eine fünftägige Therapie gleich wirksam ist wie<br />
eine zehntägige Therapie [16].<br />
Eine wichtige <strong>und</strong> oft unterschätzte zusätzliche therapeutische<br />
Massnahme ist die Hochlagerung der befallenen<br />
Extremität. Damit werden das Ödem <strong>und</strong> Entzündungsmediatoren<br />
rascher drainiert <strong>und</strong> die Heilung wird<br />
beschleunigt [6]. Massnahmen zur lokalen Kühlung (z.B.<br />
Umschläge mit Alkohol-Wickeln) werden als angenehm<br />
empf<strong>und</strong>en. Bei Patienten mit Lymphödem oder chronischer<br />
venöser Insuffizienz sollten Kompressionsverbände<br />
appliziert werden [13]. Auch andere prädisponierende<br />
Faktoren (z.B. eine Tinea pedis) müssen behandelt<br />
werden [6].<br />
<strong>Erysipel</strong><br />
Ein <strong>Erysipel</strong> wird fast immer durch beta-hämolysierende<br />
Streptokokken (meistens der Gruppe A, aber auch der<br />
Gruppe C oder G) verursacht, selten durch Streptokokken<br />
der Gruppe B oder S. aureus [6].<br />
Klinik <strong>und</strong> Diagnostik<br />
Die Klinik entspricht mehrheitlich derjenigen der <strong>Zellulitis</strong>.<br />
Im Gegensatz zur <strong>Zellulitis</strong> ist das Erythem aber<br />
scharf begrenzt <strong>und</strong> flammend rot. Typisch für das <strong>Erysipel</strong><br />
ist auch die ausgeprägte Beteiligung des lymphatischen<br />
Systems mit einer Lymphangitis <strong>und</strong> schmerzhaften<br />
regionalen Lymphknoten. Die <strong>Haut</strong>läsionen<br />
können erhaben sein. Ein schmetterlingförmiges<br />
Gesichtserysipel ist eine klassische Manifestation dieser<br />
Infektion. Die Beine sind aber heute die häufigste Lokalisation<br />
[6]. Der wahrscheinlich wichtigste prädisponierende<br />
Faktor (insbesondere bei Rezidiven) ist ein Lymphödem,<br />
das wiederum durch rezidivierende <strong>Erysipel</strong>e<br />
mit Schädigung des lymphatischen Systems begünstigt<br />
<strong>und</strong> unterhalten wird, so dass es zu einem Teufelskreis<br />
kommt.<br />
Die Diagnostik beim <strong>Erysipel</strong> entspricht derjenigen der<br />
<strong>Zellulitis</strong>.<br />
Therapie<br />
Die Therapie wird wie bei der <strong>Zellulitis</strong> durchgeführt.<br />
Theoretisch wäre eine Antibiotikatherapie nur gegen<br />
Streptokokken (mit Penicillin G oder Amoxicillin) ausreichend,<br />
weil diese Bakterien fast immer die Erreger<br />
eines <strong>Erysipel</strong>s sind. Klinisch ist es aber vor allem im<br />
Anfangsstadium meistens unmöglich zu unterscheiden,<br />
ob es sich um eine <strong>Zellulitis</strong> oder ein <strong>Erysipel</strong> handelt,<br />
so dass wir <strong>und</strong> viele Kliniker in der Regel Antibiotika<br />
einsetzen, die auch gegen S. aureus wirken (Tab. 3) [6].<br />
Die Therapie kann angepasst werden, wenn Streptokokken<br />
durch mikrobiologische Untersuchungen als<br />
Erreger identifiziert werden oder wenn Klinik <strong>und</strong> Verlauf<br />
typisch für ein <strong>Erysipel</strong> sind.<br />
Bei rezidivierendem <strong>Erysipel</strong> sind die wichtigsten Massnahmen<br />
die Sanierung der Eintrittspforten (z.B. Tinea<br />
pedis) <strong>und</strong> die Behandlung der prädisponierenden Erkrankung,<br />
insbesondere eines chronischen Lymphödems<br />
(Kompressionsstrümpfe, Behandlung von <strong>Haut</strong>läsionen,<br />
gute <strong>Haut</strong>pflege). Der Stellenwert einer antibiotischen<br />
Langzeitprophylaxe ist nicht eindeutig geklärt. Eine neue<br />
Schweiz Med Forum 2013;13(35):672–677 675
curriculum<br />
dreijährige Studie zeigte, dass bei Patienten mit Status<br />
nach ≥2 Episoden eine Prophylaxe mit niedrig dosiertem<br />
Penicillin V (2 × 250 mg/Tag p.o.) während eines<br />
Jahres die Rezidivrate in diesem Jahr signifikant von<br />
37% (in der Plazebogruppe) auf 22% reduzierte («number<br />
needed to treat» zur Vermeidung einer Episode:<br />
4−9). Dieser Effekt verschwand aber nach Absetzen des<br />
Penicillins, so dass es unklar bleibt, wie lange eine solche<br />
Prophylaxe durchgeführt werden müsste [17]. Zur<br />
Interpretation dieser Studie muss noch angemerkt werden,<br />
dass die Autoren den Begriff <strong>Zellulitis</strong> als Synonym<br />
für <strong>Erysipel</strong> benützen [18].<br />
Eine (allerdings nicht untersuchte) Alternativstrategie<br />
bei Patienten mit rezidivierendem <strong>Erysipel</strong> ist die selbstinitiierte<br />
Antibiotikabehandlung durch den Patienten,<br />
sobald sich die ersten Symptome eines Rezidivs manifestieren.<br />
Dadurch sollen Dauer <strong>und</strong> Schweregrad der<br />
neuen Episode reduziert werden [6].<br />
Nekrotisierende Fasziitis<br />
Die nekrotisierende Fasziitis ist mit einer hohen Mortalität<br />
assoziiert (20–40%), die nur durch eine frühzeitige<br />
Diagnose <strong>und</strong> aggressive Therapie reduziert werden<br />
kann [19].<br />
Ätiologie<br />
Nach mikrobiologischen Kriterien werden zwei Hauptformen<br />
von nekrotisierender Fasziitis unterschieden [20]:<br />
1. Nekrotisierende Fasziitis Typ 1: die häufigste Form<br />
(ca. 80% der Fälle). Es handelt sich um eine polymikrobielle<br />
Infektion (meistens ≥4 Bakterien) durch<br />
Anaerobier (z.B. Bacteroides, Peptostreptococcus<br />
spp.) <strong>und</strong> aerobe Bakterien wie Streptokokken <strong>und</strong><br />
Enterobacteriaceae (z.B. E. coli, Enterobacter, Klebsiella,<br />
Proteus). Die Fournier-Gangrän ist eine nekrotisierende<br />
Fasziitis Typ 1 im Genital- <strong>und</strong> Perineum-<br />
Bereich.<br />
2. Nekrotisierende Fasziitis Typ 2: monomikrobielle<br />
Form. Verursacht durch beta-hämolysierende Streptokokken<br />
der Gruppe A (Streptococcus pyogenes),<br />
seltener auch durch S. aureus <strong>und</strong>, bei entsprechender<br />
Exposition, durch Vibrio vulnificus (Salzwasser,<br />
Meeresfrüchte) oder Aeromonas hydrophila (Süsswasser).<br />
Staphylokokken <strong>und</strong> Streptokokken können<br />
gleichzeitig vorkommen [6]. Bei Infektionen mit S.<br />
pyogenes oder S. aureus tritt in ca. 50% der Fälle<br />
auch ein «toxic shock syndrome» auf.<br />
Begünstigende Faktoren für eine nekrotisierende Fasziitis<br />
sind unter anderem Diabetes mellitus, Adipositas,<br />
periphere arterielle Verschlusskrankheit, chronische<br />
Niereninsuffizienz, Alkoholabusus, Operationen, Traumen<br />
<strong>und</strong> <strong>Haut</strong>verletzungen. Die <strong>Haut</strong>verletzungen können<br />
(insbesondere beim Typ 2) auch sehr gering sein (z.B.<br />
Insektenstich) [20].<br />
Klinik<br />
Typisch ist die Präsentation mit starken Schmerzen,<br />
Ödem, Fieber <strong>und</strong> rascher Progression des Lokalbef<strong>und</strong>s<br />
mit Verschlechterung des Allgemeinzustands <strong>und</strong> Zeichen<br />
der Sepsis. Es gibt aber auch subakute Verläufe<br />
über Tage hinweg, mit einer plötzlichen akuten Verschlechterung,<br />
nachdem die Infektion eine gewisse<br />
Schwelle überschritten hat [21]. Initial sind die sichtbaren<br />
<strong>Haut</strong>veränderungen (z.B. Rötung) typischerweise<br />
gering. Diese Diskrepanz zwischen stärksten Schmerzen<br />
<strong>und</strong> «unverhältnismässig» geringen <strong>Haut</strong>veränderungen<br />
ist wahrscheinlich das wichtigste Zeichen, das an eine<br />
nekrotisierende Fasziitis denken lassen muss. Auch ein<br />
ausgeprägtes Ödem mit holzartiger Verhärtung des subkutanen<br />
Gewebes kann hinweisend sein [6]. Die Zerstörung<br />
der kutanen Nerven durch die Nekrose im subkutanen<br />
Gewebe führt manchmal zu einer Anästhesie der<br />
darüberliegenden <strong>Haut</strong>. Im weiteren Verlauf kommt es<br />
zu einer raschen Ausbreitung der Rötung, die fleckförmig-inhomogen<br />
wird <strong>und</strong> sich dunkelrot bis bläulich-livid<br />
verfärbt. Später können Blasen mit hämorrha gischem<br />
Inhalt, <strong>Haut</strong>nekrosen <strong>und</strong> eine Krepitation bei der Palpation<br />
auftreten. Ohne frühzeitige chirurgische Intervention<br />
kommt es zum Schock mit Multiorgan versagen.<br />
Diagnostik<br />
Es ist schwierig, frühzeitig eine nekrotisierende Fasziitis<br />
zu diagnostizieren <strong>und</strong> von einer «banalen» <strong>Zellulitis</strong><br />
oder einem <strong>Erysipel</strong> zu unterscheiden, weil die pathognomonischen<br />
klinischen Zeichen initial fehlen. Merkmale,<br />
die auf eine nekrotisierende Fasziitis hinweisen,<br />
sind:<br />
− Starke Schmerzen, die unverhältnismässig stark<br />
erscheinen in Anbetracht von nur geringen oder<br />
sogar fehlenden <strong>Haut</strong>veränderungen<br />
− Schwere systemische Symptome (Fieber, Leukozytose,<br />
Hypotonie)<br />
− Rasche Ausbreitung der Rötung, auch unter Antibiotikatherapie<br />
(deswegen ist zur Beurteilung des Verlaufs<br />
die initiale Markierung der Rötung essentiell)<br />
− Ödem, das die Bef<strong>und</strong>grenzen überschreitet<br />
− Blasen mit hämorrhagischem Inhalt<br />
− <strong>Haut</strong>nekrosen [6].<br />
Bei Verdacht auf eine nekrotisierende Fasziitis muss der<br />
Patient notfallmässig für die sofortige chirurgische Exploration<br />
zugewiesen werden. Die Diagnose beruht in<br />
erster Linie auf der klinischen Beurteilung <strong>und</strong> wird<br />
chirurgisch bestätigt, weil die Zusatzuntersuchungen<br />
(Labor, Radiologie) eine ungenügende Sensitivität <strong>und</strong><br />
Spezifität haben. Da die Prognose entscheidend vom raschen<br />
radikalen Débridement abhängig ist, darf keine<br />
Zeit wegen bildgebenden Untersuchungen verloren gehen,<br />
<strong>und</strong> die Indikation zur chirurgischen Exploration<br />
muss grosszügig gestellt werden. Dabei wird zuerst<br />
eine kleine exploratorische Inzision durchgeführt. Typische<br />
intraoperative Zeichen der nekrotisierenden Fasziitis<br />
sind Verlust der normalen Konsistenz der Faszie<br />
bei der Dissektion mit dem Finger, matte, grau gefärbte<br />
Faszie mit Nekrosen, Nekrosen des subkutanen Gewebes,<br />
fehlende Blutung bei der Dissektion, fauliger Geruch<br />
sowie bräunliche, spülwasserfarbene («dish water») Sekretion.<br />
Selbst bei tiefer Dissektion findet sich typischerweise<br />
kein richtiger Eiter [6]. Intraoperativ werden<br />
G e webebiopsien für Gram-Präparat <strong>und</strong> Kulturen entnommen.<br />
Schweiz Med Forum 2013;13(35):672–677 676
curriculum<br />
Tabelle 4<br />
Laboratory Risk Indicator for Necrotizing Fasciitis (LRINEC) Score<br />
[23].<br />
Variable<br />
C-reaktives Protein (mg/l)<br />
135 0<br />
110–135 1<br />
10 1<br />
Score<br />
Bei einem Cut-off von ≥6 Punkten hat der Score ein PPV von 92%<br />
<strong>und</strong> ein NPV von 96%. Diese Werte konnten aber in anderen<br />
Validierungsstudien nicht bestätigt werden.<br />
Laboruntersuchungen<br />
Wall et al. zeigten in einer retrospektiven Studie, dass<br />
die Kombination einer Leukozytenzahl ≤15,4 G/l <strong>und</strong><br />
eines Serum-Natriums ≥135 mmol/l das Vorliegen einer<br />
nekrotisierenden Fasziitis praktisch ausschliesst (negativ<br />
prädiktiver Wert [NPV] 99%). Umgekehrt eignet sich die<br />
Kombination dieser Parameter aber nicht, um die Krankheit<br />
zu diagnostizieren (positiv prädiktiver Wert [PPV]<br />
26%) [22]. Ein Score aus sechs Laborparametern<br />
(LRINEC, Tab. 4 ) zeigte in der Originalbeschreibung<br />
einen hohen PPV <strong>und</strong> NPV für die Diagnose einer nekrotisierenden<br />
Fasziitis [23]. Aber auch dieser Score basiert<br />
auf einer retrospektiven Analyse <strong>und</strong> konnte durch<br />
andere Studien nicht validiert werden [19, 20, 24].<br />
Bildgebende Untersuchungen<br />
Wenn die Diagnose unklar, der Patient stabil <strong>und</strong> eine<br />
nekrotisierende Fasziitis nicht sehr wahrscheinlich ist,<br />
wird eine Bildgebung durchgeführt. Das MRI gilt meistens<br />
als Untersuchung der Wahl (Sensitivität 80−90%).<br />
Das CT hat eine Sensitivität um 80%. Die Spezifität beider<br />
Methoden ist aber gering (MRI: ca. 50−55%, CT noch<br />
tiefer), auch wenn Untersuchungen mit neueren CT-<br />
Geräten eine verbesserte Spezifität zeigen [20].<br />
Therapie<br />
Der Gr<strong>und</strong>pfeiler der Behandlung der nekrotisierenden<br />
Fasziitis ist das frühestmögliche, radikale chirurgische<br />
Débridement mit vollständiger Entfernung des nekrotischen<br />
Gewebes <strong>und</strong> der nekrotischen Faszie. Die meisten<br />
Patienten müssen nach 24–36 St<strong>und</strong>en <strong>und</strong> dann täglich<br />
für ein Nachdébridement wieder operiert werden, bis<br />
alle Nekrosen entfernt sind [6]. Zusätzlich müssen die<br />
Patienten intensivmedizinisch monitorisiert <strong>und</strong> behandelt<br />
werden, insbesondere wegen des Volumenmanagements.<br />
Die empirische Antibiotikatherapie besteht aus einem<br />
Breitspektrum-Antibiotikum wie Imipenem/Cilastatin<br />
(4 × 500 mg/Tag i.v.), Meropenem (3 × 1 g/Tag i.v.) oder<br />
Piperacillin/Tazobactam (3 × 4,5 g/Tag i.v.) in Kombination<br />
mit Clindamycin (3 × 900 mg/Tag i.v.). Das Clindamycin<br />
wird hinzugefügt, weil es bei einem hohen<br />
Streptococcus pyogenes-Inoculum besser als Betalaktam-Antibiotika<br />
wirkt («Eagle Effekt») <strong>und</strong> weil es die<br />
bakterielle Toxinsynthese hemmt. Nach Identifikation<br />
der Erreger wird die Antibiotikatherapie angepasst.<br />
Die adjuvante Verabreichung von i.v. Immunglobulinen<br />
(IVIG) bei Patienten mit toxischem Schocksyndrom<br />
scheint einen positiven Effekt zu haben, obwohl dieser<br />
bis jetzt nicht eindeutig belegt werden konnte. Die Behandlung<br />
mit IVIG soll deshalb auch bei Patienten mit<br />
nekrotisierender Fasziitis durch Streptokokken oder S.<br />
aureus <strong>und</strong> schwerer Sepsis in Erwägung gezogen werden<br />
[6, 20].<br />
Die Daten zur adjuvanten hyperbaren Sauerstoff-Therapie<br />
sind widersprüchlich <strong>und</strong> der Stellenwert dieser<br />
Behandlung für die nekrotisierende Fasziitis ist umstritten<br />
[20].<br />
Danksagung:<br />
Die Autoren danken Herrn Dr. H. Lanter, Facharzt für Innere Medizin,<br />
Olten, für die kritische Durchsicht des Manuskripts.<br />
Korrespondenz:<br />
Prof. Dr. med. Stefano Bassetti<br />
Medizinische Klinik<br />
Kantonsspital Olten<br />
Baslerstrasse 150<br />
CH-4600 Olten<br />
stefano.bassetti[at]spital.so.ch<br />
Empfohlene Literatur<br />
– Chira S, Miller LG. Staphylococcus aureus is the most common identified<br />
cause of cellulitis: a systematic review. Epidemiol Infect.<br />
2010;138:313–7.<br />
– Stevens DL, Bisno AL, Chambers HF, Everett ED, Dellinger P, Goldstein<br />
EJC et al. Practice guidelines for the diagnosis and management of<br />
skin and soft-tissue infections. Clin Infect Dis. 2005;41:1373–406.<br />
– G<strong>und</strong>erson CG. Cellulitis: definition, etiology and clinical features.<br />
Am J Med. 2011;124:1113–22.<br />
– Thomas KS, Crook AM, Nunn AJ, Foster KA, Mason JM, Chalmers JR,<br />
et al. Penicillin to prevent recurrent leg cellulitis. N Engl J Med.<br />
2013;368:1695–703.<br />
– Ustin JS, Malangoni MA. Necrotizing soft-tissue infections. Crit Care<br />
Med. 2011;39:2156–62.<br />
Die vollständige nummerierte Literaturliste finden Sie unter<br />
www.medicalforum.ch.<br />
Schweiz Med Forum 2013;13(35):672–677 677